Cell:新型mRNA癌症疫苗,只需一针,在人类脑肿瘤患者中迅速激活抗肿瘤免疫反应
mRNA技术因为在新冠疫苗中的成功应用而受到广泛关注,对于预防性疫苗而言,mRNA通过表达来自病原体的蛋白来诱导免疫反应。此外,还有一些临床研究使用mRNA表达癌细胞的抗原来诱导免疫反应,用作癌症疫苗。但这些癌症免疫疗法 仍然受到抗原性差和抑制性肿瘤微环境 (TME)的限制。
2024年5月1日,佛罗里达大学的研究人员在国际顶尖学术期刊 Cell 上发表了题为: RNA aggregates harness the danger response for potent cancer immunotherapy 的研究论文。
该研究开发了一种 新型mRNA癌症疫苗 ,基于 “洋葱状”多层RNA-脂质颗粒聚集体 ( LPA ) ,以显著增强肿瘤mRNA抗原的装载和免疫原性。 在 自发晚期神经胶质瘤的宠物犬中,RNA-LPA显著延长了其生存期并重新编程了肿瘤微环境 (TME) 。
该研究还在 4名成年患者中进行了首次人体试验,用于治疗最具攻击性和致命性的脑肿瘤—— 胶质母细胞瘤 ,该mRNA癌症疫苗在注射后迅速重新编程了患者的免疫系统, 引发了细胞因子/趋化因子的释放、免疫激活/转运,并在胶质母细胞瘤患者中引发了特异性免疫反应。 这些数据支持RNA-LPA作为一种同时重新编程TME并引发快速持久癌症免疫疗法的新技术。
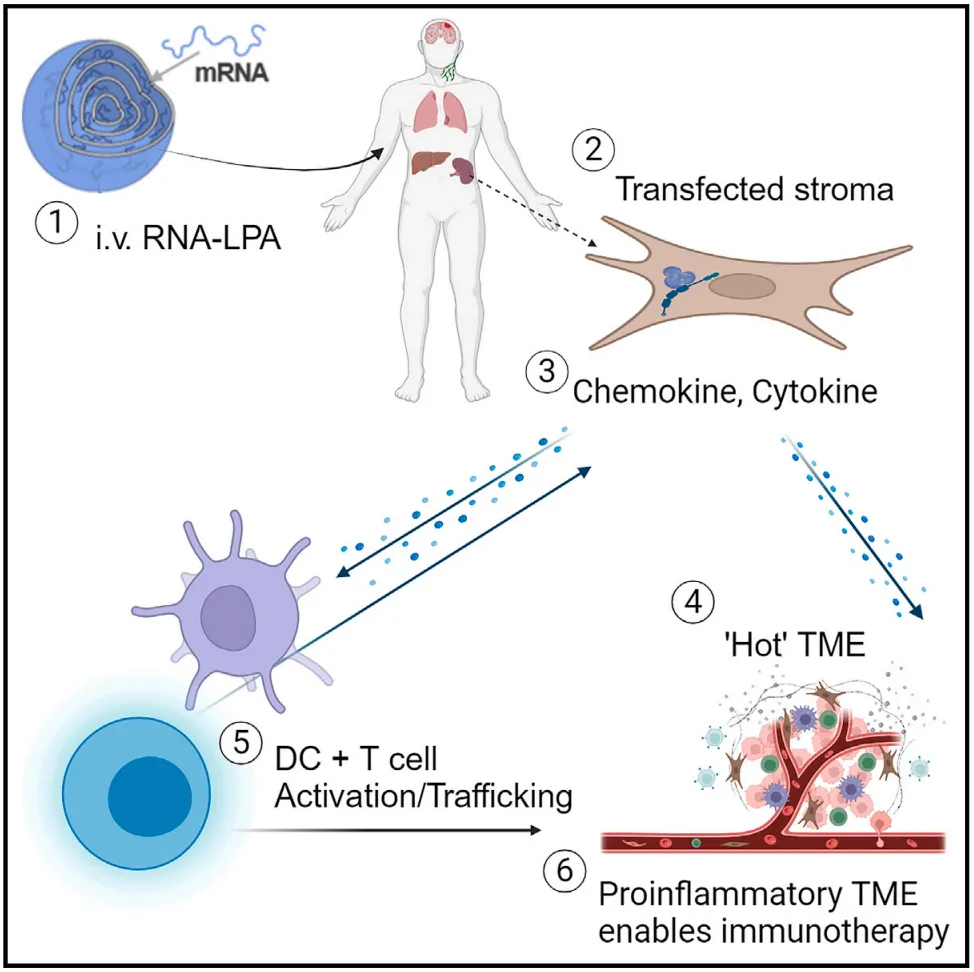
该论文的通讯作者 Elias Sayour 教授表示 ,该研究开发了一种“ 洋葱样 ”的多层RNA- 脂质颗粒聚集体 (Lipid Particle Aggregate,LPA) ,像洋葱一样具有多层结构,从而 大大增强肿瘤mRNA抗原的有效载荷包装和免疫原性。
相比单层的LNP递送的mRNA,多层的LPA递送的mRNA能够更深刻地 提醒免疫系统识别肿瘤抗原, 通过静脉注射后,能够迅速激发免疫系统对肿瘤的强烈排斥反应, 在不到48小时的时间里,就可以观察到肿瘤从免疫“冷肿瘤”状态重编程为“热肿瘤 ”。
这项研究开始于7年前,研究团队从小鼠模型开始,之后与 佛罗里达大学兽医学院的研究人员合作, 在10只自发患上 晚期神经胶质瘤 且没有其他治疗选择的宠物狗进行了试验 。经过治疗的 宠物狗的 中位生存期 为139天,而 患上 晚期神经胶质瘤 的中位生存期仅30-60天。 在使用 个性化mRNA癌症疫苗治疗了自发脑肿瘤的宠物狗后, Elias Sayour 团队获得了美国FDA的临床试验批准,以治疗人类胶质母细胞瘤患者 。
在首批接受治疗的4名成年患者中,研究团队从每个患者自己的手术切除的肿瘤中提取mRNA,然后将mRNA扩增并包装在新设计的生物相容性脂质纳米颗粒—— 脂质颗粒聚集体 (LPA) 中。这种个性化 mRNA癌症疫苗在注射到患者体内后,会被免疫系统识别为危险肿瘤,从而激活免疫系统抗肿瘤反应 。
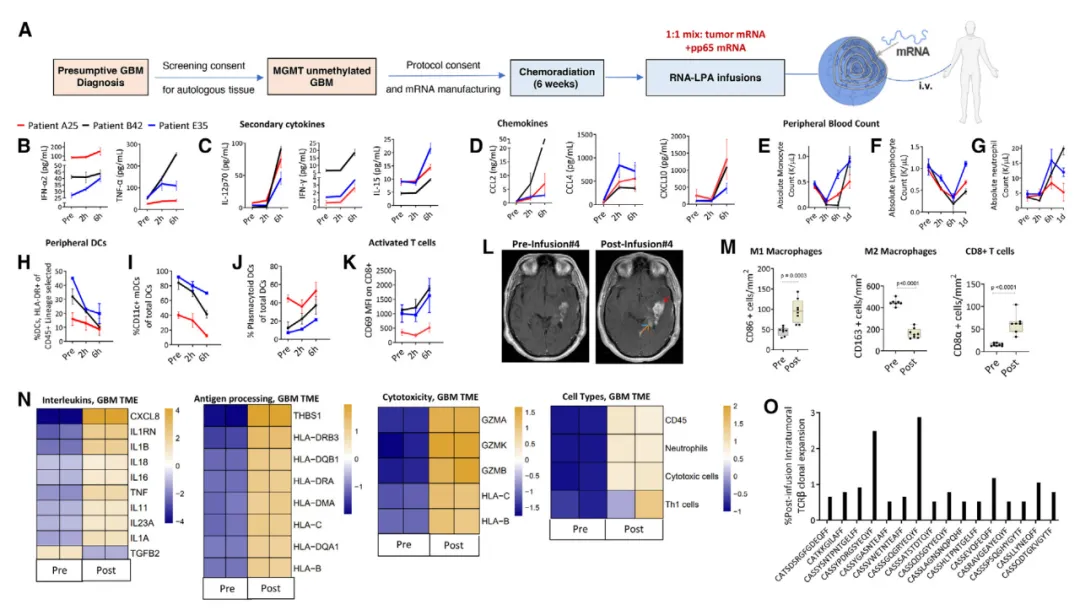
RNA-LPA介导人胶质母细胞瘤患者细胞因子/趋化因子的快速释放、外周血单个核细胞( PBMC )动员和肿瘤微环境(TME)重塑
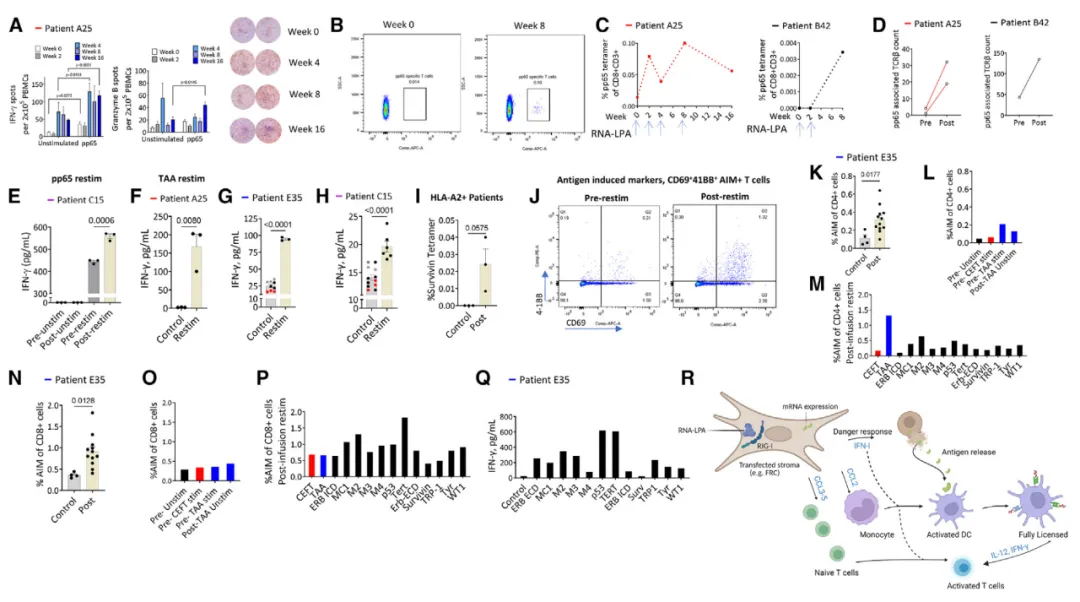
RNA-LPA诱导人胶质母细胞瘤患者抗原特异性T细胞反应
虽然目前还无法评估该 mRNA癌症疫苗 的临床效果,但这些患者的生存期和无病生存期都已超过了预期。
总的来说,该研究强调了RNA-LPA作为一种新兴的免疫疗法在治疗癌症方面的潜力,特别是对于那些难以用传统方法治疗的肿瘤, 恢复免疫原性较差的肿瘤中的免疫反应,打破 免疫耐受性,同时诱导快速且持久免疫反应,还挑战了 mRNA癌症疫苗必须作为纳米颗粒 靶向树突状细胞的范式。
基于上述结果,在美国FDA和CureSearch儿童癌症基金会的支持下,研究团队下一步将进行一项扩大的1期临床试验,纳入多达24名成人和儿童患者,以进一步验证该mRNA癌症疫苗的效果。
研究团队创立了一家名为 iOncologi 的公司,该公司已开发了多种突破性的免疫调节疗法,其中,两款干细胞疗法 (IONC201和IONC202) 在 免疫疗法耐药的 实体瘤 方面显示出显著的 临床前疗效,一款mRNA癌症疫苗 ( IONC101) 正在开展早期临床试验。
https://www.cell.com/cell/abstract/S0092-8674(24)00398-2
版权声明:本文为“乐问号”作者或机构在乐问医学上传并发布,仅代表该作者或机构观点,不代表乐问医学的观点或立场,不能作为个体诊疗依据,如有不适,请结合自身情况寻求医生的针对性治疗。
链接:http://www.lewenyixue.com/2024/05/15/Cell%EF%BC%9A%E6%96%B0%E5%9E%8BmRNA%E7%99%8C%E7%97%87%E7%96%AB%E8%8B%97%EF%BC%8C%E5%8F%AA%E9%9C%80%E4%B8%80%E9%92%88/
THE END