肺癌克星:王洁教授学术的戎马生涯
前言
 图片来源:人物
图片来源:人物 主要内容
一、研究方向一:液体活检-ctDNA
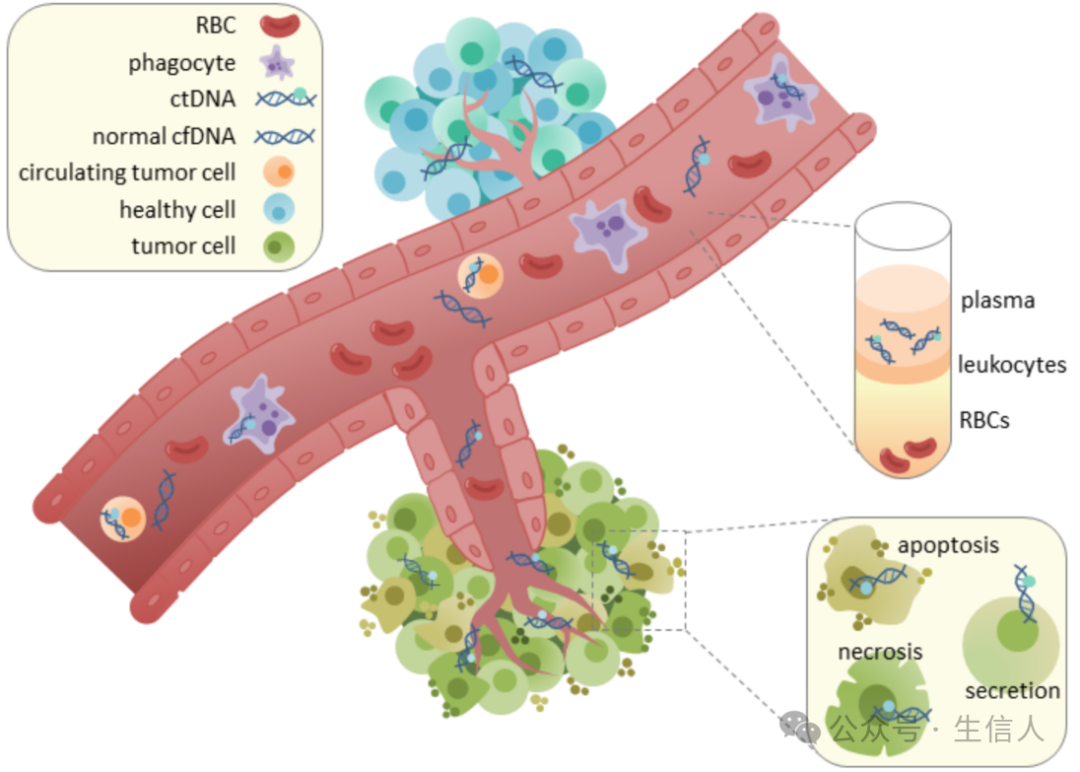






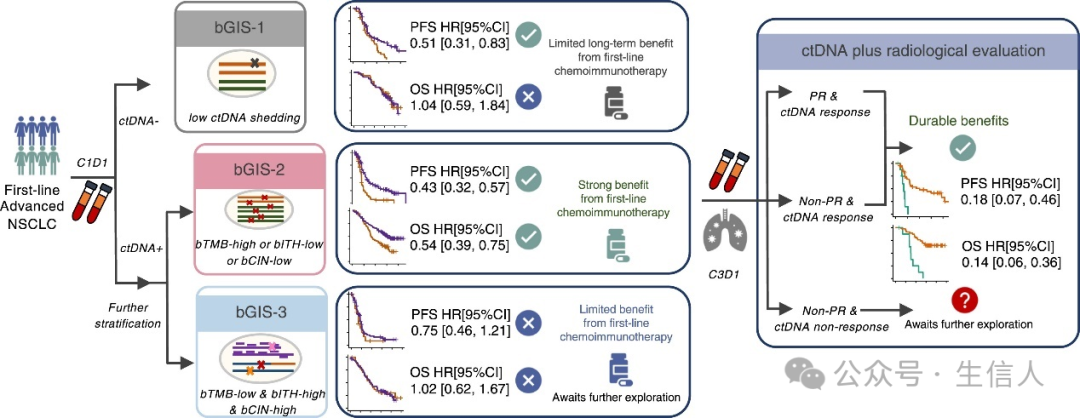
二、研究方向二:肺癌的临床治疗



1.2021年5月,Journal of Thoracic Oncology,Tislelizumab Plus Chemotherapy as First-Line Treatment for Locally Advanced or Metastatic Nonsquamous NSCLC (RATIONALE 304): A Randomized Phase 3 Trial,与单纯化疗相比,在化疗基础上加用替雷利珠单抗(抗PD-1)可显著延长PFS、提高应答率和延长应答持续时间,为晚期非鳞状NSCLC的一线治疗提供了一种新的潜在选择。
2.2022年5月,Lancet Oncology,Adebrelimab or placebo plus carboplatin and etoposide as first-line treatment for extensive-stage small-cell lung cancer (CAPSTONE-1): a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial,在化疗的基础上加用阿得贝利单抗(抗PD-L1)可明显改善ES-SCLC患者的总生存期,且安全性可接受。
3.2022年10月,Journal of Clinical Oncology,Toripalimab Plus Chemotherapy for Patients With Treatment-Naive Advanced Non–Small-Cell Lung Cancer: A Multicenter Randomized Phase III Trial (CHOICE-01),特瑞普利单抗(首个国产抗PD-1单抗)联合化疗能明显改善免疫治疗晚期NSCLC患者的PFS和OS,同时具有可控的安全性。
|
公司、 合作伙伴 |
通用名 ( 商品名 ) |
靶点 |
Isotype |
获批时间 |
适应症 |
|
辉瑞 |
Gemtuzumab ozogamicin (Mylotarg) |
CD33 |
IgG4k |
17 May 2000(USA; withdrawn in 2010); 1 Sep 2017(USA), 19 Apr 2018(EU) |
AML |
|
Seagen, 武田 |
维布妥昔单抗 (Adcetris) |
CD30 |
IgG1k |
19 Aug 2011(USA); 25 Oct 2012(EU) |
HL, ALCL |
|
基因泰克 罗氏 |
恩美曲妥珠单抗 (Kadcyla) |
HER2 |
IgG1k |
22 Feb 2013(USA); 15 Nov 2013(EU) |
HER2+ early or metastatic BC |
|
辉瑞 |
Inotuzumab ozogamicin (Besponsa) |
CD22 |
IgG4x |
17 Aug 2017(USA); 28 Jun 2017(EU) |
ALL |
|
基因泰克 |
Polatuzumab vedotin(Polivy) |
CD79b |
IgG1k |
10 Jun 2019(USA); 16 Jan 2020(EU) |
DLBCL |
|
Astellas Pharma US, Seagen |
Enfortumab vedotin(Padcev) |
Nectin-4 |
IgG1k |
18 Dec 2019(USA); 13 Apr 2022(EU) |
Metastatic urothelial cancer |
|
第一三共 |
Trastuzumab deruxtecan (Enhertu) |
HER2 |
IgG1k |
20 Dec 2019(USA); 18 Jan 2021(EU) |
HER2+, HER2-low BC, NSCLC, GC/GOJ adenocarcinoma |
|
吉列德 |
Sacituzumab govitecan (Trodelvy) |
TROP2 |
IgG1k |
22 Apr 2020(USA); 22 Nov 2021(EU) |
TNBC, metastatic urothelial cancer |
|
GSK |
Belantabab mafodotin (Blenrep) |
BCMA |
IgG1k |
05 Aug 2020(USA); 25 Aug 2020(EU) |
MM |
|
Cetuximab Saratolacan |
Cetuximab Saratolacan |
EGFR |
I g G1 k |
25 S ep 2020(JAN) |
SCCHN |
|
Seagen |
Tisotumab vedotin(Tivdak) |
Tissue factor |
IgG1k |
20 Sep 2021(USA) |
Cervical cancer |
|
ADC Therapeutics |
Loncastuximab tesirine (Zynlonta) |
CD19 |
IgG1k |
23 Apr 2021(USA); 02 Dec 2022(EU) |
DLBCL |
|
RemeGen |
Disitamab vedotin(Aidixi) |
HER2 |
IgG1k |
NA(2021 approval in China) |
GC |
|
ImmunoGen |
Mirvetuximab soravtansine (Elahere) |
FR |
IgG1k |
14 Nov 2022(USA) |
Ovarian cancer |
|
Byondis |
Trastuzumab duocarmazine |
HER2 |
IgG1k |
USA review; EU review(FDA, PDUFA date 12 May 2023) |
HER2+BC |
|
荣昌生物 |
维迪西妥单抗 ( 爱地希 ) |
HER2 |
IgG1k |
6 JUN 2021(CHN) |
HER2+ 胃癌三线 |
已上市的ADC药物
1.2023年ASCO大会:王洁教授展示了一项首次人体试验(first-in-human)、多中心、开放标签的Ⅰ期研究(ARTEMIS-001),该研究在晚期实体瘤患者中使用靶向B7-H3的抗体药物偶联物HS-20093。对于小细胞肺癌(SCLC)患者,HS-20093后线治疗的有效率超过60%,这在以往的研究中极为罕见。
2.2024年WCLC大会/ESMO大会:王洁教授再次成为焦点,她带来了TROP2 ADC药物SHR-A1921的研究结果(NCT05154604)。该研究报告了SHR-A1921对经过治疗的广泛期小细胞肺癌(ES-SCLC)患者的临床实践和安全性。结果显示,SHR-A1921对多线经治的ES-SCLC患者,甚至是TROP-2低表达患者,都表现出良好的临床疗效和可控的安全性。

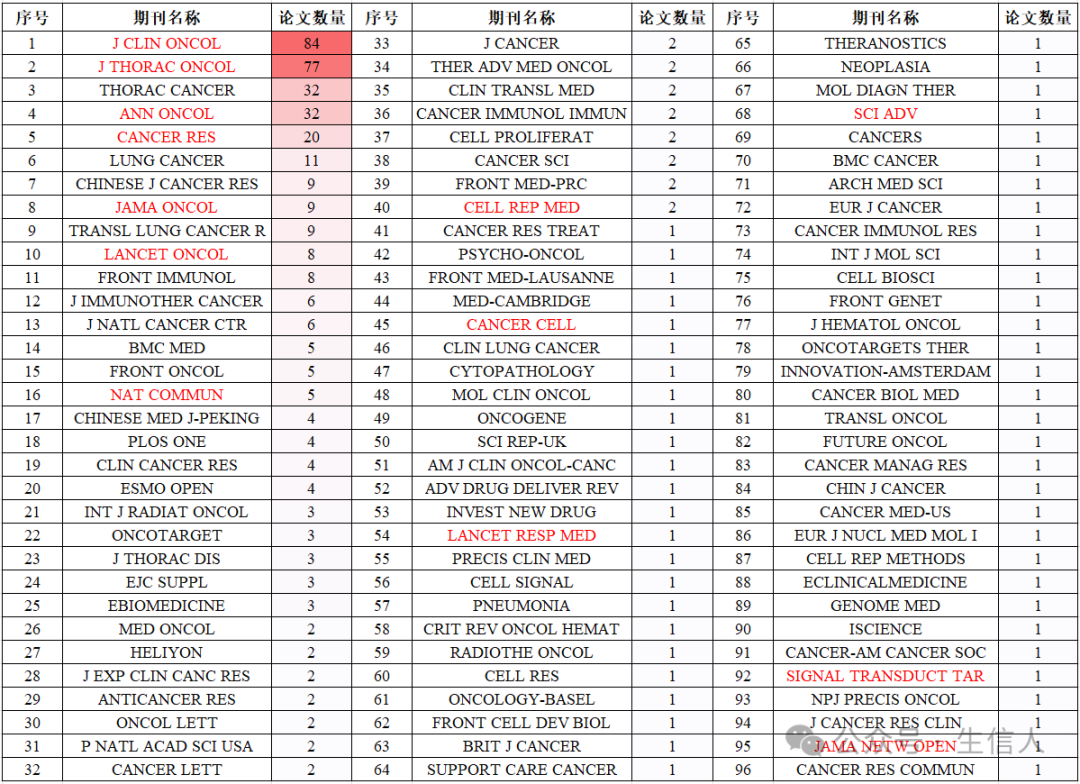
【代表作汇总】
1 . 2009/06 Epidermal growth factor receptor mutations in plasma DNA samples predict tumor response in Chinese patients with stages IIIB to IV non-small-cell lung cancer(J Clin Oncol)
2. 2012/09 Influence of Chemotherapy on EGFR Mutation Status Among Patients With Non–Small-Cell Lung Cancer(J Clin Oncol)
3. 2013/12 Reproducible Copy Number Variation Patterns among Single Circulating Tumor Cells of Lung Cancer Patients(Proc Natl Acad Sci USA)
4. 2018/02 Mechanistic Exploration of Cancer Stem Cell Marker Voltage-Dependent Calcium Channel α2δ1 Subunit-mediated Chemotherapy Resistance in Small-Cell Lung Cancer(Clinical Cancer Research)
5.2018/05 Prediction of Chemotherapeutic Efficacy in Non-Small Cell Lung Cancer by Serum Metabolomic Profiling(Clinical Cancer Research)
6.2018/09 Detection of EGFR mutations in plasma circulating tumour DNA as a selection criterion for first-line gefitinib treatment in patients with advanced lung adenocarcinoma (BENEFIT): a phase 2, single-arm, multicentre clinical trial(Lancet Respir Med)
7.2019/05 Assessment of Blood Tumor Mutational Burden as a Potential Biomarker for Immunotherapy in Patients With Non–Small Cell Lung Cancer With Use of a Next-Generation Sequencing Cancer Gene Panel(JAMA Oncology)
8.2020/01 TCR Repertoire Diversity of Peripheral PD-1(+)CD8(+) T Cells Predicts Clinical Outcomes after Immunotherapy in Patients with Non-Small Cell Lung Cancer(Cancer Immunol Res)
9.2020/03 Use of Immunotherapy With Programmed Cell Death 1 vs Programmed Cell Death Ligand 1 Inhibitors in Patients With Cancer(JAMA Oncology)
10.2020/05 Active and Effective Measures for the Care of Patients With Cancer During the COVID-19 Spread in China(JAMA Oncology)
11.2021/05 Weighting tumor-specific TCR repertoires as a classifier to stratify the immunotherapy delivery in non-small cell lung cancers(Science Advances)
12.2021/05 Tislelizumab Plus Chemotherapy vs Chemotherapy Alone as First-line Treatment for Advanced Squamous Non–Small-Cell Lung Cancer(JAMA Oncology)
13.2021/09 Treatment-related adverse events of PD-1 and PD-L1 inhibitor-based combination therapies in clinical trials: a systematic review and meta-analysis(The Lancet Oncology)
14.2022/05 Adebrelimab or placebo plus carboplatin and etoposide as first-line treatment for extensive-stage small-cell lung cancer (CAPSTONE-1): a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial(The Lancet Oncology)
15.2022/09 Evaluation of Clinical Outcomes of Icotinib in Patients With Clinically Diagnosed Advanced Lung Cancer With EGFR-Sensitizing Variants Assessed by Circulating Tumor DNA Testing(JAMA Oncology)
16.2022/11 Single-cell transcriptomic profiling reveals the tumor heterogeneity of small-cell lung cancer(Signal Transduction And Targeted Therapy)
17.2022/10 Toripalimab Plus Chemotherapy for Patients With Treatment-Naive Advanced Non–Small-Cell Lung Cancer: A Multicenter Randomized Phase III Trial (CHOICE-01)(J Clin Oncol)
18.2023/09 Ablation of ERO1A induces lethal endoplasmic reticulum stress responses and immunogenic cell death to activate anti-tumor immunity(Cell Reports Medicine)
19.2024/02 Assessment of human leukocyte antigen-based neoantigen presentation to determine pan-cancer response to immunotherapy(Nature Communications)
20.2024/09 Circulating tumor DNA-based stratification strategy for chemotherapy plus PD-1 inhibitor in advanced non-small-cell lung cancer(Cancer Cell)
链接:http://www.lewenyixue.com/2025/03/14/%E8%82%BA%E7%99%8C%E5%85%8B%E6%98%9F%EF%BC%9A%E7%8E%8B%E6%B4%81%E6%95%99%E6%8E%88%E5%AD%A6%E6%9C%AF%E7%9A%84%E6%88%8E%E9%A9%AC%E7%94%9F%E6%B6%AF/





赶快来坐沙发