无创智能精准预测乳腺癌残癌负荷
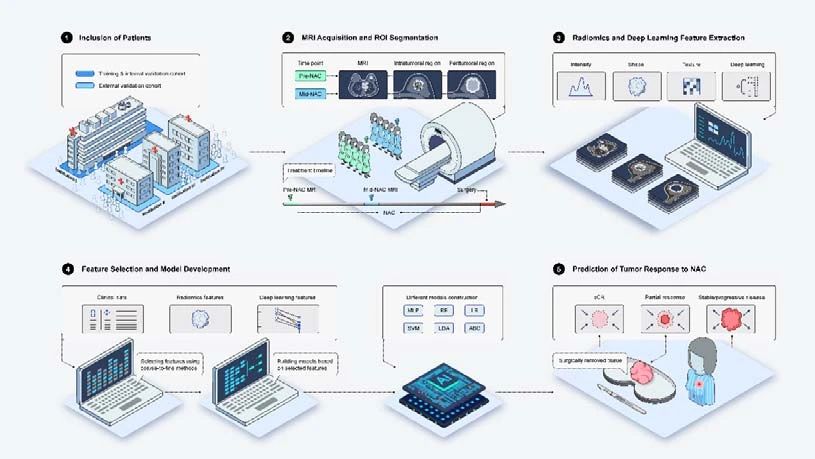
对于乳腺癌术前新辅助化疗患者,根据五项参数(原发灶残癌范围、残癌细胞密度、原位癌所占比例、阳性淋巴结数量、淋巴结转移癌最大径)可以计算残癌负荷指数及其对应分级,治疗早期准确预测残癌负荷分级有助于制定合适的手术方案及随访策略。然而,目前仍然缺乏能在术前精准预测残癌负荷的无创工具。 2024年4月1日,创刊于1885年的美国外科学会和欧洲外科学会官方期刊《外科年鉴》在线发表广东省人民医院王坤教授牵头、佛山市第一人民医院、中山大学附属第一医院、汕头市中心医院共同参与的原创研究,利用人工智能深度学习方法,建立多时序磁共振成像影像组学模型,可在新辅助化疗早期精准预测乳腺癌的残癌负荷分级,在不同分子亚型乳腺癌中均取得良好的预测性能,将有助于对乳腺癌患者进行个体化手术及护理分层管理。该研究共同通信作者为广东省人民医院王坤教授、佛山市第一人民医院叶国麟教授、中山大学附属第一医院林颖教授,共同第一作者为李巍博士、黄育鸿博士后、朱腾博士。该研究对2015年7月~2021年12月广东省人民医院、佛山市第一人民医院、中山大学附属第一医院、汕头市中心医院连续1048例完成新辅助化疗并进行手术的患者进行回顾分析,收集新辅助化疗之前和新辅助化疗期间的多模态磁共振成像影像数据,根据残癌负荷0~I、II、III将佛山市第一人民医院335例患者分为三组。从乳腺癌的多模态磁共振成像影像分别提取影像组学特征和深度为50层的卷积神经网络ResNet-50迁移学习特征,采用曼-惠特尼U检验、斯皮尔曼等级相关分析、最小绝对值收敛和选择算子回归以及Boruta算法进行特征选择,并采用逻辑回归、随机森林和支持向量机等多种机器学习算法,根据HER2阳性、激素受体阳性HER2阴性、三阴性三类特定分子亚型分别构建人工智能模型,以预测乳腺癌在完成新辅助化疗后的残癌负荷分级,并对三个外部验证队列共计713例患者进行充分验证。该模型有望为乳腺癌患者及时调整治疗方案和确定手术时机,被预测为残癌负荷III级的患者可能对终止化疗和立即手术获益,有可能提高乳腺癌患者的总生存率。
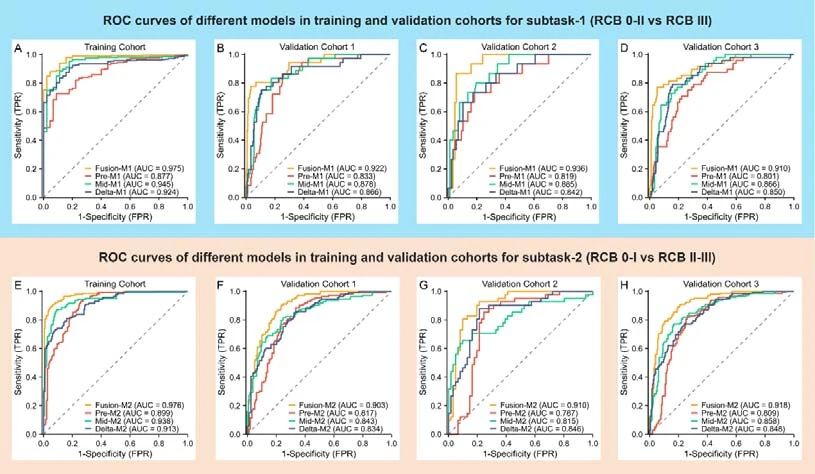
该影像人工智能系统包括模型I及模型II,对于区分残癌负荷0~II级和残癌负荷III级,模型I融合三种基模型输出以及HER2状态,主要队列的真假阳性率曲线下面积达0.975,验证队列达0.923,验证队列的准确率分别达94.10%、93.14%、92.35%。亚组分析显示,模型I对HER2阳性、激素受体阳性HER2阴性和三阴性三种亚型的敏感性分别为82.61%、74.19%、81.25%。对于cT1~2、cT3和cT4分期,模型I的敏感性分别为77.36%、81.82%、76.92%。模型II对预测残癌负荷0~I与残癌负荷II~III表现出色,融合三种基模型输出以及cT分期、雌激素受体和HER2状态,主要队列的曲线下面积达0.976、准确率达92.54%。三个外部验证队列的曲线下面积分别达0.903、0.910、0.918,准确率分别为82.29%、84.31%、84.12%。亚组分析证实,模型II对不同临床背景的表现一致,敏感性无显著变化。HER2阳性、激素受体阳性HER2阴性和三阴性三种亚型的平均敏感性分别为87.69%、91.11%、89.83%。对cT1~2、cT3和cT4期的患者敏感性分别为88.18%、88.89%、93.75%。
该研究还发现,与新辅助化疗之前或新辅助化疗期间磁共振成像构建的单时序模型相比,联合新辅助化疗之前及期间多时序磁共振成像以及临床因素的人工智能模型,对外部验证集的曲线下面积和准确率都获得显著提升。模型I对验证队列的曲线下面积范围达0.910~0.936,而模型II对验证队列的曲线下面积范围达也达0.903~0.918。因此,该研究结果表明,影像人工智能系统可为早期预测乳腺癌残癌负荷分级提供无创影像工具,有望辅助临床医生进行个体化新辅助化疗方案调整,把握手术时机和制定合适的随访策略。
链接:http://www.lewenyixue.com/2024/04/08/%e6%97%a0%e5%88%9b%e6%99%ba%e8%83%bd%e7%b2%be%e5%87%86%e9%a2%84%e6%b5%8b%e4%b9%b3%e8%85%ba%e7%99%8c%e6%ae%8b%e7%99%8c%e8%b4%9f%e8%8d%b7/





赶快来坐沙发