中国医学科学院王洁团队:ATAD2靶点为小细胞肺癌免疫治疗注入新活力
【导读】小细胞肺癌(SCLC)是一种侵袭性极强的神经内分泌肿瘤,预后极差。目前,能够促进小细胞肺癌免疫疗法的特异性肿瘤抗原仍未找到。
2025年1月13日,中国医学科学院肿瘤医院肿瘤内科王洁教授团队在期刊《eBioMedicine》上发表了题为“ATAD2 is a potential immunotherapy target for patients with small cell lung cancer harboring HLA-A∗0201”的研究论文。 研究结果凸显了以ATAD2 YSDDDVPSV免疫肽为靶点进行SCLC免疫治疗的潜力,从而为开发采用T细胞疗法有效治疗携带HLA-A∗02:01的ASCL1阳性或NEUROD1阳性SCLC提供了一条前景广阔的途径。

https://www.thelancet.com/journals/ebiom/article/PIIS2352-3964(24)00551-6/fulltext
关于哮喘
01
ATAD2是一种属于AAA+ATPase和溴域蛋白家族的CTA,是一种新发现的致癌基因,在多种恶性肿瘤中表现出致癌功能。多项研究报道了ATAD2在多种信号通路中的致癌功能,包括p53介导和p38-MAPK介导的细胞凋亡通路、AKT通路、RB/E2F-cMYC通路、上皮细胞向间质转化(EMT)通路和类固醇激素信号通路。此外,ATAD2还与染色质动力学、DNA复制和基因转录过程有关,发挥着表观遗传阅读器和转录因子或共激活因子的作用,促进肿瘤发生。
这项研究的主要目的是鉴定和描述SCLC中的CTA类型,重点是阐明ATAD2在5种不同SCLC亚型中的表达模式和生物学功能。此外,团队还希望将ATAD2及其衍生的免疫肽作为SCLC免疫疗法的潜在靶点进行研究。
ATAD2的表达与ASCL1的表达呈正相关
02
ATAD2的表达水平在5个亚型(SCLC-A/N/Y/P和混合型)中存在差异。具体而言,与其他SCLC亚型(SCLC-P的5.76%、SCLC-Y的9.61%和SCLC-MIX的7.69%)相比,SCLC-A(82.69%)和 SCLC-N(65.38%)样本的ATAD2阳性率更高。此外, ATAD2的高表达与SCLC-A相关,与SCLC-MIX负相关, 而ATAD2的表达水平与SCLC-N、SCLC-P或SCLC-Y没有相关性。团队也没有发现ATAD2的表达与任何临床特征(年龄、性别、吸烟史和VALSG分期)相关。
ATAD2和NOL4在未经治疗的CDX和一名顺铂耐药患者的CTC中表达量最高,而在未经治疗的CTC和对顺铂有反应的肿瘤患者的CTC中,这些基因的表达量较低。在未经治疗的CDX肿瘤中,ATAD2、NOL4和SPAG1的表达水平高于未经治疗的CTC,但在顺铂治疗应答患者的CTC中,ATAD2、NOL4和SPAG1的表达水平低于顺铂耐药患者的CTC。这些数据表明, ATAD2的表达是动态的,会随着SCLC临床病程的变化而变化。
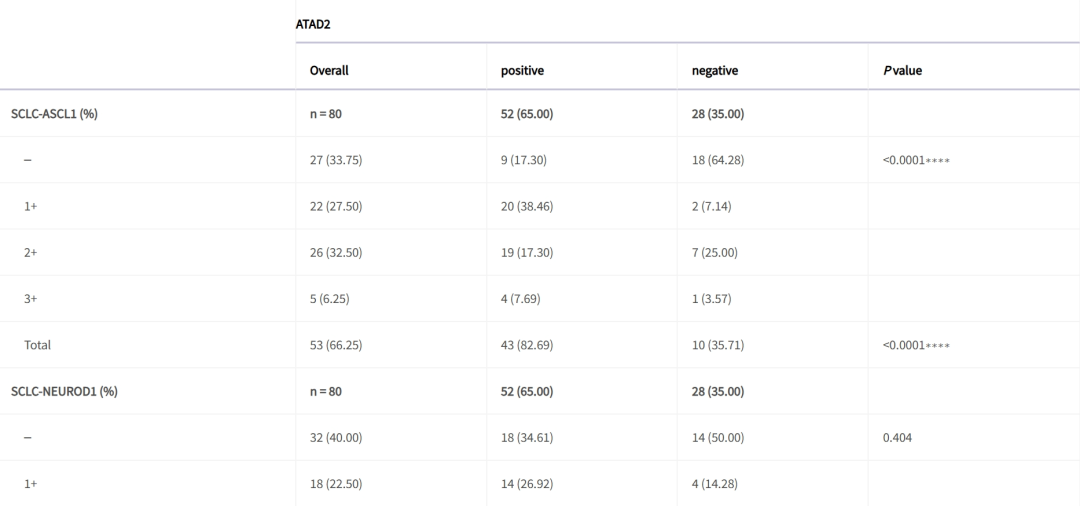
ATAD2表达与ANPY亚型标志物表达之间的相关性。
总结
03
1. 研究发现,肿瘤相关抗原(TAAs)中的癌睾抗原(CTAs)在肿瘤细胞、睾丸和胎盘组织中高表达,而在其他正常组织中几乎不表达,是很有希望的疾病特异性抗原靶点。
2. 通过LC - MS/MS分析发现,CTAs在SCLC亚型中表达模式存在显著差异,强调了确定SCLC亚型共同肿瘤抗原的必要性。
3. ATAD2是SCLC中发现的常见CTA之一,其表达水平明显高于正常相邻组织或NSCLC组织,且在SCLC亚型中表达模式差异显著,可能是SCLC-A和SCLC-N亚型的潜在肿瘤抗原靶点。
4. SCLC-A/N亚型中CTAs和免疫肽数量明显低于SCLC-P/Y亚型,可能与更严重的免疫逃逸有关,导致对免疫靶向药物反应不佳。
5. 研究发现的100种ATAD2免疫肽中,YSDDDVPSV具有最有利的免疫靶向特征,且HLA-A∗02:01 T细胞对其反应性强,表明HLA-A∗02:01-YSDDDVPSV抗原肽是未来开发免疫疗法的潜在靶点。
6. 研究团队正在用ATAD2衍生的YSDDDVPSV免疫肽改造TCR构建TCR-T细胞,测试其杀伤SCLC肿瘤细胞的能力,若成功将使大多数携带HLA-A∗02:01的SCLC-A患者及表达ASCL1的复杂SCLC亚型患者受益。
参考资料:
1.Rudin, C.M. ∙ Brambilla, E. ∙ Faivre-Finn, C. ∙ et al.
Small-cell lung cancer
Nat Rev Dis Primers. 2021; 7:3
2.Farago, A.F. ∙ Keane, F.K.
Current standards for clinical management of small cell lung cancer
Transl Lung Cancer Res. 2018; 7:69-79
链接:http://www.lewenyixue.com/2025/01/15/%E4%B8%AD%E5%9B%BD%E5%8C%BB%E5%AD%A6%E7%A7%91%E5%AD%A6%E9%99%A2%E7%8E%8B%E6%B4%81%E5%9B%A2%E9%98%9F%EF%BC%9AATAD2%E9%9D%B6%E7%82%B9%E4%B8%BA/





赶快来坐沙发