Immunity | 罕见遗传病解释癌症免疫治疗与感染增加之间的联系
一项由加文医学研究所、洛克菲勒大学和京都大学医学研究生院共同领导的跨国合作,揭示了为什么有些接受检查点抑制剂免疫治疗的癌症患者对常见感染的易感性增加的潜在解释。这些发现为免疫反应提供了新的见解,并揭示了预防常见癌症治 疗副作用的潜在方法。
“免疫检查点抑制剂疗法使 T 细胞更有效地攻击肿瘤和癌细胞,从而彻底改变了癌症治疗。” Garvan 免疫学和免疫缺陷实验室负责人 Stuart Tangye 博士说,“但这并非没有副作用——其中之一是,大约 20% 接受检查点抑制剂治疗的癌症患者感染率增加,这一现象以前鲜为人知。”
Tangye 是该团队在《 Immunity 》杂志上发表的论文的资深作者之一,该论文题为“ Impaired development of memory Bcells and antibody responses in humans and mice deficient in PD-1 signaling ”。

在他们的研究中,研究人员专注于分子 PD-1 ,它可以作为免疫系统的“手刹”,防止 T 细胞过度激活。检查点抑制剂疗法通过释放这种分子手刹来增强免疫系统对抗癌症的能力。研究人员表示:“广泛用于癌症免疫治疗的针对 PD-1 和 PD-L1 的中和抗体( nAb )释放 T 细胞介导的对自身和肿瘤衍生抗原( Ag )的免疫力。”
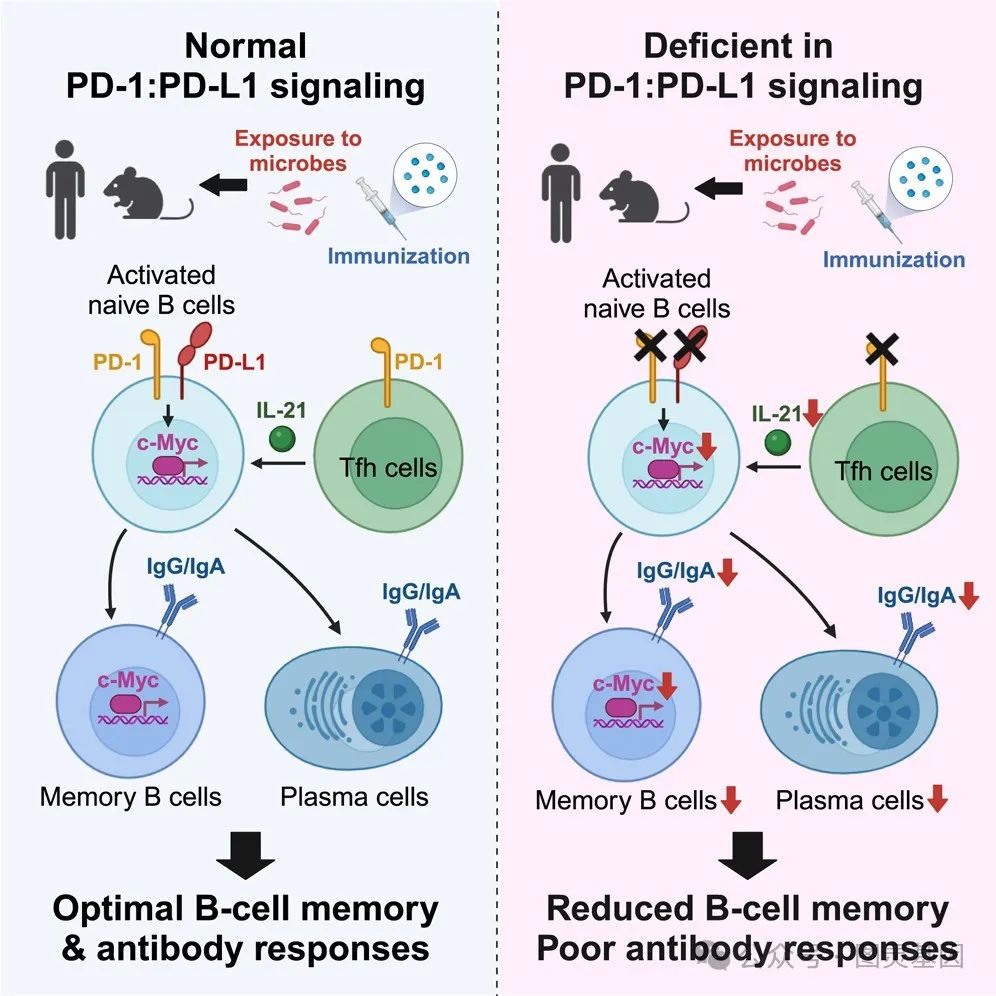
然而,正如该团队也指出的那样,“证据表明, PD-1/PD-L1 介导的人类癌症免疫治疗的不良后果是,无论是否使用其他免疫抑制剂进行治疗,细菌感染的频率都会增加。”
研究人员检查了罕见的 PD-1 或其结合伴侣 PD-L1 遗传缺陷患者的免疫细胞,以及缺乏 PD-1 信号的动物模型。他们发现, PD-1 活性受损或缺失会显著降低记忆 B 细胞产生的抗体的多样性和质量。记忆 B 细胞是一种“记住”过去感染的长寿免疫细胞。
Tangye 说:“我们的研究结果表明,检查点抑制剂在提高抗癌免疫力的同时,也会阻碍 B 细胞, B 细胞是免疫系统中产生抗体以防止常见感染的细胞。这一理解是理解和减少这种癌症治疗对免疫的副作用的关键第一步。”
“我们发现,天生缺乏 PD-1 或 PD-L1 的人,其抗体的多样性降低,记忆 B 细胞减少,这使得更难产生针对病毒和细菌等常见病原体的高质量抗体。”第一作者、斯坦福大学博士后 Masato Ogishi 博士补充道。
Tangye 教授进一步评论道:“记忆 B 细胞的产生和质量受到抑制,这可以解释接受检查点抑制剂治疗的癌症患者感染率上升的原因。”
作者指出,重要的是, PD-1 和 PDL1 缺陷患者尚未表现出抗体缺乏症患者通常出现的严重细菌感染,“这表明观察到的体液免疫缺陷可能不足以在儿童期引起临床上明显的表型。”他们还指出,大多数接受 PD-1 或 PDL1 阻断免疫治疗的癌症患者,由于恶性肿瘤类型、合并症和年龄较大,已经出现免疫功能低下。他们写道:“因此, PD-1 或 PD-L1 阻断引起的体液免疫的细微干扰可能会引发毁灭性的细菌感染。”
共同作者、京都大学教授 Kenji Chamoto 博士指出:“ PD-1 抑制具有‘阴阳’性质:它激活抗肿瘤免疫,但同时阻碍 B 细胞免疫。这种二元性似乎源于免疫稳态的保守机制。”
研究人员表示,这些发现强调了临床医生需要监测接受检查点抑制剂的患者的 B 细胞功能,并为感染风险较高的患者提供预防性干预措施。“尽管 PD-1 抑制剂极大地改善了癌症治疗,但我们的研究结果表明,临床医生需要意识到增强的抗肿瘤免疫和受损的抗体介导的免疫之间的潜在权衡。”洛克菲勒大学的研究人员 StéphanieBoisson-Dupuis 博士说,“一种潜在的预防性解决方案是免疫球蛋白替代疗法( IgRT ),这是一种现有的治疗方法,用于替代免疫缺陷患者体内缺失的抗体,可以被视为感染风险较高的癌症患者的一种预防措施。”
研究 PD-1 或 PD-L1 缺乏等罕见遗传疾病的病例,使团队能够深入了解人类免疫系统的正常工作方式,以及我们对免疫系统的操作如何影响免疫系统。“多亏了这些患者,我们找到了一种微调癌症免疫疗法的途径,可以在最大限度减少伤害的同时使益处最大化。”
研究人员在论文中表示,他们的研究结果“应该促使进一步调查细菌和其他感染的频率和严重程度,以及预防性疫苗接种(例如肺炎链球菌和流感嗜血杆菌)和接受 PD-1 或 PD-L1 阻断免疫治疗的癌症患者低剂量静脉注射 Ig 的潜在临床益处。”
展望未来,研究人员将探索改进检查点抑制剂治疗的方法,以保持其强大的抗癌效果,同时保持免疫系统抵抗感染的能力。 Tangye 说:“这项研究突出了癌症、基因组学和免疫学研究相互促进的潜力,使研究结果能够惠及更广泛的人群。”
链接:http://www.lewenyixue.com/2024/12/25/Immunity%20%7C%20%E7%BD%95%E8%A7%81%E9%81%97%E4%BC%A0%E7%97%85%E8%A7%A3%E9%87%8A%E7%99%8C%E7%97%87/