24年肿瘤血管生成还有得做吗?Nature教你用单细胞在泛癌水平发高分文章
肿瘤通过血液供应获得进展和转移所需的营养和氧气。因此,了解肿瘤血管的复杂性,对抗血管生成治疗具有重要的临床意义。今天,小编要和大家分享一篇 2024年7月发表在Nature(IF:50.5) 上的文章,分析了来自372个病人,代表31种癌症类型的肿瘤血管系统的单细胞转录图谱,揭开了肿瘤血管系统的复杂性。

一、背景介绍
肿瘤血管生成是癌症的一个重要标志。它的诱导作用是帮助肿瘤获得维持生长所需的营养和氧气。血管生成可以发生在肿瘤进展的任何阶段,并通过现有血管网络形成新血管来表现。与正常血管相比,肿瘤血管系统表现出渗透性增加、形态不规则和组织不良。内皮细胞(EC)和壁细胞(MC)是直接参与肿瘤血管生成的主要血管成分。EC亚群是相当异质的,包括不同的血管类型和器官特异性特征。EC的可塑性使其成为抗血管生成治疗(AAT)的靶点,致力于通过阻断血管生成信号传导实现肿瘤血管正常化。在临床前研究中,AAT与肿瘤免疫疗法相结合已被证明可产生更有效的抗肿瘤作用。利用单细胞分析技术,研究人员生成了覆盖约20万个血管细胞的泛肿瘤血管景观,并解开了肿瘤血管系统的复杂性。
二、主要结果
1.肿瘤血管的单细胞图谱
为了剖析肿瘤血管微环境(TVM),研究人员整合了来自内部372名供体的437份肿瘤样本和相邻非肿瘤(ANT)样本,和公共数据集中的EC和MC的数据,共有183,977个TVM细胞接受了严格的质量控制,其中24.2%是本研究中新测序的。随后,基于代表性基因特征对细胞类型进行了注释。在肿瘤组织中,EC主要分为淋巴EC(LEC)和血管EC(VEC);MC主要分为周细胞(PC)和平滑肌细胞(SMC)。
接下来,对VEC、LEC和MC进行无监督图聚类分析,分为29个VEC(V0-V28)、8个LEC(L0-L7)和16个MC(M0-M15)亚群。进一步通过计算观察到的细胞数相对于预期细胞数的相对分数(R o/e 分数;)估计了这些亚群的癌症类型富集,发现大多数亚群表现出泛肿瘤起源。然而,位于UMAP中表示外围的某些VEC和LEC亚群显示出明显的组织来源特异性,因此这些亚群不包括在随后的泛肿瘤分析中。
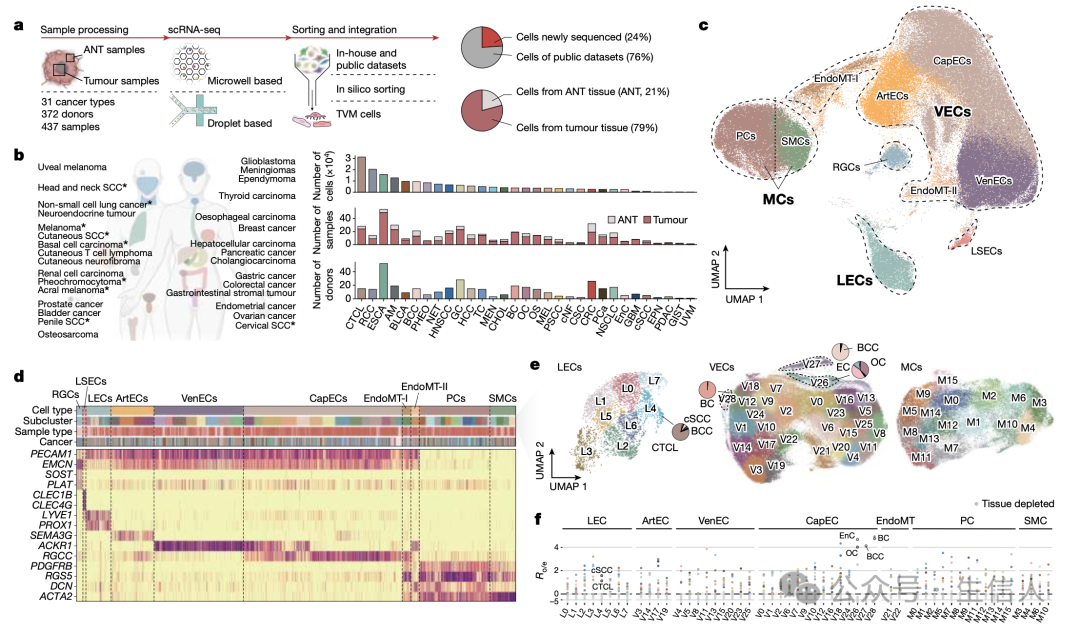
图1. 肿瘤血管系统的细胞类群
2.肿瘤血管生成起源于VenEC
肿瘤血管生成涉及从已有的血管床发展形成新血管。为了研究其分子基础,研究人员基于116,958个泛肿瘤VEC(包括18,048个ArtEC、61,400个CapEC和37,510个VenEC)的转录组学谱概括了肿瘤血管生成。进一步利用扩散成分分析,研究人员推断出从VenEC到ArtEC通过CapEC的分化轨迹,并且将血管生成阶段定义为SI、SII和SIII。作为血管生成起始,APLN被鉴定为TipSI 细胞(下文称为APLN+ TipSI 细胞)的特异性标志物。
为了研究VEC的临床意义,研究人员首先在TCGA中使用去卷积分析评估细胞浸润。在大多数ANT组织中几乎检测不到APLN + TipSI细胞,但在TCGA肿瘤样品中随着肿瘤分期的升高而增加。接下来,研究人员检查了VEC亚型对AAT的反应,发现在用贝伐珠单抗组合疗法治疗后,APLN+ TipSI 细胞显著减少,表明尽管具有高APLN+ TipSI细胞肿瘤浸润的患者预后较差,但更可能受益于AAT。
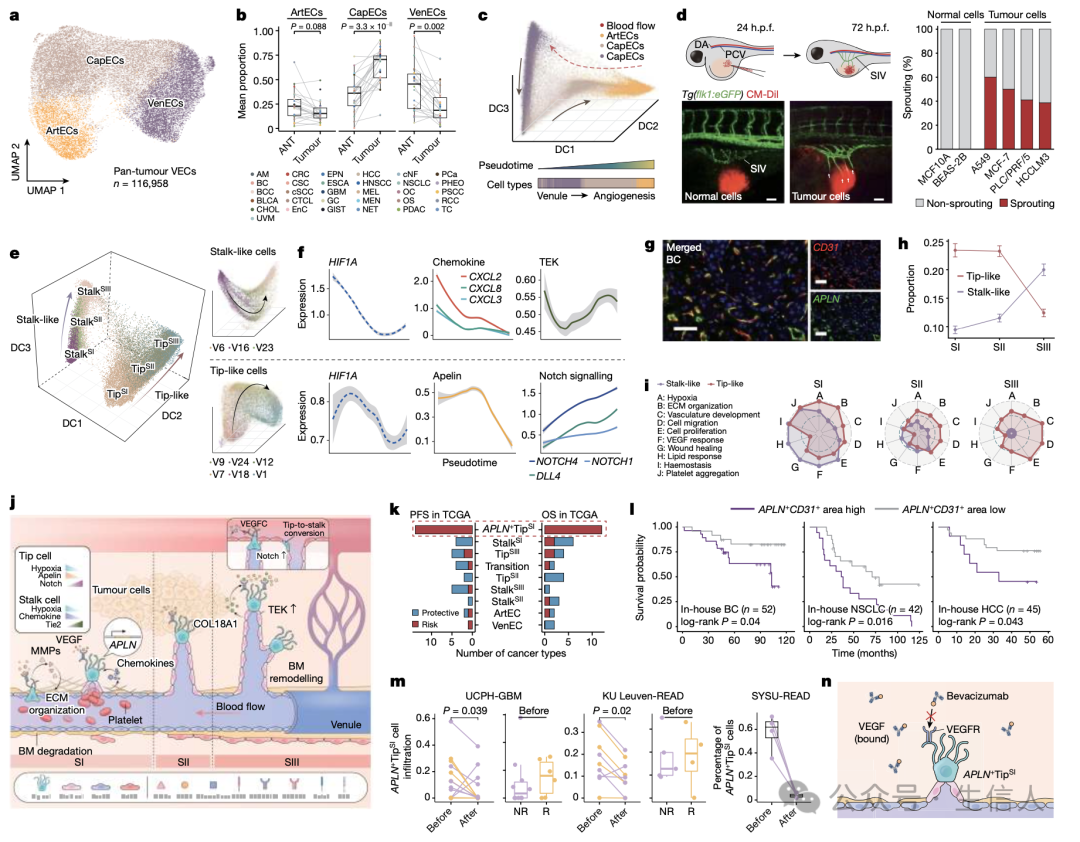
图2. 协调的TME细胞程序与反应性表现出不同的相关性
3.肿瘤LEC的分化谱系
除了VEC,作者接下来描述了LEC的相关特征。总共检测到9,283个泛肿瘤LEC(L0-L3和L5-L7),其中L0和L7亚群主要来自ANT样品,被注释为正常样LEC(NLEC)。通过轨迹推断显示了源自NLEC的两种不同的分化谱系。基因表达分析进一步揭示了每种亚群的特征,发现缺氧可能是肿瘤淋巴管生成的诱导剂。随后鉴定了谱系相关的转录因子,发现炎症反应在LEC分化中具有关键作用。
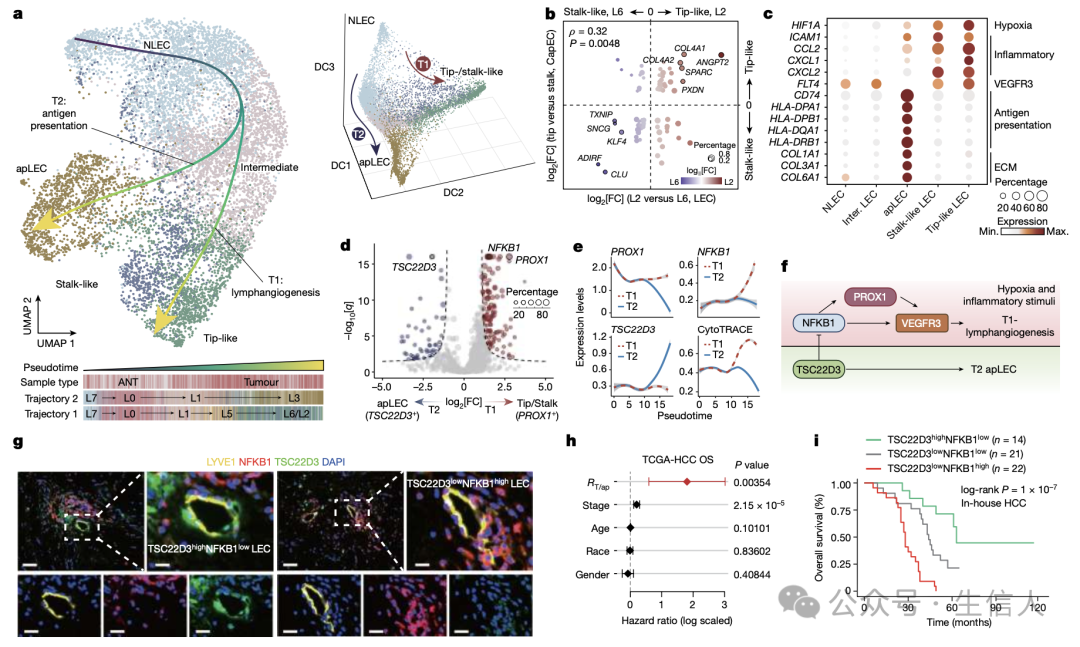
图3. 不同的LEC分化谱系
4.内质网应激驱动促血管生成matPC
分析完EC,接下来,作者开始分析MC。在TVM中检测到40,391个MC,包括29,572个PC和10,819个SMC,其中进一步在泛肿瘤组织中鉴定了四种PC亚型:(1)血管舒张相关PC(vdPC);(2)脂肪细胞样PC;(3)肌样PC;和(4)产生基质的PC(matPC)。进一步根据静态PC的特征对PC的静态状态进行评分,发现vdPC亚型的特征是比其他PC亚型具有更高的静止评分。并且对静止高(Q high)和静止低(Q low)细胞之间的差异表达基因(DEG)分析发现二者代谢状态不同,这其中Qhigh细胞高表达氧化磷酸化相关基因,Qlow细胞高表达ECM和糖酵解调节因子,说明代谢重编程与PC活性密切相关。
值得注意的是,matPC显示静止和代谢状态转变,因此评估了matPC的TF活性,发现内质网(ER)-应激相关的TF ATF 3和XBP1在转录和TF活性水平均显示与假时间的明确关联,表明ER应激可能是matPC进化的关键因素。
随后开始分析MC和EC之间的细胞间相互作用。在内部和外部空间转录组学数据中,进行空间转录组学去卷积分析,并结合染色质免疫沉淀测序(ChIP-seq)数据,进一步支持了ER应激在肿瘤血管生成中的关键作用。
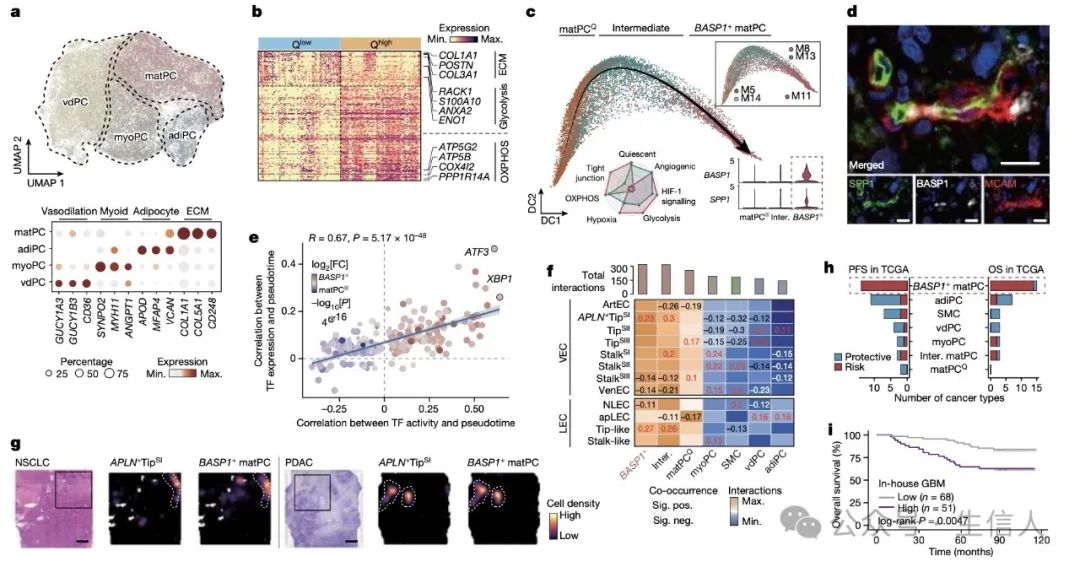
图4. 泛肿瘤MC的表征
5.血管系统和TME之间的串扰
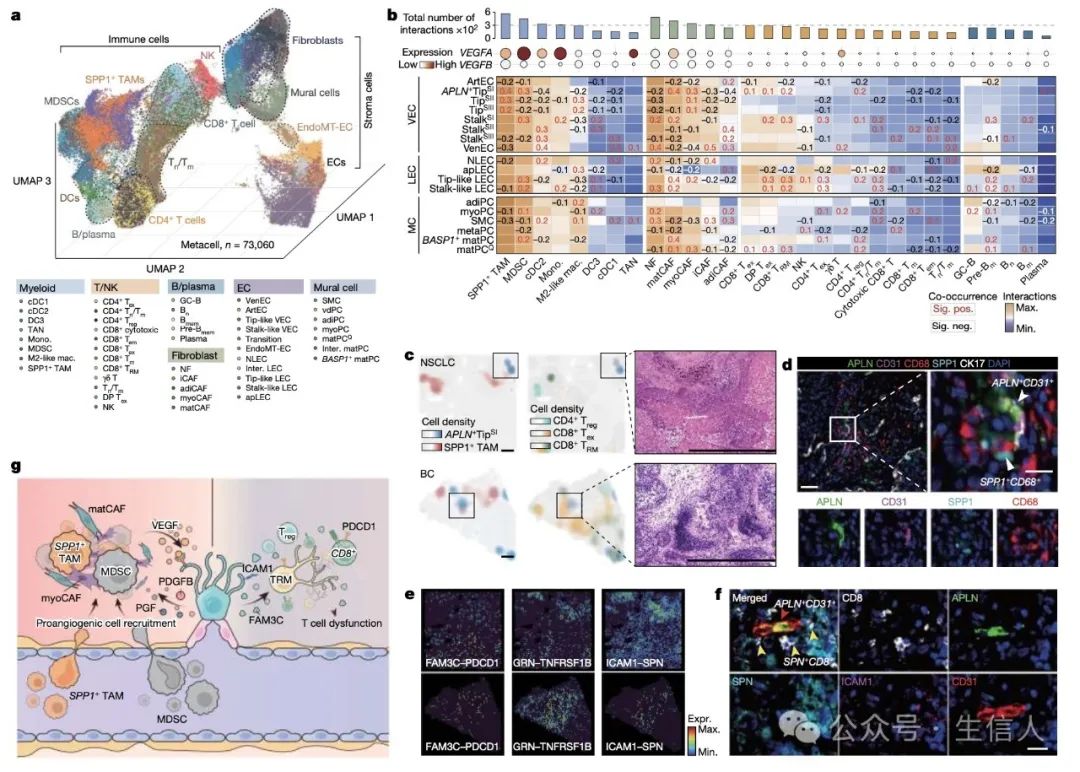
接下来,作者开始分析血管系统和TME之间的细胞通讯。分选了160,366个骨髓细胞、261,751个T细胞和自然杀伤细胞(NK细胞)、42,342个B细胞和92,297个成纤维细胞,并确定了它们的亚型。进一步在血管细胞和TME细胞之间进行了无偏LR相互作用分析,发现骨髓细胞和成纤维细胞显示出比T/NK和B细胞更多的相互作用,包括关键的VEGF信号传导。
此外,mIHC染色揭示了促血管生成细胞在物理上也彼此靠近,形成肿瘤支持性小生境。值得注意的是,APLN+ TipSI 细胞显示出对多种T细胞的免疫调节潜力。总的来说,APLN+ TipSI 细胞有助于形成促血管生成的免疫抑制性TME。
三、小结
到这里文章的主要内容就介绍完了。总的来说,肿瘤血管生成是肿瘤的一个重要过程,但推动这一动态过程的EC的起源仍然是一个重要的未解决的问题。在这篇文章里,研究人员使用计算机模拟和体内模型证明VenEC是血管生成起始的起点,并且全面分析了肿瘤血管生成的两类关键细胞(EC和MC)的的分化轨迹及其特征,为具有临床意义的潜在靶点和AAT提供了新的见解。
参考文献
Pan, X., Li, X., Dong, L. et al. Tumour vasculature at single-cell resolution. Nature (2024).
链接:http://www.lewenyixue.com/2024/12/20/24%E5%B9%B4%E8%82%BF%E7%98%A4%E8%A1%80%E7%AE%A1%E7%94%9F%E6%88%90%E8%BF%98%E6%9C%89%E5%BE%97%E5%81%9A%E5%90%97%EF%BC%9FNatur/