安罗替尼治疗晚期肉瘤的有效性和安全性分析

闫强, 姚伟涛, 杜鑫辉, 等. 安罗替尼治疗晚期肉瘤的有效性和安全性分析[J]. 中华肿瘤杂志, 2023, 45(10):904-910. DOI:10.3760/cma.j.cn112152-20210820-00632.
目的
探讨安罗替尼治疗晚期肉瘤的有效性和安全性,分析不良反应与疗效间的关系。
方法
回顾性分析2018年6月至2021年8月在郑州大学附属肿瘤医院接受安罗替尼治疗的45例晚期肉瘤患者的临床资料。根据实体肿瘤疗效评价标准1.1版计算客观缓解率(ORR)和疾病控制率(DCR),分析无进展生存时间(PFS)与治疗相关不良反应间的关系,生存分析采用Kaplan-Meier法,生存率的比较采用Log rank检验。
结果
45例患者中,40例患者用药时间超过1.5个月,3个月ORR为7.5%(3/40),DCR为80.0%(32/40)。全组患者的整体ORR为2.5%(1/40),DCR为27.5%(11/40),中位PFS为6.70个月。腺泡状软组织肉瘤患者中位PFS为10.27个月,长于其他亚型的肉瘤患者( P=0.048),腺泡状软组织肉瘤、滑膜肉瘤患者的DCR[分别为100.0%(5/5)和100.0%(9/9)]明显优于骨肉瘤患者[(25.0%(1/4),均 P<0.05]。常见的不良反应有促甲状腺素升高(17.8%,8/45)、贫血(15.6%,7/45)、乏力(11.1%,5/45)等,5例患者治疗后出现了3级不良反应。治疗后出现手足综合征患者的PFS(14.10个月)长于未出现手足综合征的患者(6.00个月, P=0.024)。
结论
安罗替尼治疗腺泡状软组织肉瘤、滑膜肉瘤的疗效优于其他亚型,治疗后出现手足综合征患者的PFS明显长于未出现手足综合征的患者。
【关键词】骨肉瘤;软组织肉瘤;安罗替尼;有效性;安全性
肉瘤是一种源于间充质组织的恶性肿瘤,目前报道有70多种组织学亚型,包括骨肉瘤和软组织肉瘤。晚期肉瘤的治疗方法少且预后较差,全身化疗是最常用的治疗方法,然而化疗的中位总生存时间约为12个月,5年生存率<10%。此外化疗有效率仅为14%~48%,且长期应用阿霉素等细胞毒性药物会增加心肌病的发生风险。因此,需要探索能够提高生存率和安全性的治疗方法。
病理性血管生成在肉瘤的生长、进展中起重要作用,因此抗血管生成治疗对控制肉瘤的进展极为重要。安罗替尼是一种新型的多靶点酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TKI),具有抗肿瘤增殖及抗血管生成的作用。安罗替尼治疗晚期软组织肉瘤的Ⅱ期临床试验显示,12周无进展生存率为68%,客观缓解率(objective response rate, ORR)为13%,中位无进展生存时间(progression-free survival, PFS)为5.6个月,中位总生存时间为12个月。与安慰剂比较,安罗替尼可延长PFS,对ORR、疾病控制率(disease control rate, DCR)同样有所改善。Tian等报道,骨肉瘤患者在安罗替尼治疗后的ORR为0,DCR为23%,中位PFS为2.7个月;软组织肉瘤患者治疗后的ORR为14%,DCR为55%,中位PFS为6个月。
然而肉瘤亚型众多且具有高度异质性,导致无法精确判定安罗替尼治疗不同亚型肉瘤的敏感度差异,且安罗替尼治疗晚期肉瘤的疗效和不良反应之间的关系尚不明确,需进一步探索两者之间的联系。本研究旨在评价安罗替尼治疗晚期转移性肉瘤的有效性和安全性,并探讨不良反应与疗效之间的关系。


1 .临床资料:
本研究是一项单中心回顾性研究。选取自2018年6月至2021年8月在郑州大学附属肿瘤医院接受了安罗替尼治疗的既往治疗失败的晚期肉瘤患者(45例)。纳入标准:(1)根据世界卫生组织肿瘤分类,组织学确诊为骨肉瘤或软组织肉瘤,并根据美国癌症联合委员会癌症分期手册(第8版),参照骨与软组织肉瘤的TNM分期标准,确诊为ⅣA期或ⅣB期;(2)在郑州大学附属肿瘤医院首次接受安罗替尼治疗;(3)既往无其他恶性肿瘤病史;(4)病灶无法切除或发生远处转移或复发;(5)美国东部肿瘤协作组(Eastern Cooperative Oncology Group, ECOG)评分≤2分;(6)根据实体肿瘤疗效评价标准1.1有可测量的病变;(7)可接受血液学及肝肾功能等检查;(8)临床资料完整,可进行统计分析。本研究按照《赫尔辛基宣言》进行,并获得郑州大学附属肿瘤医院伦理委员会的批准(批件号:2021-083-002)。
2 .用药方案:
所有患者均接受安罗替尼单药治疗,初始治疗剂量为12 mg/d或10 mg/d,连续服用2周,停用1周,3周为1个疗程,具体初始剂量由至少2名临床医师根据患者病情及耐受性来确定。当患者出现与药物相关的3~4级不良反应时,药物剂量需减至10 mg/d或8 mg/d,直至出现疾病进展(progressive disease, PD)、死亡或不可接受的不良反应时停药。
3 .疗效和安全性评估:
记录患者的治疗反应、药物疗效、生存时间和不良反应。每疗程(3周)复查安全性指标,每1~2个疗程复查靶病灶大小,但若观察到PD表现,则立即进行评估。根据实体肿瘤疗效评价标准1.1评估肿瘤疗效,分为完全缓解(complete response, CR)、部分缓解(partial response, PR)、疾病稳定(stable disease, SD)和PD,同时评估PFS、ORR及DCR。本研究主要终点为PFS,次要终点为ORR和DCR。PFS定义为从开始用药到PD或因疾病导致死亡或末次随访的时间。ORR按(CR+PR)/总例数计算,DCR按(CR+PR+SD)/总例数计算。45例患者均接受门诊随访,随访截至2021年8月1日,随访时间为1.53~18.10个月,中位随访时间8.23个月,其中5例患者随访时间不足1.5个月,未进行疗效评估。
所有患者均根据美国国家癌症研究所常见不良反应事件分级标准对与治疗相关的不良反应进行评估和分级。
4 .统计学方法:
采用SPSS 26.0软件进行统计学分析,生存分析采用Kaplan-Meier法,生存率的比较采用Log rank检验。检验水准α=0.05。


1 .临床病理特征:
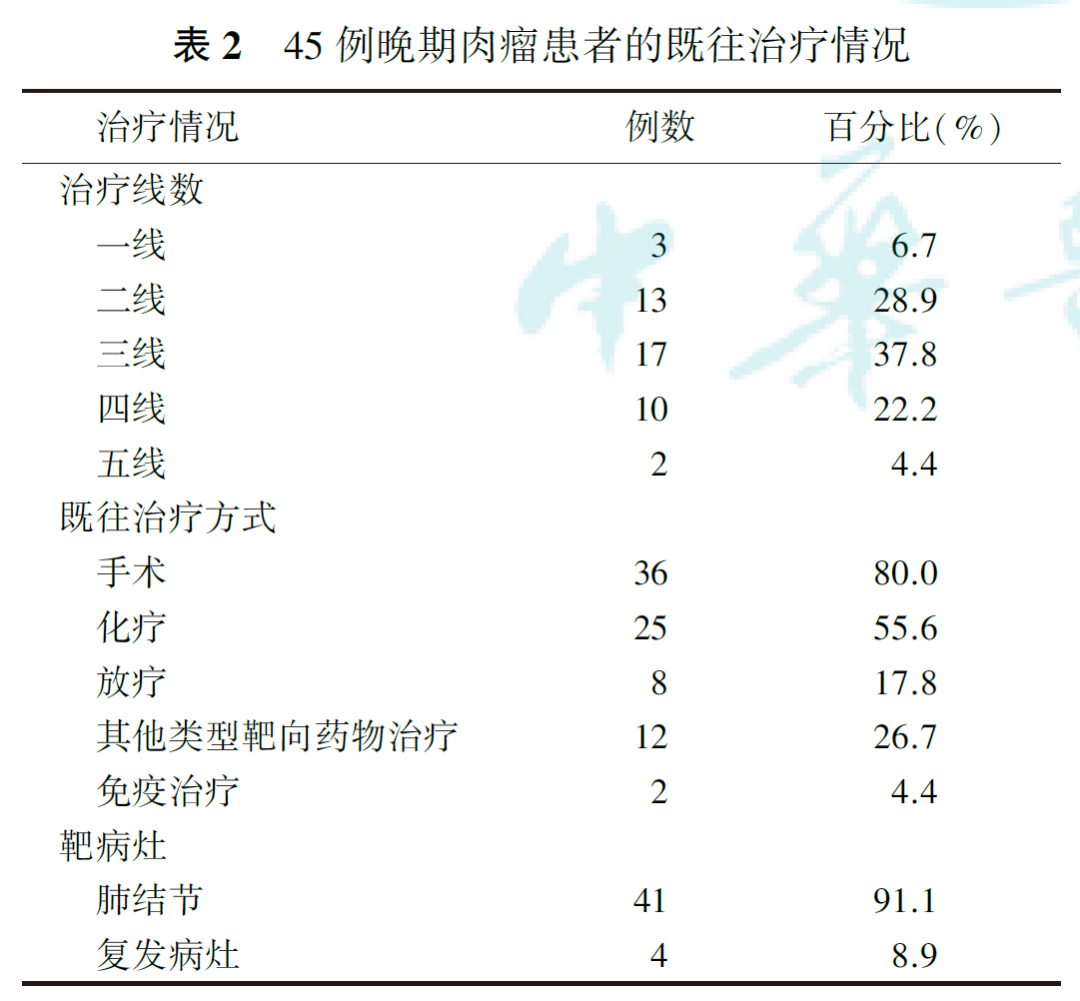
45例晚期肉瘤患者的年龄为8~79岁,中位年龄为43岁;男29例,女16例。36例患者既往接受了手术治疗,25例接受了化疗。治疗后有41例患者发生了肺转移。全组患者的临床病理特征详见表1,既往治疗情况见表2。

2 .疗效:
45例晚期肉瘤患者中,5例患者因用药时间过短(<1.5月)仅行安全性评估,40例患者同时纳入疗效评估和不良反应评估。
40例患者用药3个月后,无一例达到CR,PR 3例,SD 29例,PD 8例,ORR为7.5%(3/40),DCR为80.0%(32/40)。
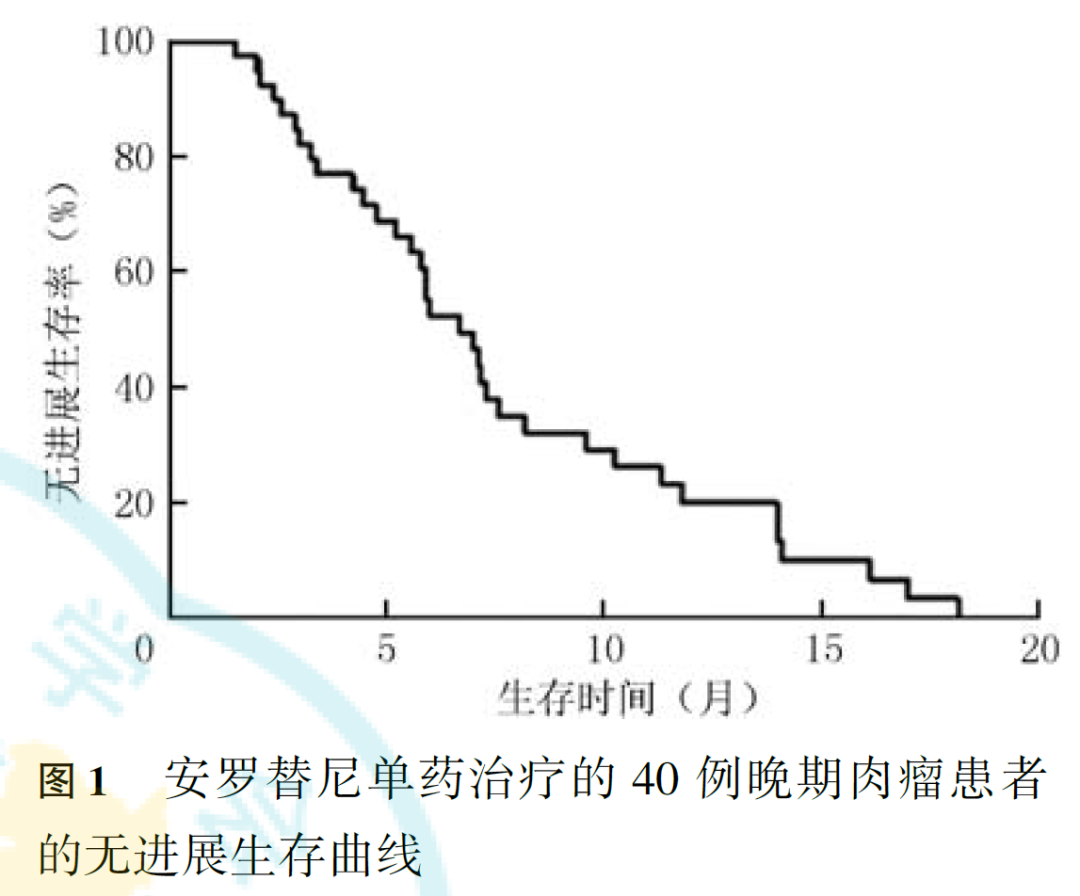
长期疗效方面,40例患者中,无一例达到CR,PR 1例,SD 10例,PD 29例。总体ORR为2.5%(1/40),DCR为27.5%(11/40),中位PFS为6.70个月(图1),中位总生存时间未达到。
3 .影响因素分析:
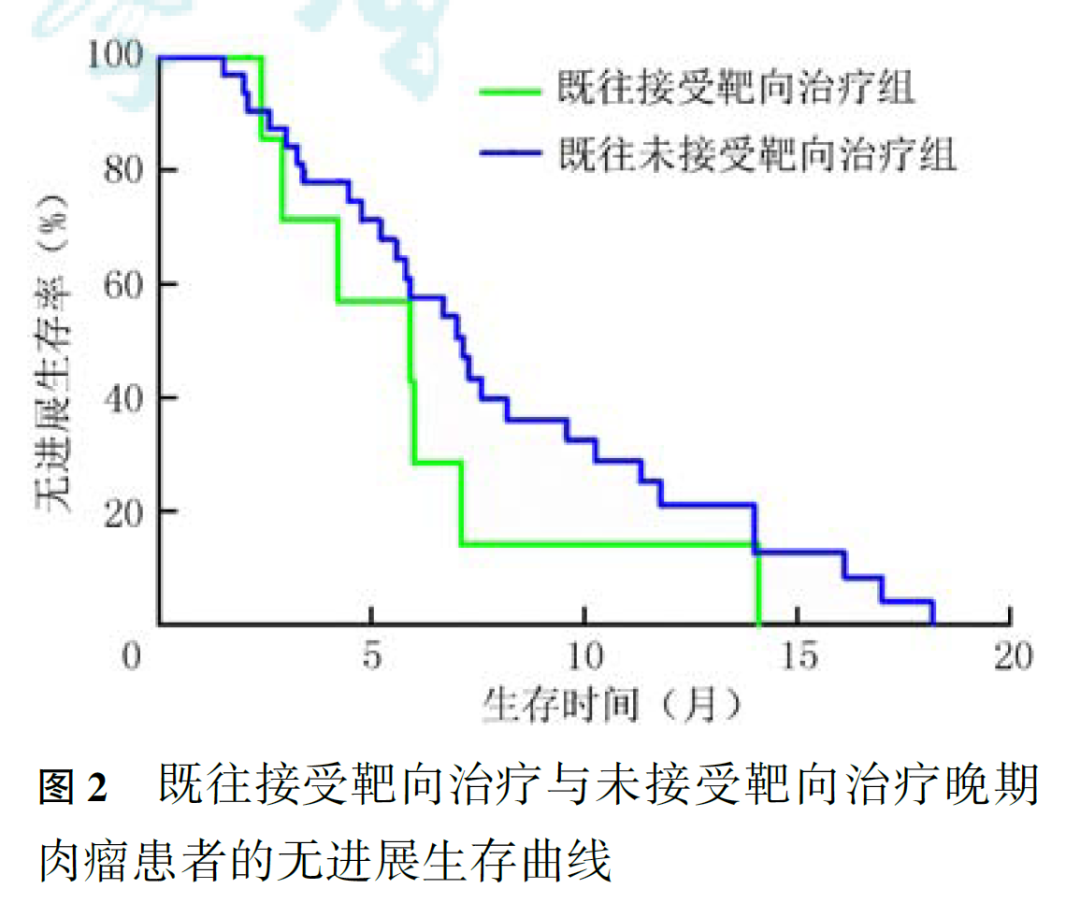
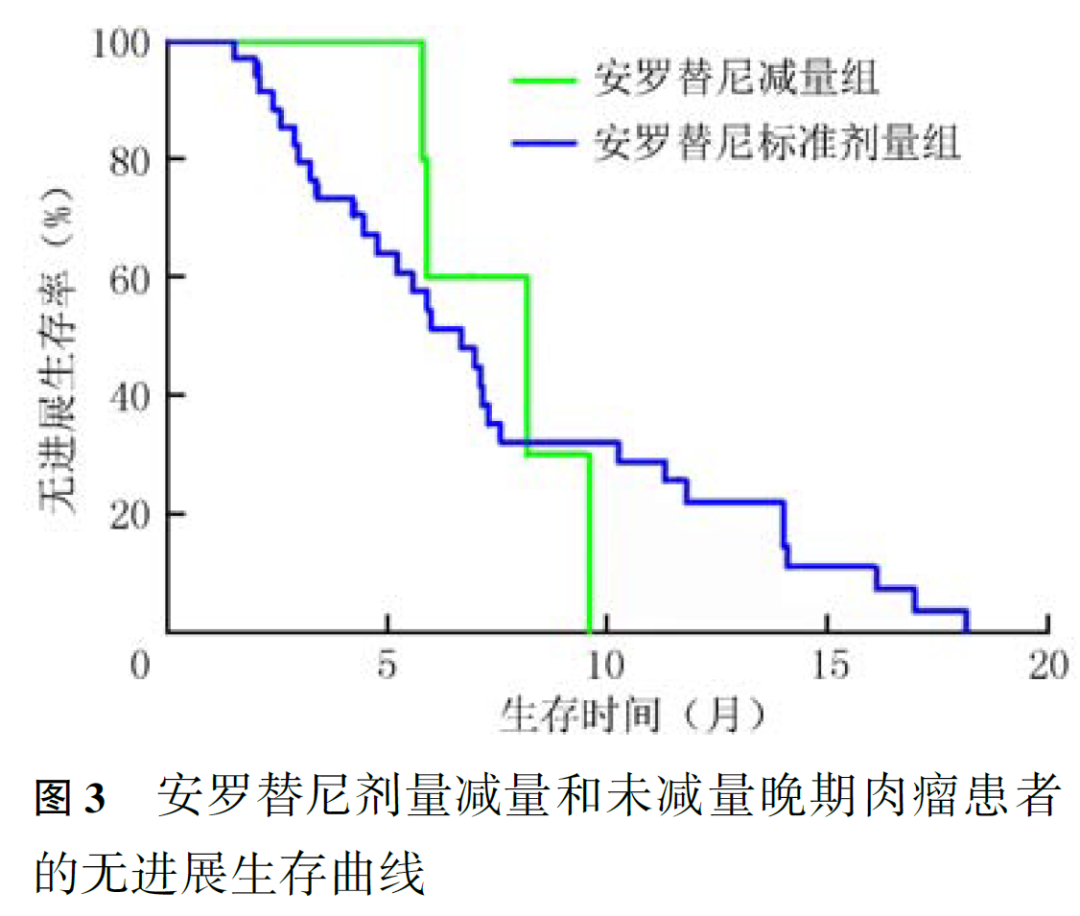
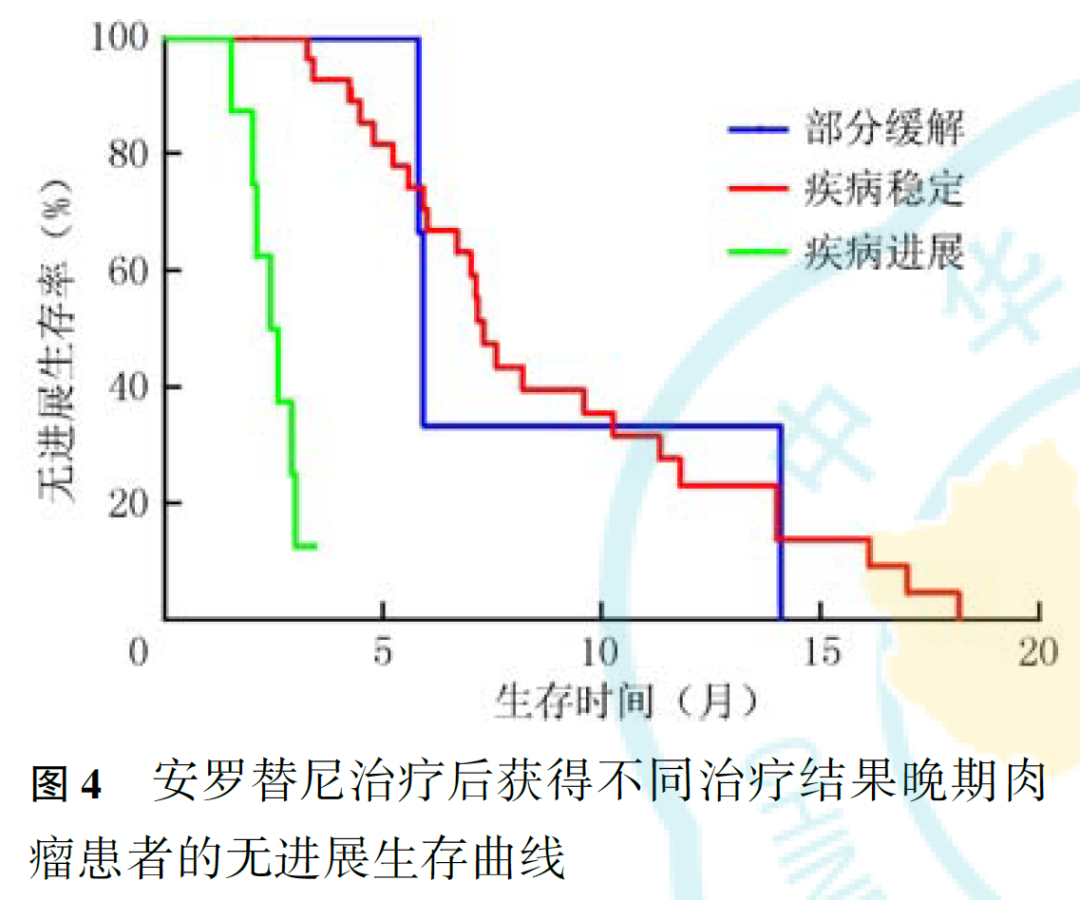
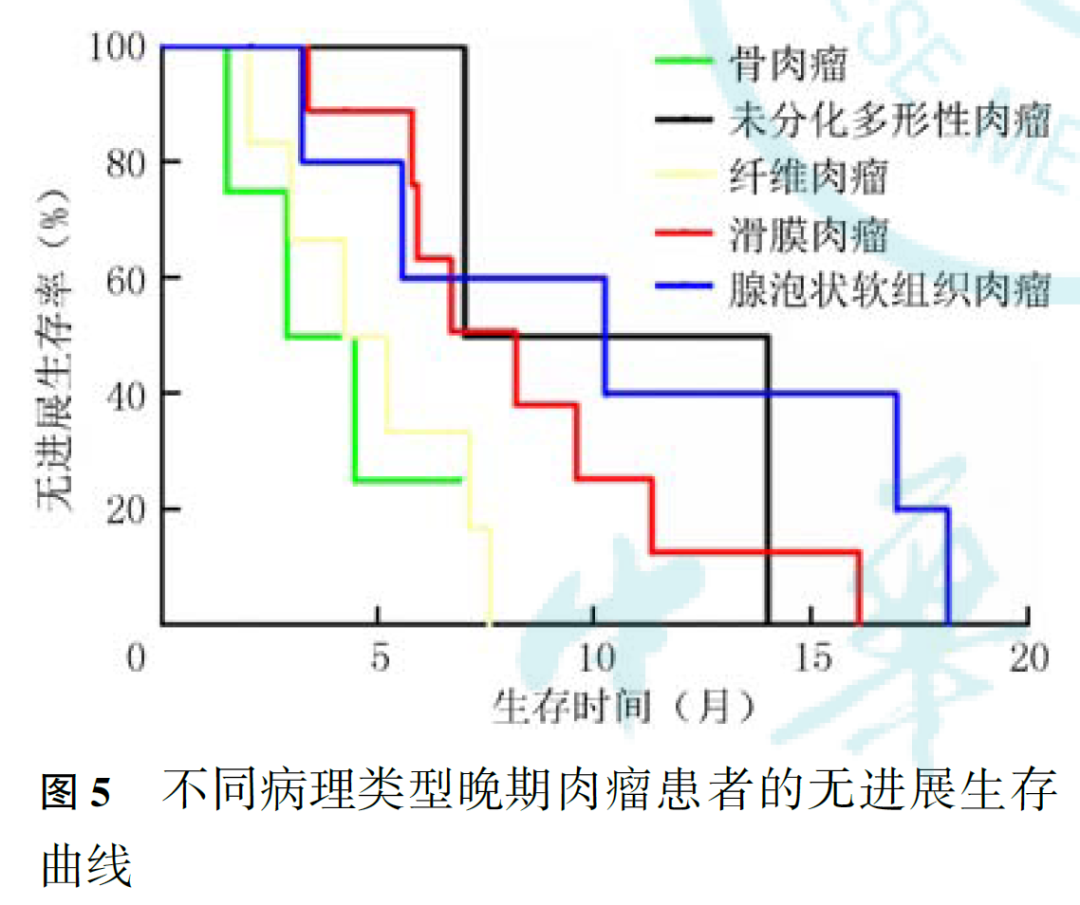
既往接受靶向治疗与未接受靶向治疗晚期肉瘤患者的中位PFS分别为5.93和7.17个月( P =0.260,图2),安罗替尼药物剂量减量和未减量晚期肉瘤患者的中位PFS分别为8.20和6.70个月( P =0.972,图3)。PR、SD患者的中位PFS(分别为5.93和7.30个月)长于PD患者(2.43个月, P <0.001;图4)。腺泡状软组织肉瘤患者中位PFS最长,为10.27个月,未分化多形性肉瘤、滑膜肉瘤、纤维肉瘤及骨肉瘤组的中位PFS分别为7.00、8.20、4.23和2.90个月,不同亚组间差异有统计学意义( P =0.048,图5)。
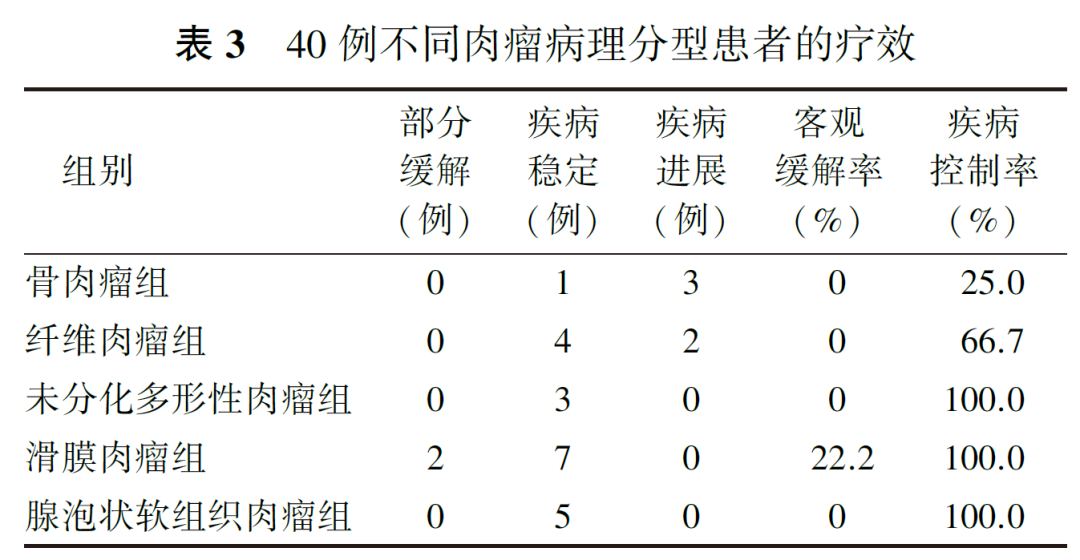
4 .不同肉瘤亚型的疗效对比:
骨肉瘤、纤维肉瘤、未分化多形性肉瘤、滑膜肉瘤和腺泡状软组织肉瘤组的ORR和DCR见表3,5组患者间的DCR差异有统计学意义( P =0.008)。进一步行多组DCR之间的两两比较,结果显示,滑膜肉瘤、腺泡状软组织肉瘤组患者的DCR(分别为100.0%和100.0%)明显优于骨肉瘤组(25.0%, P 值分别为0.014和0.048)。
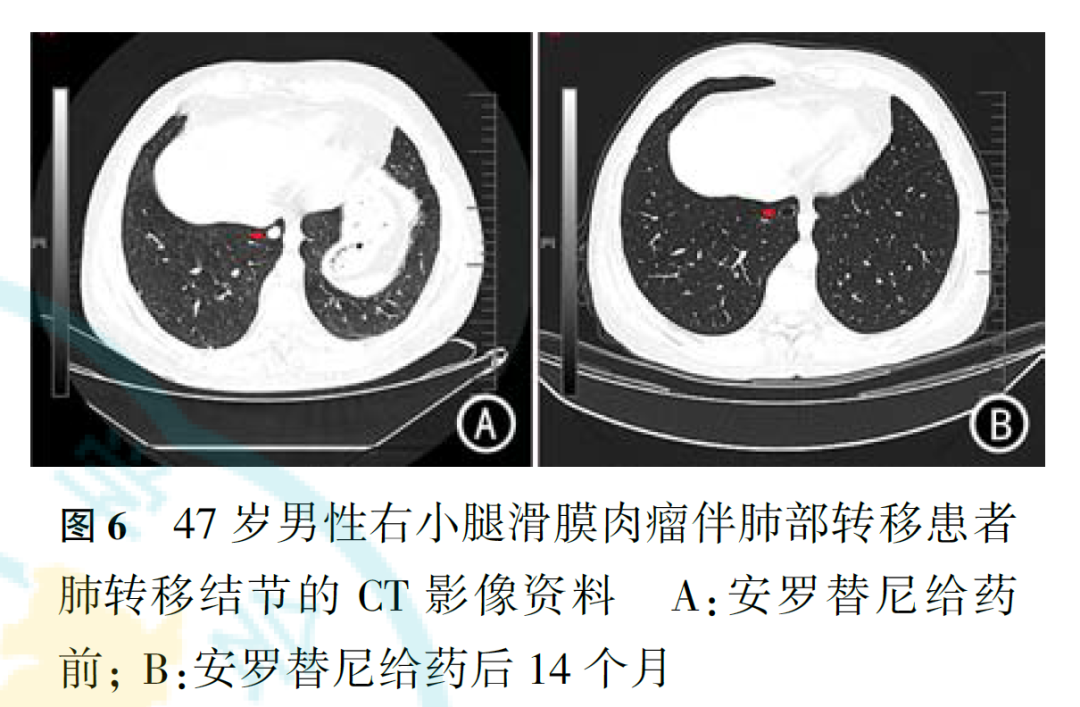
1例47岁男性滑膜肉瘤患者用药前后的肺部转移灶变化情况见图6。该患者诊断为右小腿滑膜肉瘤伴肺部转移,既往行手术及标准AI方案(阿霉素联合异环磷酰胺)化疗,后病情进展,于2019年9月至2020年11月应用安罗替尼治疗,用药后肺部转移灶可见明显缩小,且伴有空洞形成,该患者肿瘤疗效为PR。
5 .安全性评估:
45例患者均进行了安全性评估,共有29例患者出现不良反应(表4)。1~2级不良反应占所有不良反应的84.6%(44/52),3~4级不良反应占所有不良反应的15.4%(8/52)。45例患者的常见不良反应包括甲状腺功能减退(促甲状腺激素升高,8例,17.8%)、贫血(7例,15.6%)、乏力(5例,11.1%)、食欲减退(5例,11.1%)、肝功能减退(5例,11.1%)、白细胞减少(4例,8.9%)和手足综合征(4例,8.9%)等。
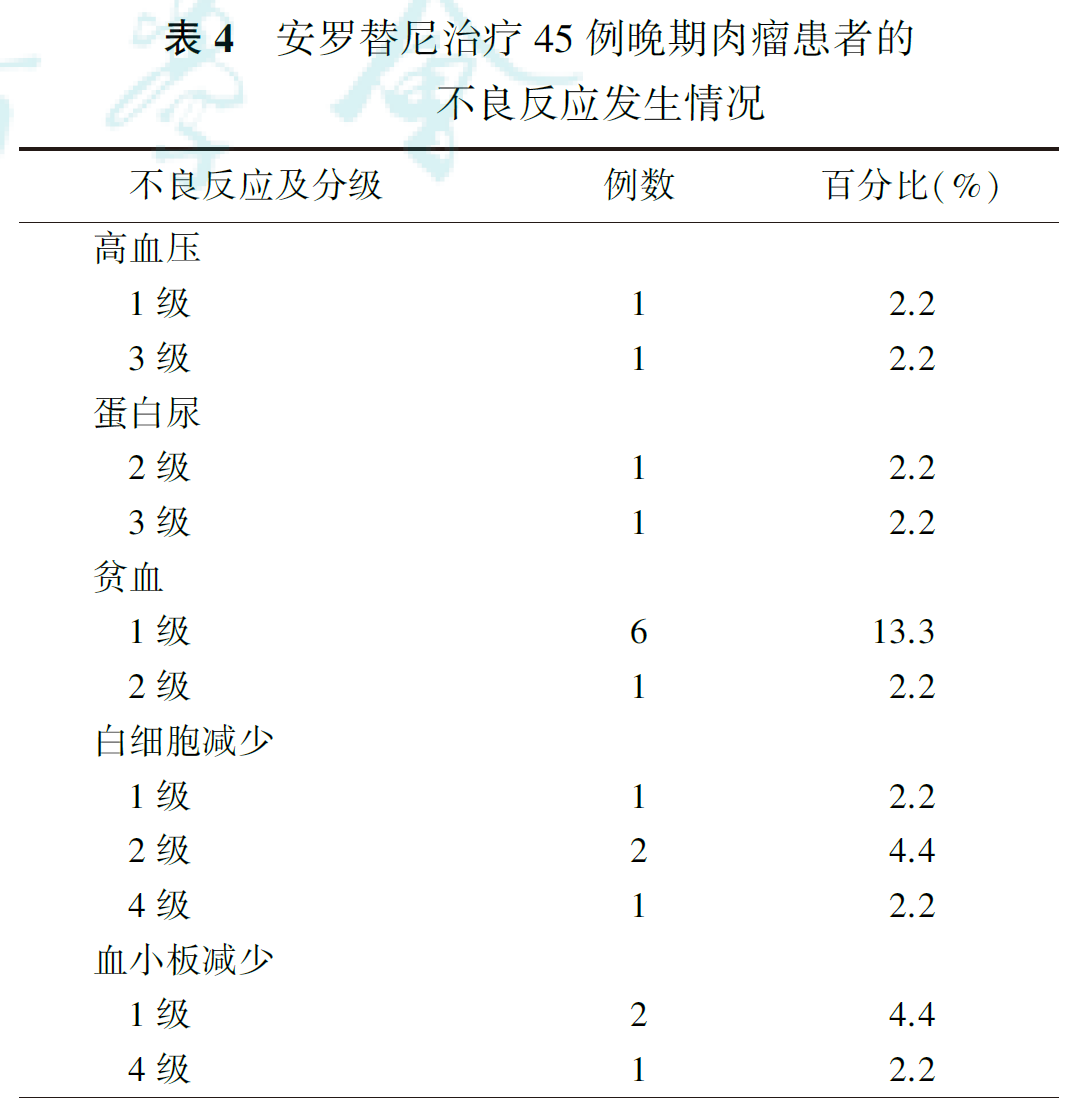
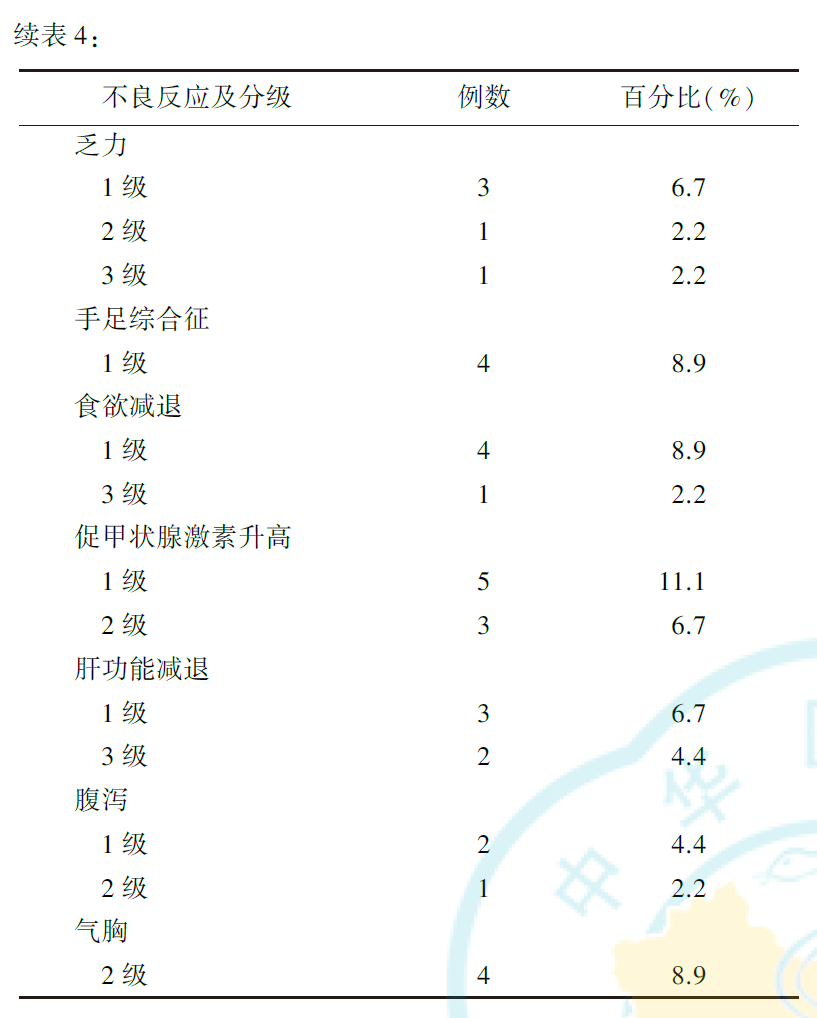
全组45例患者中,5例出现3级不良反应,常见的3级不良反应有肝功能减退(2例,4.4%)、高血压(1例,2.2%)、蛋白尿(1例,2.2%)、乏力(1例,2.2%)、食欲减退(1例,2.2%)。出现3级不良反应的5例患者未停止安罗替尼治疗,行减量和对症治疗后,不良反应逐渐好转。1例患者出现严重骨髓抑制,白细胞与血小板明显减少,评估为4级不良反应,被迫中止治疗。无患者因不良反应而死亡。
6 .治疗后不良反应与疗效间的关系:
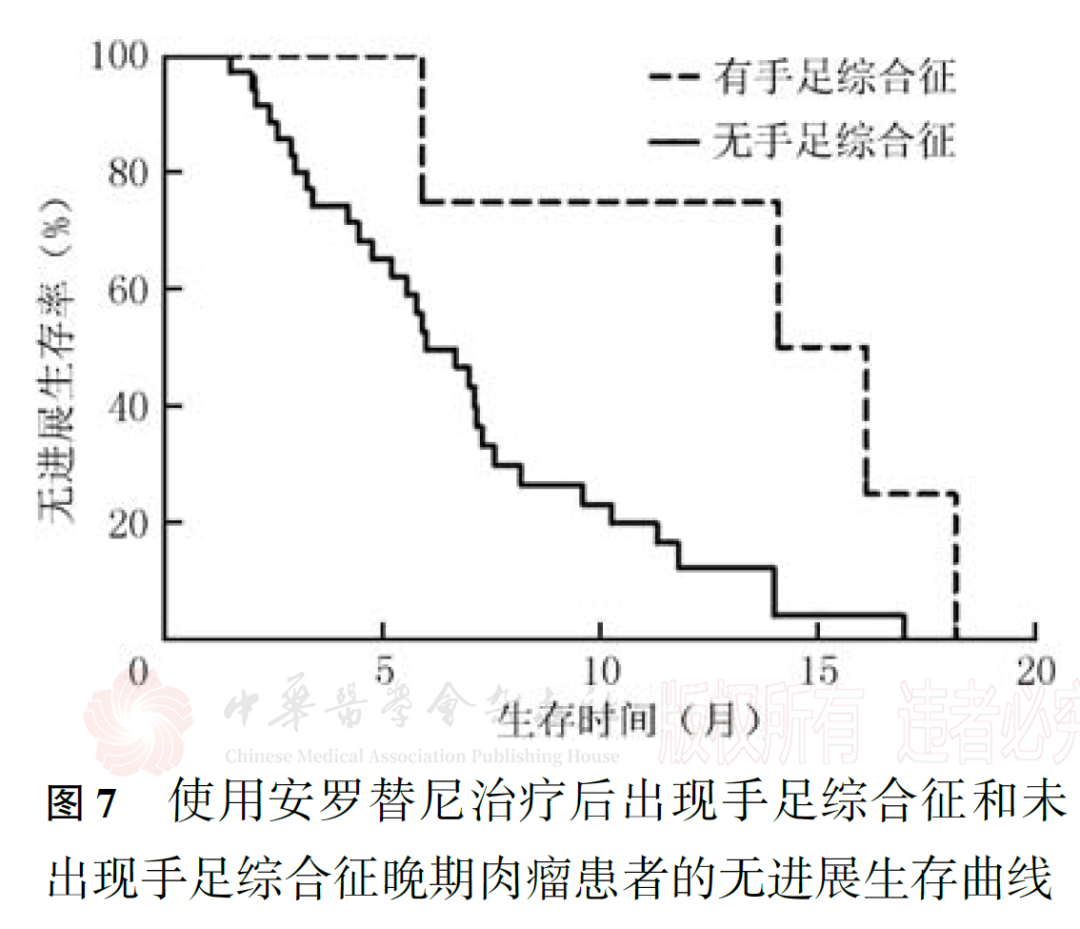
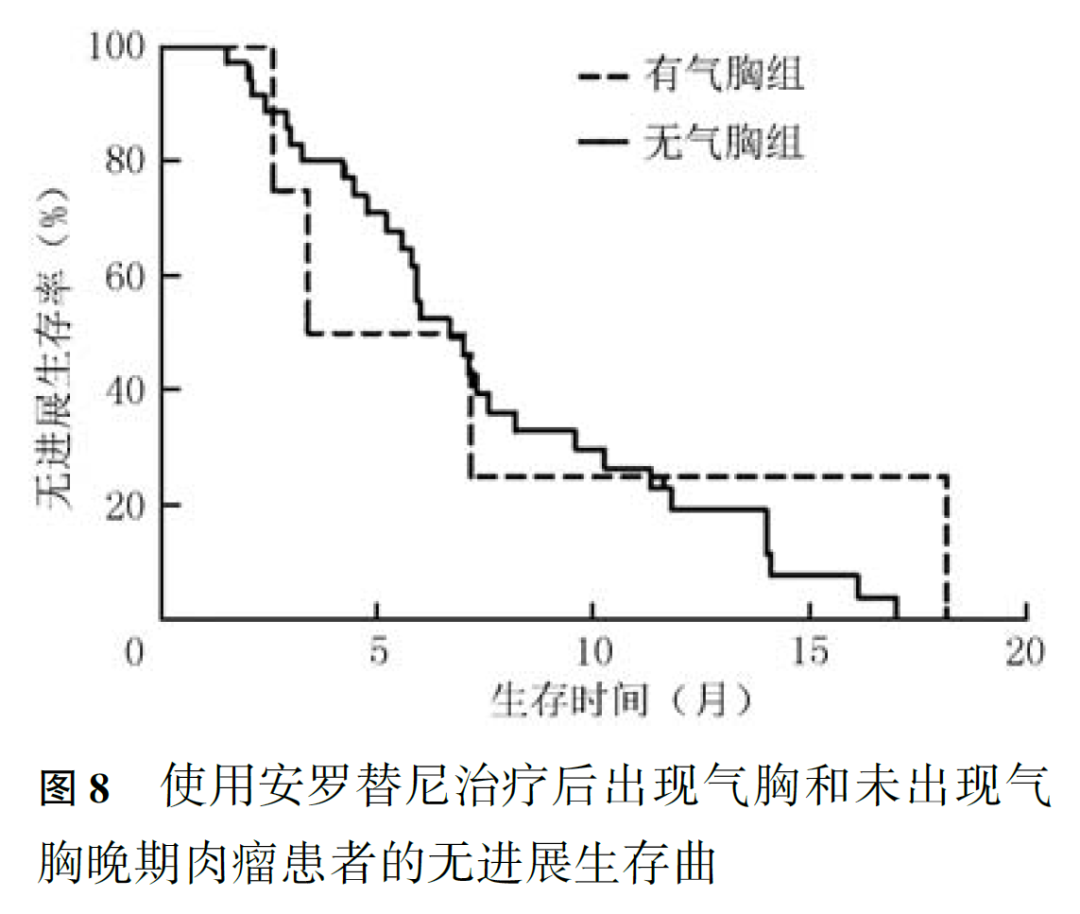
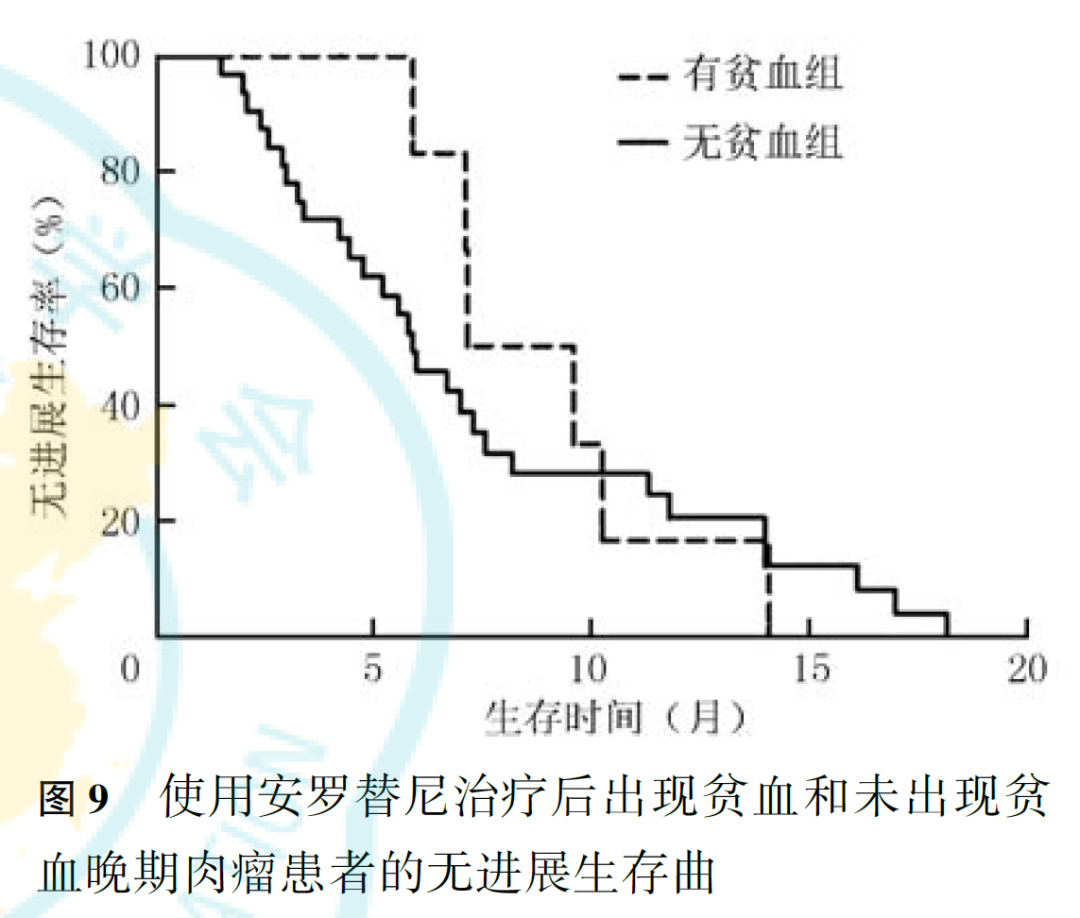
4例出现手足综合征患者的中位PFS(14.10个月)长于未出现手足综合征的患者(6.00个月, P =0.024;图7)。治疗后是否出现气胸和贫血的患者PFS差异无统计学意义( P 值分别为0.504和0.598;图8、图9)。


既往研究证实,血管生成在肿瘤的发生及进展中有重要作用。目前小分子靶向药物TKIs已被应用于肉瘤的治疗,且表现出不错的效果,包括帕唑帕尼、阿帕替尼、舒尼替尼、安罗替尼等。Palette研究为一项帕唑帕尼治疗晚期软组织肉瘤的Ⅲ期临床研究,结果显示,6%的患者达到PR,67%的患者达到SD,23%的患者为PD,中位PFS为4.6个月。Liu等报道阿帕替尼治疗肉瘤的ORR为23.68%,中位PFS为7.87个月,中位总生存时间为17.55个月,另外几项阿帕替尼的研究也报道了类似结果。一项研究报道结果显示,晚期肉瘤患者应用舒尼替尼治疗后,1.8%的患者达到PR,20%的患者达到SD。
本研究结果显示,40例肉瘤患者的3个月ORR为7.5%,DCR为80.0%,总体ORR为2.5%,DCR为27.5%,中位PFS为6.70个月。在本研究中安罗替尼的疗效略优于帕唑帕尼和舒尼替尼,而与阿帕替尼的疗效相似,两者的DCR和中位PFS相仿,遗憾的是本研究的ORR较低,此外本研究与Chi等报道的安罗替尼治疗肉瘤的疗效相似,虽然ORR较低,但中位PFS显著延长。
对影响PFS的因素进行分析,结果显示,安罗替尼治疗不同亚型肉瘤的疗效存在差异。腺泡状软组织肉瘤患者的疗效最佳,中位PFS为10.27个月,明显优于其他亚型的肉瘤。既往多项研究报道了类似的结果,例如,Stacchiotti等报道舒尼替尼治疗腺泡状软组织肉瘤的中位PFS为17个月,Stacchiotti等报道帕唑帕尼治疗腺泡状软组织肉瘤的中位PFS为13.6个月,Wang等报道阿帕替尼治疗腺泡状软组织肉瘤的中位PFS为18.53个月,Chi等报道安罗替尼治疗腺泡状软组织肉瘤的中位PFS为21个月。TKI治疗腺泡状软组织肉瘤的疗效优于其他亚型的原因尚未完全清楚,目前认为可能与以下几个因素相关,首先,腺泡状软组织肉瘤是一种惰性肉瘤,因此患者的生存期长于其他亚型的肉瘤;其次,由于肉瘤的高度异质性,导致不同亚型肉瘤对TKI的敏感度不同,有必要对不同肉瘤的靶点行进一步研究。
既往多项研究报道,转移性软组织肉瘤应用阿帕替尼治疗后的ORR高于骨肉瘤,但两者的DCR、中位PFS、中位生存时间等无明显差异。而Zhu等报道,与骨肉瘤相比,阿帕替尼有改善软组织肉瘤PFS的趋势。本研究中,安罗替尼治疗骨肉瘤的中位PFS为2.90个月,不及腺泡状软组织肉瘤、滑膜肉瘤、纤维肉瘤及未分化多形性肉瘤,与Zhu等的报道相符。此外,骨肉瘤组的DCR明显不及滑膜肉瘤和腺泡状软组织肉瘤组,差异有统计学意义。安罗替尼治疗骨肉瘤与软组织肉瘤产生疗效差异的原因尚未明确,可能与以下原因相关,首先,骨肉瘤与软组织肉瘤的生物学特征不同,导致对安罗替尼的敏感性不同;其次,骨肉瘤与软组织肉瘤的好发人群不同,骨肉瘤好发于儿童及青少年,而软组织肉瘤在成人中较多见。由于儿童与成人的身体条件、生理机制、免疫功能等存在差异,可能导致在安罗替尼治疗后产生不同的疗效;再者,两者在基因学与基因组学上存在明显不同,可能导致对靶向药物的敏感度及疗效产生差异。
本研究中,安罗替尼治疗肉瘤的安全性良好,大多数患者只出现了1、2级不良反应。常见的不良反应有甲状腺功能减退(促甲状腺激素升高)、贫血、乏力、食欲减退、肝功能减退、白细胞减少和手足综合征等,与既往报道的安罗替尼的不良反应相似。有1例患者出现严重骨髓抑制,Wang等也有类似的报道,因此在治疗过程中要及时监测患者的血常规等检查,以及时发现骨髓抑制并妥善处理。
阿帕替尼治疗软组织肉瘤后出现高血压、手足综合征、蛋白尿等不良反应患者的生存时间长于未出现不良反应的患者,而ORR、DCR及PFS等无明显差异,Liao等也报道了类似的结果。本研究中,多数患者未达到中位生存时间,因此无法评估不良反应与骨肉瘤之间的关系。但在本研究中,4例出现手足综合征患者的PFS长于未出现手足综合征的患者(分别为14.10和6.00月, P =0.024),而气胸和贫血的出现与PFS无关。关于不良反应与临床疗效间关系的原因仍未明确,需纳入更多例数患者进一步探讨两者间的关系。
综上所述,本研究显示,安罗替尼治疗腺泡状软组织肉瘤、滑膜肉瘤的疗效优于其他亚型肉瘤,治疗后出现手足综合征患者的PFS长于未出现患者。本研究存在一定的局限性。首先,本研究是回顾性研究,且未设立对照组;其次,某些亚型纳入的患者例数较少,鉴于肉瘤的异质性,在进行不同亚组间疗效分析时可能会出现偏差;第三,患者接受的既往治疗方案不同,可能会对结果产生一定的影响。最后,本研究仅局限于临床评价,未进行靶点及分子生物学的监测研究。
链接:http://www.lewenyixue.com/2024/10/21/%E5%AE%89%E7%BD%97%E6%9B%BF%E5%B0%BC%E6%B2%BB%E7%96%97%E6%99%9A%E6%9C%9F%E8%82%89%E7%98%A4%E7%9A%84%E6%9C%89%E6%95%88%E6%80%A7%E5%92%8C%E5%AE%89%E5%85%A8%E6%80%A7%E5%88%86%E6%9E%90/