前沿分享 | 基于衰老细胞核特征采用深度学习技术预测乳腺癌风险

近期,Indra Heckenbach等人在 The Lancet Digital Health上发表了题为“ Deep learning assessment of senescence-associated nuclear morphologies in mammary tissue from healthy female donors to predict future risk of breast cancer: a retrospective cohort study”的研究论文,深度探讨了细胞衰老(senescence)在乳腺癌(BC)发生发展过程中的作用。该研究团队开发了一种基于细胞核形态的单细胞深度学习衰老预测器——NUSP,随后用被不同因素诱发的衰老细胞训练所构建的多个模型预测终末导管小叶单位(TDLU)和非终末导管小叶单位的上皮、基质和脂肪组织区域的衰老。这些模型通过分析健康乳腺组织标本中的细胞衰老特征来预测其未来癌症风险。同时,该研究表明联合多种模型以及Gail评分(目前评估罹患乳腺癌的临床金标准),能够显著提高癌症预测的精确性,为BC的早期干预提供了有效指导。
BC是全球女性最常见的癌症之一,且具有较高的死亡率。仅在美国,每年就有近29万例发病病例和4万余例死亡 病 例。年龄是BC的主要风险因素之一,超过80%的病例发生在50岁以后。因此,细胞衰老可能在BC发生发展过程中扮演重要角色,然而目前衰老在癌症发展过程中的确切作用尚不明朗。
该研究旨在通过分析健康乳腺组织标本中的细胞衰老情况,来探索其与BC风险之间的联系。研究使用了深度学习技术来分析细胞核形态,以预测不同组织类型的细胞衰老,并探讨这些衰老细胞是否可作为BC的预测指标及其预测的精准性。
该队列研究涉及4382名健康女性(年龄中位数为45岁,四分位数间距为34-57岁),回顾分析了2009年至2019年期间来源于印第安纳大学西蒙癌症中心科曼组织库(KTB)的健康女性乳腺组织标本。截至数据截止日期(2022年7月31日),这些研究对象中已有86人确诊为BC,平均诊断时间为4.8年(标准差,SD为2.84年)。
1)研究者从KTB获取4382名健康女性捐赠的乳腺组织标本对应的HE染色组织学图像以及包含人口统计学资料和临床特征等信息的问卷(由参与者在捐赠时填写);
2)基于NUSP在经过电离辐射(IR)、复制性衰老(RS)、抗霉素A(antimycin A)、阿扎那韦-利托那韦(atazanavir–ritonavir)、多柔比星(doxorubicin)等因素诱导衰老的成纤维细胞上进行训练。由于药物治疗的高度相关性,用其相同的图像训练产生新模型--AAD模型;除此之外,基于IR、RS诱导衰老的细胞训练对应IR模型以及RS模型,而Unified模型包括前述所有因素;
3)使用多个经验证模型(Unified、IR、RS及AAD)对TDLU和非终末导管小叶单位的上皮、基质和脂肪组织区域进行衰老预测并生成评分。 并且使用UMAP(一种用于降维的机器学习技术)对组织样本中的细胞核进行分类和可视化以协助组织类型的分割。 为了对基于衰老的癌症预测结果进行基准标记,该研究根据乳腺组织捐赠时的特征为所有≥35岁的参与者生成了5年的Gail评分(从研究对象的病史和生育史及其一级亲属中的BC病史等方面估计未来5年内发生BC的概率);
4)根据纳入女性在数据截止日期(2022年7月31日)之前的患病情况将其划分为病例组(已确诊为BC)和对照组(未罹患BC)。使用统计学方法对两组人群的人口统计学资料和临床特征进行描述和对比分析。进一步使用逻辑回归模型分析四种组织区域的衰老评分和BC发病率之间的相关性;
5)使用逻辑回归模型对与BC有显著相关性的组织区域的模型结果进行交叉分类分析,并对与BC有独立关联的协变量进行调整。
1)研究者使用UMAP技术发现聚类按组织类型分离,这表明分割方法是稳健的( 见图1 );
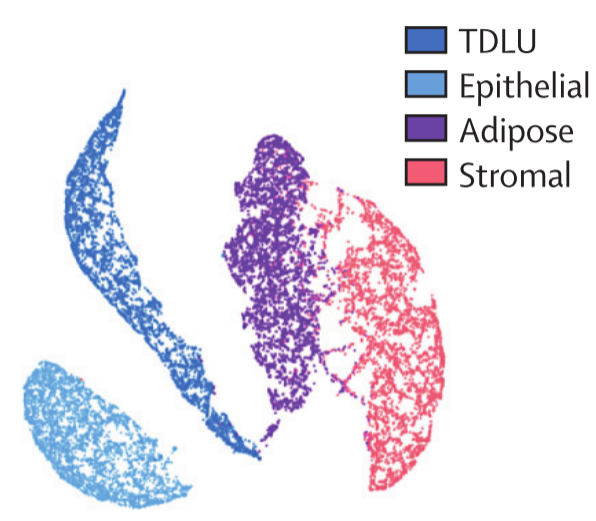
图1 单个组织的形态学指标UMAP情况
2)该研究可视化具有高预测衰老(分数超过第90百分位数)的细胞核揭示了整个组织的空间分布,其在TDLU和上皮组织区域大量聚集( 见图2 );
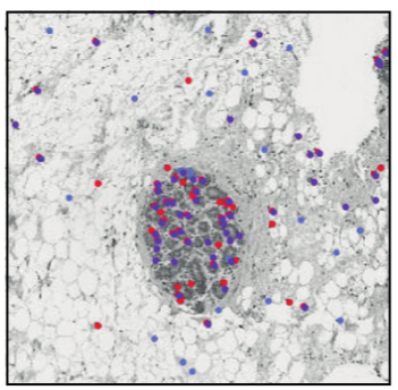
图2 显示预测衰老程度高的细胞核的代表性组织学图像(红色为IR模型,紫色为RS模型,蓝色为AAD模型)
3)高评分衰老细胞核周围的衰老空间分布类似于指数衰减,进一步支持了旁分泌SASP因子通过局部扩散传播衰老的假设( 见图3a-d );
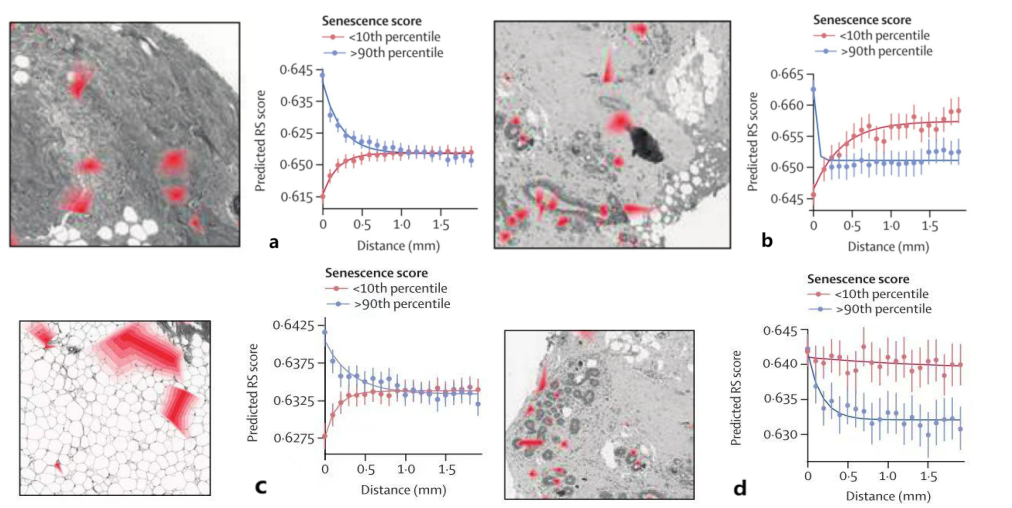
图3 代表性图像以及与之对应的指数拟合曲线【 (a)-(d)依次为基质、上皮组织、脂肪、TDLU组织 】
4)研究发现IR模型和RS模型均与AAD模型呈负相关,且相互之间相关性较弱( 见图4 )。因此,研究者推测这些模型捕获了三种相对不同的衰老表型;
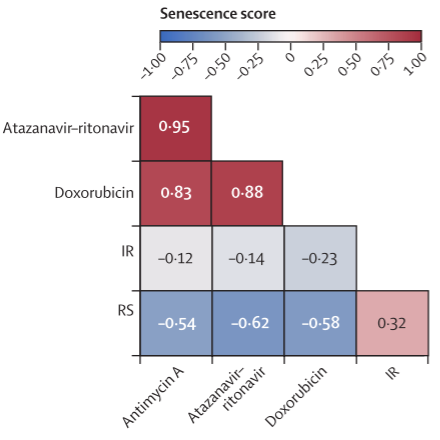
图4 细胞核衰老模型之间的相关性
5)在这三种模型中,研究者发现了个体间每种组织类型的平均衰老评分之间的相关性。同时,他们发现了几种组织之间(最值得注意的是脂肪和基质组织)的中度相关性( 见图5 )。推测可能与个体的系统暴露或他们对压力源的反应有关;
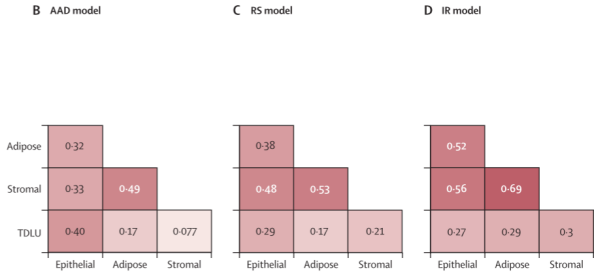
图5 不同组织在同一衰老模型之间的相关性
6)研究者使用Unified模型发现病例组的平均预测衰老评分与对照组显著不同——它在三个组织区域(基质、脂肪和非终末导管小叶单位上皮组织)中评分较低( 见图6 )。衰老可能在这三个组织区域中具有保护作用,从而降低发生癌症的风险。值得注意的是,活检是在诊断前平均4.8年(SD为2.84年)进行的,这表明预测的衰老评分可能是恶性肿瘤风险的关键指标。该研究还应用于IR、RS和AAD模型,以评估不同类型的衰老是否会影响致癌作用。研究者观察到IR模型的所有细胞类型、RS模型的脂肪和基质组织以及AAD模型的上皮、脂肪和基质组织的平均预测衰老评分的显著差异( 见图6 ),表明不同类型的衰老可能会对癌症的发生发展起到不同作用;
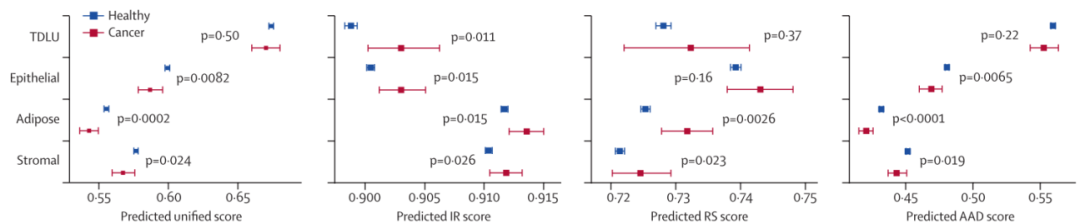
图6 不同模型对病例组和对照组的四个区域组织平均衰老评分的比较结果
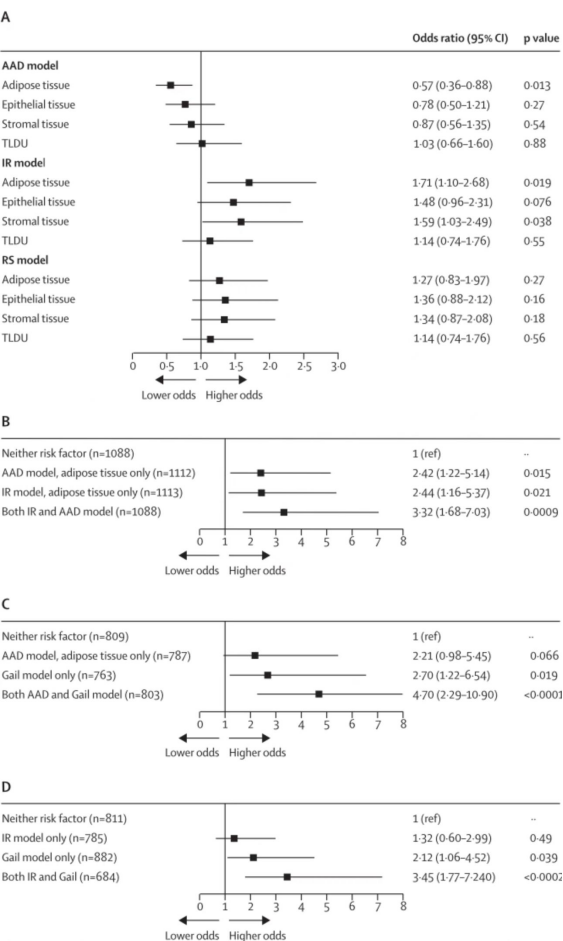
7)研究者用不同形式的衰老预测BC发生的概率,并将病例组和对照组结果进行对比分析,发现( 见图7 ):
①脂肪组织IR模型评分高于中位个体乳腺癌发生概率显著较高(OR:1.71, P =0.019);
②脂肪组织AAD模型评分高于中位个体乳腺癌发生概率显著较低(OR:0.57, P =0.013);
③具有两种脂肪风险因素(IR&AAD)个体乳腺癌发生概率显著较高(OR:3.32, P =0.0009);
④与Gail评分模型联合:个体乳腺癌发生概率均显著提高——AAD风险模型:OR : 4.70, P <0.0001;IR风险模型:OR : 3.45, P <0.0002。
这篇文章提供了有关细胞衰老与BC发生风险之间关系的新见解,并展示了利用深度学习模型预测组织特异性衰老分数的潜力。该研究对新的癌症风险评估工具提供一定启发,并为BC的 预防治疗策略提供了潜在的靶点。
文献来源:
Heckenbach,I. , Powell,M. , Fuller,S. , Henry,J. , Rysdyk,S. , Cui,J. , Teklu,A.A. , Verdin,E. , Benz,C. ,& Scheibye-knudsen , M.(2024).Deep learning assessment of senescence-associated nuclear morphologies in mammary tissue from healthy female donors to predict future risk of breast cancer: a retrospective cohort study.The Lancet Digital Health,6(10),e681-e690.https://doi.org/10.1016/S2589-7500(24)00150-X.
原文链接:
https://www.thelancet.com/journals/landig/article/PIIS2589-7500(24)00150-X/fulltext
魏梦姣
本硕就读于山东大学齐鲁医学院—临床医学5+3一体化专业(研究方向为甲状腺乳腺疾病的临床及基础研究); 博士在读于重庆大学智能肿瘤学教育部医药基础研究创新中心(研究方向为乳腺肿瘤学)。 曾参与省重点研发项目,目前已发表文章2篇,以第一作者身份发表文章1篇。
版权声明:本文为“乐问号”作者或机构在乐问医学上传并发布,仅代表该作者或机构观点,不代表乐问医学的观点或立场,不能作为个体诊疗依据,如有不适,请结合自身情况寻求医生的针对性治疗。
链接:http://www.lewenyixue.com/2024/10/15/%E5%89%8D%E6%B2%BF%E5%88%86%E4%BA%AB%20%7C%20%E5%9F%BA%E4%BA%8E%E8%A1%B0%E8%80%81%E7%BB%86%E8%83%9E%E6%A0%B8%E7%89%B9%E5%BE%81%E9%87%87%E7%94%A8%E6%B7%B1%E5%BA%A6/
THE END











