5天肿瘤几乎完全消失?CAR-T疗法本月多次登上NEJM顶刊!
CAR-T细胞疗法为血液肿瘤治疗带来了革命性突破,然而,由于实体瘤具有肿瘤异质性强、靶抗原选择有限、T细胞浸润率低、免疫抑制肿瘤微环境(TME)等特点,在实体瘤治疗领域进展缓慢。
脑肿瘤是最常见的实体瘤,由于血脑屏障的半透性特性而呈现出更多的困难点。今年3月,《Nature Medicine》、《NEJM》全球知名杂志公布了CAR-T细胞疗法治疗脑肿瘤的最新研究数据。
CAR-T细胞治疗脑肿瘤有3大策略
CAR-T细胞是一种基因改造的T细胞,可以识别癌细胞表面的抗原,而不依赖人类主要组织相容性复合体(MHC)分子,与天然T细胞相比,能区分更广泛的靶标。当CAR-T细胞与靶向抗原结合时,它们被激活并充当攻击肿瘤的“活性药物”。
血脑屏障是保护大脑免受有害毒素和化学物质侵害的主要成分,是一种独特的物理屏障,但给CAR-T的递送带来了挑战。因此,许多研究人员将重点放在局部和直接CAR-T细胞递送治疗脑肿瘤上。
目前,CAR-T细胞在脑肿瘤的临床应用上包括静脉注射、肿瘤内注射和脑室内注射。
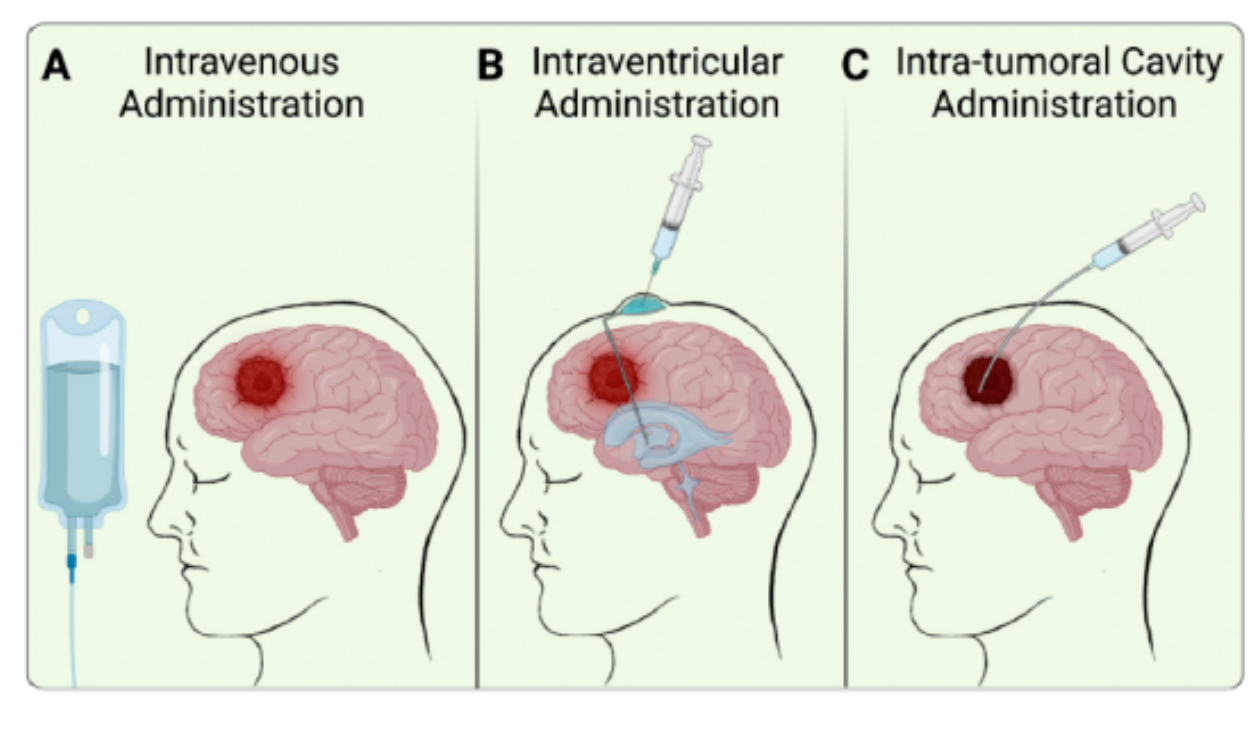
CAR-T细胞治疗脑肿瘤的机制(A)静脉注射 (B)局部脑室内递送 (C) 肿瘤内注射
策略一:静脉注射
目前,静脉注射CAR-T细胞是临床试验中最常见的递送途径。静脉注射CAR-T细胞治疗实体瘤具有挑战性,因为这些细胞很难在TME内定位、浸润和扩张。
策略二:肿瘤内注射
CAR-T细胞也可以直接注射到肿瘤腔内,不需要CAR-T细胞穿过血脑屏障迁移。
策略三:局部脑室内递送
局部脑室内(ICV)递送包括将CAR-T细胞通过脑室系统注射到脑脊液中。在先前的脑肿瘤CAR-T治疗中,ICV首次用于复发性胶质母细胞瘤患者,并导致所有中枢神经系统肿瘤消退。
直接向脑肿瘤局部注射CAR-T细胞,50%患者病情稳定至少2个月
3月7日,美国的一个研究团队在《Nature Medicine》发表了一篇关于CAR-T治疗脑肿瘤的文章,该研究将CAR-T细胞直接注入脑肿瘤和脑脊液中。

《Nature Medicine》截图
这项开创性的局部递送CAR-T细胞疗法的1期临床试验,在脑肿瘤治疗领域显示出了良好的临床效果,同时是迄今为止报道的最大规模的实体瘤CAR-T细胞治疗临床试验。
该研究评估了靶向肿瘤相关抗原白细胞介素-13受体α2(IL13Rα2,在大多数胶质母细胞瘤中过度表达的肿瘤相关抗原)的CAR-T细胞,在65名复发性高级别胶质瘤患者中的安全性和有效性,其中大多数是复发性胶质母细胞瘤 (rGBM)。
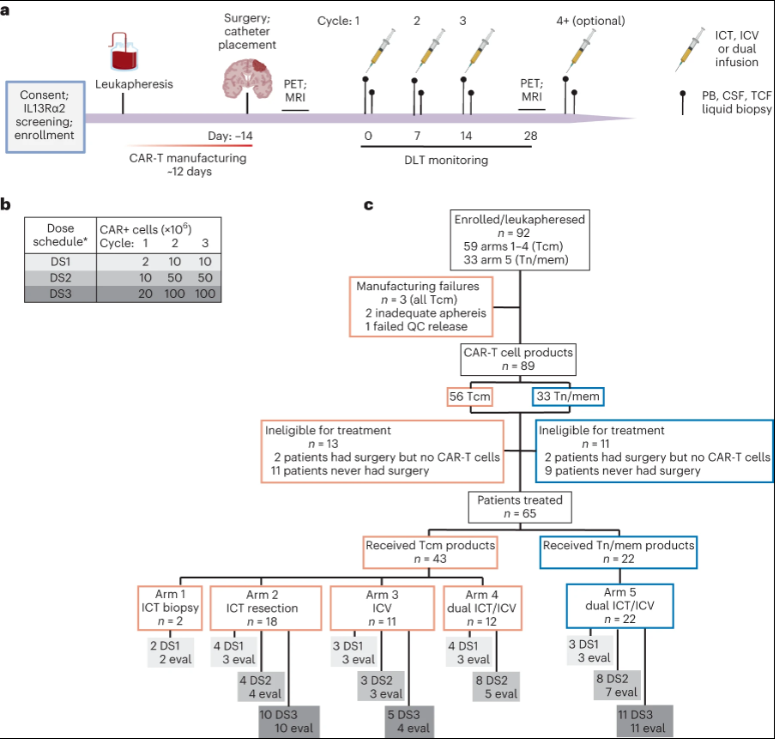
研究设计与治疗方案
研究者设计了三种局部T细胞给药途径,即直接注射到肿瘤部位(肿瘤内,ICT)、注入脑脊液(脑室内,ICV),或同时注射到这两个区域(双重ICT/ICV),还设计了两种制造平台,最终形成了第5组,该组利用了双重ICT/ICV给药和优化的制造工艺。
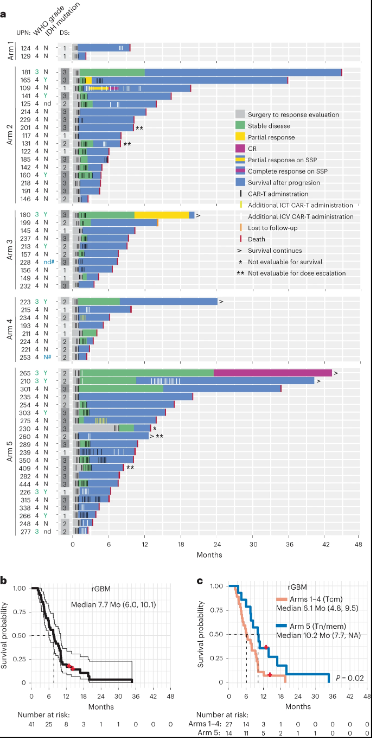
局部递送的IL-13Rα2-CAR-T细胞的临床活性
65名患者至少接受了一次CAR-T细胞输注,58名患者接受了至少3次CAR-T细胞输注,且疗效可评估。在这58名患者中,29名(50%)患者在CAR-T细胞治疗后病情稳定至少两个月。其中,2例部分缓解,2例完全缓解。
在生存期方面,所有患者的中位总生存期(OS)为7.7个月,第 5组实现了10.2个月的最佳OS,第 1-4 组OS仅为6.1个月。
试验中,患者耐受良好,所有组中没有剂量限制毒性。另外,可能与治疗相关的3+级毒性为1例3级脑病、1例3级共济失调。
3名患者复发后用CAR-T细胞治疗,1-5天内肿瘤缩小,短期疗效显著!
3月13日,国际顶尖医学期刊《NEJM》上刊登了一篇研究论文,3名患者应用CAR-T细胞疗法联合疗法后,1-5天内肿瘤快速缩小,其中1名患者的肿瘤“几乎完全”消失。

《NEJM》截图
研究团队之前开发了靶向表皮生长因子受体变异型III(EGFRv3)的CAR-T细胞疗法,EGFRv3是一种胶质母细胞瘤的肿瘤特异性抗原(该突变在正常脑细胞中不表达,在80%以上的胶质母细胞瘤患者中表达),但该疗法在单独使用时效果有限。
因此,研究团队采用一种创新策略,将CAR-T细胞疗法和双特异性抗体两种癌症治疗策略结合起来,让靶向EGFRv3的CAR-T细胞表达并分泌靶向野生型EGFR的T细胞结合抗体分子(TEAM),即CAR-TEAM疗法,并首次在复发性胶质母细胞瘤患者中进行脑室内递送。
这是一项非随机、开放标签、单中心的1期临床试验,2023年3月到2023年7月,3名复发性胶质母细胞瘤患者入组,研究团队收集了患者的T细胞,并转化为新型CAR-TEAM细胞,然后将其注射到患者大脑中,主要为单次输注10×10^6CAR阳性CARv3-TEAM-E T细胞。
这3名患者此前均接受了标准的放疗和替莫唑胺化疗,并在疾病复发后入组接受这项临床试验,其中患者2的数据最为亮眼。
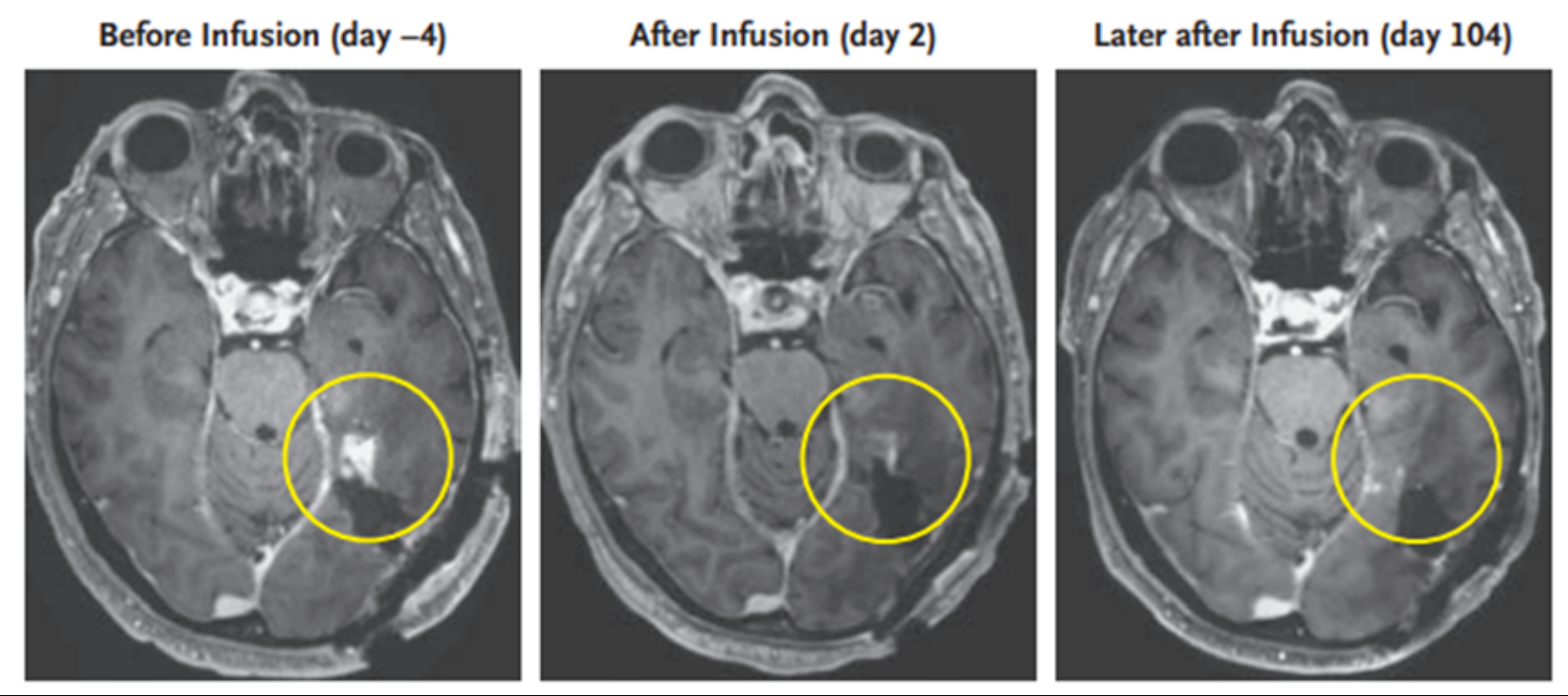
患者2的MRI扫描结果
患者1:74岁男性,在单次输入CAR-TEAM细胞治疗后,肿瘤迅速消退,但只是暂时的。血液和脑脊液中EGFRvIII和EGFR拷贝数下降,最终变得不可检测。
患者2:72岁男性,治疗后第2天,核磁共振(MRI)扫描结果显示肿瘤缩小了18.5%,到第69天时,患者的肿瘤比治疗开始时缩小了60.7%。
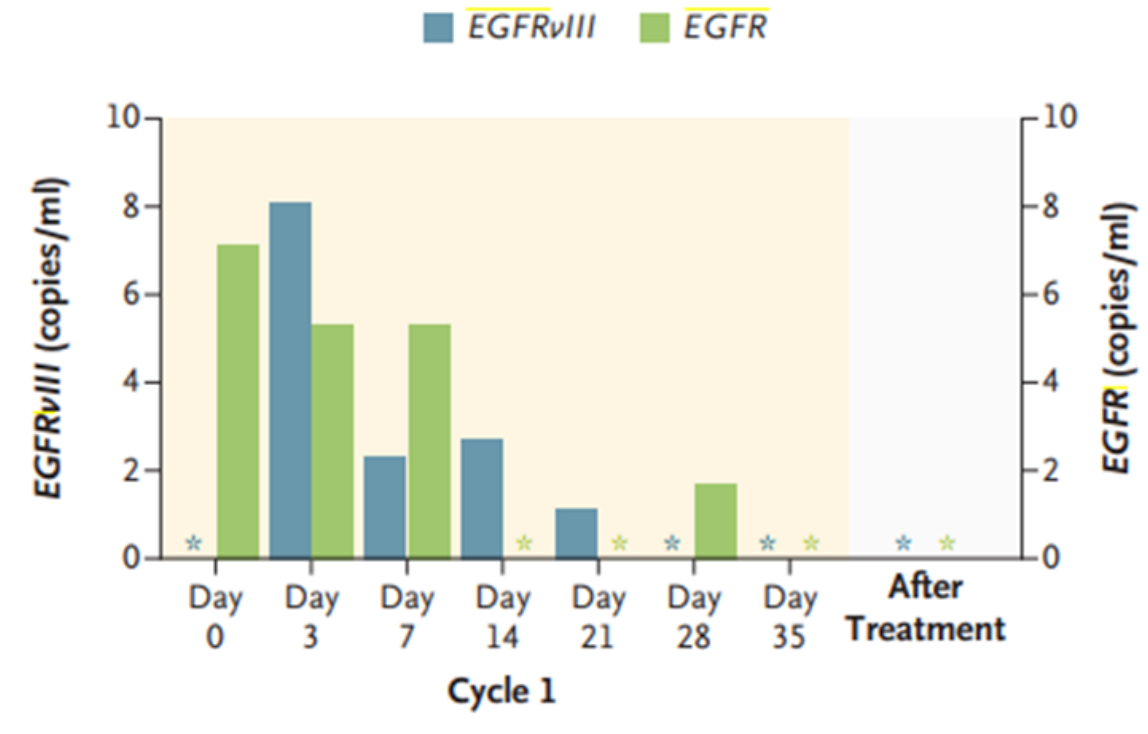
患者2的脑脊液液体活检结果
同时,在接受单次输注CARv3-TEAM-E后的情况下,病情缓解已超过5个月,这一期间并没有接受糖皮质激素或抗血管生成治疗。
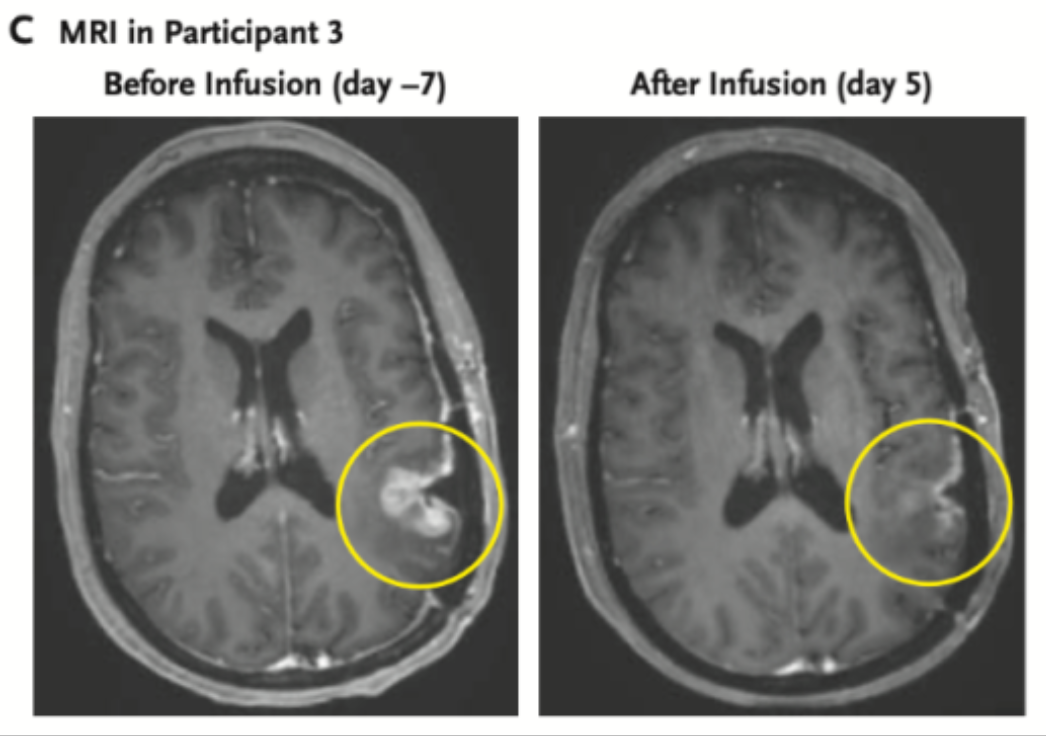
患者3在治疗5天后MRI显示:肿瘤几乎完全消退
患者3:57岁女性,她在单次输入CAR-TEAM细胞治疗5天后,肿瘤近乎完全消退。
作为一项1期试验,该疗法呈现出良好的安全性,3名患者均未出现3级以上不良事件或剂量限制性毒性。但是,患者1和患者3都在治疗后的几个月内复发了,且3名患者最终都出现了疾病进展,研究者考虑与输注后几周内CAR-TEAM细胞的有限持久性有关。
小结
上述两个最新研究,显示了CAR-细胞疗法在治疗脑肿瘤方面的潜力,虽然仍存在诸多挑战,但新的策略和解决方案正在不断被提出。
在实体瘤患者中,为改善CAR-T的浸润和转运难题,研究者提出了局部注射给药的方式,比如脑部、乳腺、胸膜、肝脏等,还具有降低脱靶效应带来的风险,减少毒副反应等优点。我们期待更多的结果出炉,加速CAR-T疗法各类实体瘤治疗领域的研发进程,让更多患者有药可用。
链接:http://www.lewenyixue.com/2024/03/29/5%e5%a4%a9%e8%82%bf%e7%98%a4%e5%87%a0%e4%b9%8e%e5%ae%8c%e5%85%a8%e6%b6%88%e5%a4%b1%ef%bc%9fcar-t%e7%96%97%e6%b3%95%e6%9c%ac%e6%9c%88%e5%a4%9a%e6%ac%a1%e7%99%bb%e4%b8%8anejm%e9%a1%b6%e5%88%8a%ef%bc%81/