Lancet Oncol 丨不良反应预测肿瘤患者生存预后?哈佛医学院团队近2.7万患者回顾分析
【CMT&CHTV 文献精粹】
导语: 哈佛医学院研究团队一项近2.7万患者的回顾性分析, 深入探讨了免疫检查点抑制剂(ICI)治疗中多器官免疫相关不良事件(irAEs)的共现模式及其对患者生存预后的影响。
研究背景
免疫检查点抑制剂(ICI)治疗是肿瘤免疫治疗的一大突破,其作用机制在于靶向阻断免疫细胞表面的关键免疫检查点蛋白,如 P D-1、 P D-L1和CTLA-4等,这些蛋白在正常情况下有助于调节免疫反应,防止对机体自身组织的攻击。肿瘤细胞经常利用这些免疫检查点通路来逃避免疫系统的攻击。ICI通过干预免疫抑制,恢复或增强T细胞对肿瘤细胞的识别和杀伤能力。
PD-1/ P D-L1抑制剂是当前研究和应用最广泛的ICI之一,通过阻断PD-1与其配体PD-L1之间的相互作用,解除了肿瘤细胞对T细胞的免疫抑制,更有效地攻击肿瘤细胞。CTLA-4抑制剂,作用于T细胞的早期激活,通过竞争性结合CTLA-4的配体CD80和CD86,增强免疫系统对肿瘤细胞的攻击。此外LAG-3抑制剂、TIM-3抑制剂也在积极探索中。新型ICI的加入,有望为肿瘤患者提供更多的治疗选择。
ICI在多种恶性肿瘤中展现出显著的疗效,但也可能引发一系列免疫相关的不良事件,影响多个器官/系统。既往研究多聚焦于单一器官的irAEs,对合并多器官irAEs及其对生存的影响认知有限。2024年7月, The Lancet Oncology 杂志发表了题为“Multi-organ Immune-related Adverse Events from Immune Check P oint Inhibitors and Their Downstream Im P lications: A Retospective Multicohort Study”一文,旨在进一步探索不同器官irAEs的发生规律及对患者的生存预后影响。

该研究是一项回顾性、多队列研究,纳入了2015年5月31日至2022年6月29日期间,美国麻省总医院、Brigham妇女医院和Dana-Farber癌症研究所接受ICI治疗的患者(简称MGBD队列);另一部分来自TriNetX医疗数据库,该数据库汇聚了全球数亿患者的数百亿份诊疗数据。
01
入组标准
研究纳入了来自MGBD队列的15 246名和TriNetX队列的50 503名接受免疫检查点抑制剂治疗的患者。通过倾向得分匹配,最终分别有13 086名和26 172名患者被纳入分析,研究排除了化疗后 3 个月内被诊断为疑似irAEs的患者。
02
研究结果
irAEs的共现现象
统计结果为,MGBD队列irAEs的发生率为37.7%(3 284名),TriNetX队列中irAEs的发生率为30.5%(5 538名)。
研究者聚类分析探索了内分泌、皮肤、呼吸、胃肠、肝脏、肌肉骨骼和神经系统的irAE,结果显示内分泌和皮肤irAEs是最常见的类型。MGBD、TriNetX队列内分泌irAEs的发生率分别为36%(1 196名)、37%(2 069名);皮肤irAEs的发生率分别为24%(787名)、25%(1 399名),详细数据见表1。
表1 各器官/系统irAEs的发生率

研究者观察到,不同器官/系统中的irAEs在两个队列中都普遍存在共现现象(co-occurrence Patterns)。在MGBD队列中,有817名患者出现内分泌系统的irAEs,与其他器官/系统的irAEs共现,其中269名(33%)也出现了皮肤的irAEs,267名(33%)出现了胃肠系统的irAEs,256名(31%)出现了肌肉骨骼系统的irAEs(图1.B)。TriNetX队列中也观察到了类似情况(图1.D)。
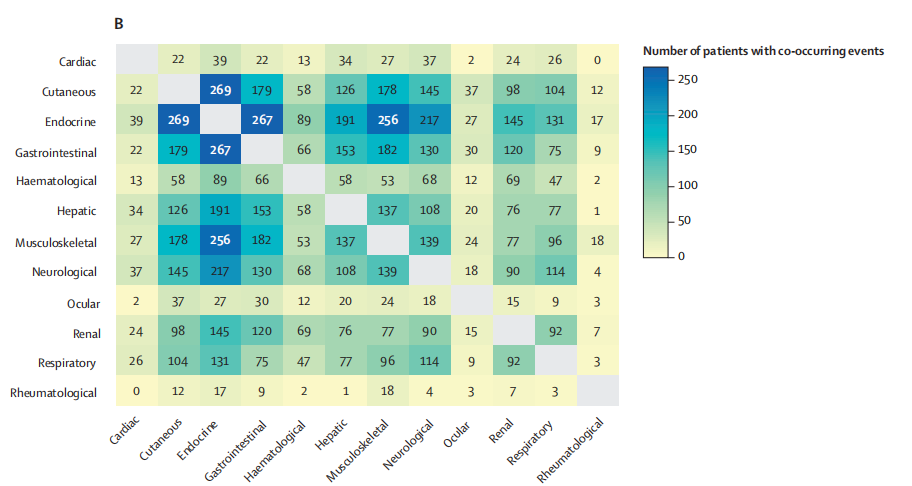

图2 不同器官/系统存在共现事件的患者数量(B.MGBD队列;D.TriNetX队列)
其次,两个队列中均观察到,在所有评估的器官/系统中,皮肤、内分泌、胃肠、肌肉骨骼和肾脏的irAEs共现现象较为显著。其中,眼睛的irAEs通常与皮肤、胃肠的irAEs共现,风湿病的irAEs通常与肌肉骨骼系统的irAEs共现(图2A,C)。


图2 不同器官/系统irAEs共现事件的相比风险比(A.MGBD队列;C.TriNetX队列)
研究者验证了不同器官/系统出现irAEs的风险与肿瘤种类的关联,如胸部肿瘤、泌尿生殖系统肿瘤、血液和淋巴系统恶性肿瘤、非黑色素瘤皮肤癌,以及大脑、神经或眼部的肿瘤,irAEs的发生往往与其肿瘤发生的器官/系统紧密相关。即肿瘤生长的部位在接受免疫治疗时,irAEs的发生风险增加。其中, 黑色素瘤除了皮肤,还同时存在多器官/系统的irAEs发生风险增加, 提示黑色素的免疫治疗方案需更加注重irAEs的监测与管理。
irAEs与生存预后显著相关
研究涵盖了MGBD队列和TriNetX队列中分别有13 086名和26 172名患者被纳入倾向得分匹配队列。经过中位317天和249天的随访,两个队列中普遍观察到irAEs的发生存在显著的共现现象,根据不同患者以特定器官/系统的irAEs为主,研究团队划分七个具有不同irAEs特征的患者群体:内分泌型、皮肤型、呼吸型、胃肠型、肝脏型、肌肉骨骼型和神经型。
在MGBD队列中,以 内分泌 型( HR= 0.53,95% CI:0.40~0.70 ,P<0.0001,)和皮肤型( HR= 0.61 ,95% CI:0.46~0.81 ,P=0.000 7)irAEs为主的患者群体,6个月(6-month landmark timepoint)观察到具有更好的 生存结局 。 相比之下, 呼吸型( HR= 1.60 ,95% CI:1.25~2.03 ,P=0.0001)的患者群体的生存结局则相对较差 , 胃肠型、肌肉骨骼型、肝脏型和神经型则无特殊性。
在TriNetX队列中,内分泌型( HR = 0.75 , 95% CI :0.60~0.93 ,P =0.0078)和皮肤型( HR = 0.62 , 95% CI :0.48~0.82 ,P =0.0007)、呼吸型( HR = 1.21 , 95% CI :1.00~1.46 ,P =0.044)的患者群体的生存结局与MGBD队列类似。但TriNetX队列中的神经型患者群体的生存结局则较差( HR = 1.30 , 95% CI :1.06~1.59 ,P =0.013)。
该发现强调了不同器官/系统irAEs对患者生存预后的影响(表2,图3),提示在临床实践中对特定irAEs群体进行个性化管理的必要性。
表2 不同系统类型的irAEs患者群的 生存结局 分析(6-month landmark timepoint)

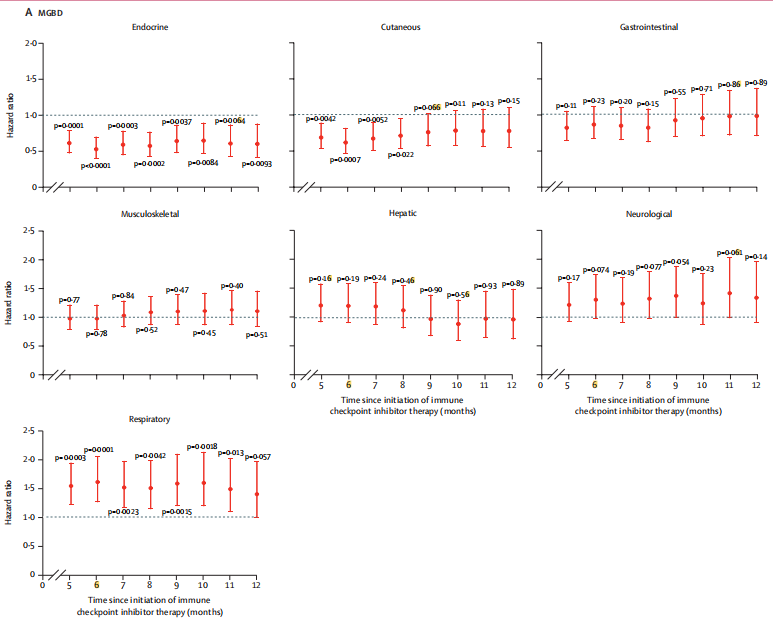

图3 MGBD(A)和TriNetX(B)队列中不同系统类型的irAEs患者群的 生存结局 (6-month landmark timepoint)
irAEs与系统性免疫抑制治疗的联系
系统性免疫抑制治疗通常会用于irAEs的管理,但同时免疫制剂会减弱免疫治疗的抗肿瘤活性,影响治疗疗效。研究者们试图调查系统性免疫抑制治疗使用上的差异在多大程度上解释了研究中观察到的总体生存结果。通过复查MGBD队列中1 049名患者的病历,提取系统性免疫抑制治疗的开始日期、状态、剂量以及接受治疗的理由。
研究者建立了一种计算方法来识别患者中最常用的系统性免疫抑制--系统性糖皮质激素的使用情况,发现其在不同类型irAEs患者群中的使用率差异显著。从内分泌型的21%到胃肠型的66%,研究者推测 系统性免疫抑制治疗的使用可能与 irAEs的类型和严重程度有关。
大多数irAE在治疗开始后的6个月内发生,且研究中大多数irAEs为2级及更高级别(如MGBD队列中,通过手动病历复查的100名患者中有84.5%的事件是2级或更高级别的irAEs),但其对生存结果的影响仍需进一步研究。
03
总结讨论
该研究强调了识别irAEs共现模式在临床治疗中的重要意义。对于表现内分泌型和皮肤型irAEs的患者,从ICI治疗中获益的可能性更高,需要更为积极地监测和管理。相反,对于呼吸型和神经型irAEs的患者,则需要更为谨慎的治疗策略,以避免不必要的治疗风险。此外,研究还指出,系统性免疫抑制治疗的使用与生存结果之间存在关联,提示临床治疗中需要更细致地考虑其应用的时机和剂量。
参考文献
GUIHONG WAN, WENXIN CHEN, SARA KHATTAB, et al. Multi-organ immune-related adverse events from immune checkpoint inhibitors and their downstream implications: a retrospective multicohort study[J/OL]. THE LANCET Oncology, 2024. [2024-7-15]. https://pubmed.ncbi.nlm.nih.gov/35924238. DOI:org/10.1016/S1470-2045(24)00278-X
链接:http://www.lewenyixue.com/2024/08/28/Lancet%20Oncol%20%E4%B8%A8%E4%B8%8D%E8%89%AF%E5%8F%8D%E5%BA%94%E9%A2%84%E6%B5%8B/