Nat Med 丨可切除食管/胃食管交界处癌:新辅助免疫疗法新突破!
【CMT&CHTV 文献精粹】
导语: 食管癌和胃食管交界癌(E/GEJ)的临床管理在过去几十年中进展有限,大多数患者在确诊后5年内经历疾病进展和死亡。尽管新辅助放化疗(CRT)后完全切除的食管/胃食管交界癌患者中,美国食品药品管理局(FDA)批准了纳武利尤单抗作为辅助治疗,但对于可切除的E/GEJ癌患者,新辅助PD-1途径抑制剂与CRT的结合使用,以及其与病理反应、循环肿瘤DNA(ctDNA)动态和系统性新抗原特异性T细胞反应之间的关系尚未充分明确。2024年4月,《 Nature Medicine 》杂志发表了题为《Neoadjuvant nivolumab or nivolumab plus LAG-3 inhibitor relatlimab in resectable esophageal/gastroesophageal junction cancer: a phase Ib trial and ctDNA analyses》一文提供了新的参考。

研究方法
本研究是一项开放标签、多中心的Ib期临床试验,旨在评估新辅助纳武利尤单抗(Arm A,n=16)或纳武利尤单抗联合Relatlimab(Arm B,n=16)与CRT相结合治疗32名可切除II/III期胃食管癌患者的安全性和可行性,并深入评估病理、分子和功能性免疫反应。研究的主要终点是安全性;次要终点是可行性;探索性终点包括病理完全(pCR)和主要病理反应(MPR)、无复发生存期(RFS)和总生存期(OS)。
研究结果
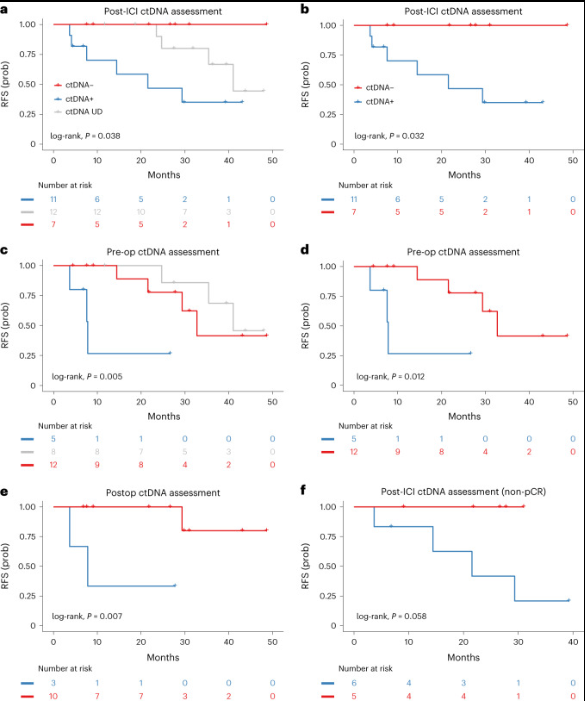
Arm A达到了主要的安全终点,而Arm B需要修改以减轻毒性。pCR和MPR率分别为Arm A的40%和53.5%,Arm B的21.4%和57.1%。最常见的不良事件包括疲劳、恶心、血小板减少和皮炎。总体,2年RFS和OS率分别为72.5%和82.6%。基线PD-L1和LAG-3表达水平更高的患者与更深的病理反应相关。循环肿瘤DNA(ctDNA)的探索性分析显示,在接受免疫检查点抑制剂(ICI)诱导、术前和术后无法检测到ctDNA的患者中,RFS和OS显著更长;ctDNA清除反映了新抗原特异性T细胞反应。
安全性与可行性
本研究在Arm A中成功达到了主要的安全终点,证实了新辅助纳武利尤单抗联合放化疗的安全性。然而,Arm B在治疗初期就遭遇了挑战,由于不可接受的毒性,包括心包炎和肾上腺功能不足,研究方案不得不进行修改。这一调整对于后续患者的安全性至关重要,也提示了在免疫治疗中对潜在毒性的严格监控和管理的必要性。
病理反应
在病理反应方面,Arm A和Arm B的病理完全缓解(pCR)率分别为40%和21.4%,而主要病理缓解(MPR)率则分别为53.5%和57.1%。这些数据表明,尽管Arm B因毒性问题进行了调整,但其病理缓解率并未显著低于Arm A,这可能表明即使在减量的情况下,联合LAG-3抑制剂仍能发挥一定的疗效。
生存期分析
在生存期分析中,2年无复发生存率(RFS)和总生存率(OS)分别为72.5%和82.6%。这一结果令人鼓舞,因为它不仅反映了治疗的有效性,也显示了患者在接受治疗后的长期生存获益。
基线生物标志物表达
研究还发现,基线时PD-L1和LAG-3的表达水平与病理反应的深度相关。特别是,PD-L1表达水平较高的患者(CPS ≥5)在无复发生存期(RFS)上有显著延长的趋势,这为未来可能的生物标志物驱动的治疗策略提供了依据。
ctDNA动态与临床结果的关联
ctDNA的动态变化与肿瘤的分子水平退缩紧密相关。研究中,治疗后无法检测到ctDNA的患者,其复发后生存期(RFS)和总生存期(OS)显著更长。这一发现表明,ctDNA不仅可以作为治疗反应的早期指标,也可能预测长期临床结果。
新抗原特异性T细胞反应
最后,研究通过MANAFEST分析法观察到,与ctDNA清除相一致,系统性肿瘤负担收缩与新抗原特异性T细胞的检测和扩张相关。这进一步支持了ctDNA分析在捕捉功能性抗肿瘤免疫反应中的价值,并可能指导未来新辅助研究的设计。
总结讨论
相较于其他研究,本研究的独特价值在于它不仅评估了新辅助纳武利尤单抗或纳武利尤单抗加Relatlimab与CRT相结合治疗的安全性和可行性,而且还深入探讨了ctDNA动态和系统性新抗原特异性T细胞反应,为个体化治疗提供了潜在的生物标志物。此外,研究结果强调了在新辅助治疗期间监测系统性肿瘤负担的重要性,这可能有助于临床决策,以最大化治疗效益。
参考文献:
Kelly RJ, Landon BV, Zaidi AH, et al. Neoadjuvant nivolumab or nivolumab plus LAG-3 inhibitor relatlimab in resectable esophageal/gastroesophageal junction cancer: a phase Ib trial and ctDNA analyses [J]. Nat Med. 2024;30(4):1023-1034. doi:10.1038/s41591-024-02877-z
链接:http://www.lewenyixue.com/2024/07/10/Nat%20Med%20%E4%B8%A8%E5%8F%AF%E5%88%87%E9%99%A4%E9%A3%9F%E7%AE%A1-%E8%83%83%E9%A3%9F%E7%AE%A1%E4%BA%A4%E7%95%8C/