J Hepatol 吉林大学樊钟琦团队发现顺铂诱导的线粒体分裂体的破坏导致胆管癌对顺铂的耐药性增强!

胆管癌(CCA)是一种胆管上皮的恶性肿瘤,全球发病率和死亡率不断上升,5年生存率为106 7%–20%。在诊断中,不到25%的患者符合治疗性切除的条件。对于晚期CCA,顺铂(CDDP)联合吉西他滨(CisGem),有或没有PD-1抑制剂durvalumab,代表标准一线姑息治疗。然而,由于CCA7的“冷”免疫肿瘤微环境(TME ),免疫检查点抑制剂单一疗法在未选择的患者中显示出有限的疗效。 有趣的是,CDDP可以将TME从“冷”改造为“热”,正在进行的试验正在探索CisGem与其他药物的组合。因此,克服CDDP阻力仍然至关重要。
虽然大多数关于耐药性的研究都集中在静态变化上,但是对药物暴露的适应性变化可能会提供更多的临床相关性见解。线粒体凋亡途径在CDDP-诱导的细胞毒性中起着重要作用,线粒体在压力下经历动态形态重塑。 以前的研究表明,CDDP在CDDP耐药CCA细胞中诱导线粒体融合,而线粒体分裂在ABT737存在下使它们对CDDP敏感,暗示线粒体融合是CDDP耐药的关键驱动因素。
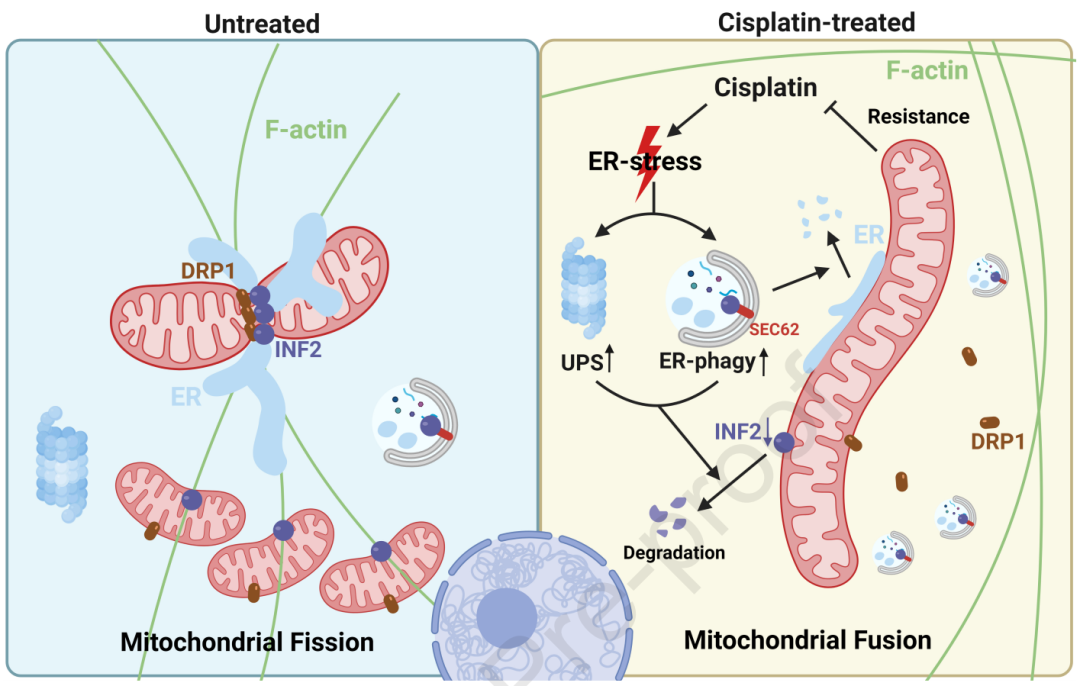
线粒体分裂体(MD)是一个控制线粒体分裂的多组分系统,以动力蛋白相关蛋白1 (DRP1)及其外膜受体为核心成分。DRP1介导的分裂由细胞骨架元件、内质网(ER)和肌动蛋白-结合蛋白如倒置的formin-2 (INF2)支持,它们协调细胞器间接触位点。 有趣的是,CDDP不仅形成DNA加合物,而且还破坏细胞骨架细丝,潜在地改变MD以促进fusion介导的抗性。
该研究确定了基线的高INF2表达与胆管癌(CCA)患者的不良预后相关。此外,顺铂诱导的INF2降解通过蛋白酶体和SEC62介导的ER吞噬被揭示为CCA中线粒体超融合和化疗耐药的关键驱动因素。它建立了线粒体形态靶向作为克服化疗耐药性的新策略。 此外,这项研究强调需要关注治疗期间肿瘤蛋白或细胞器功能的动态变化(功能性精确肿瘤学),而不是将分析局限于静态肿瘤状态。 项工作为针对CCA和其他具有类似耐药机制的恶性肿瘤的线粒体-靶向方法提供了基础。

— END —
链接:http://www.lewenyixue.com/2025/04/08/J%20Hepatol%20%E5%90%89%E6%9E%97%E5%A4%A7%E5%AD%A6%E6%A8%8A%E9%92%9F%E7%90%A6%E5%9B%A2%E9%98%9F%E5%8F%91/





赶快来坐沙发