Nat Commun丨李莹/唐本忠/李国新团队合作为靶向结肠癌治疗设计多功能诊断剂铺平了一条途径

恶性肿瘤对人类健康构成严重威胁,是全球死亡的主要原因之一。 手术、化疗和放疗等传统方式经常受到与疗效、副作用和患者预后不良相关的挑战的阻碍,这加剧了对更有效癌症疗法的需求。光疗是一种非侵入性方法,对健康组织的影响最小,仅针对受照射区域,从而符合精准医学的原则。近年来,光动力疗法(PDT)和光热疗法(PTT)因其克服与传统疗法相关的许多限制的潜力而受到广泛关注。这种药物不仅可以简化治疗过程,还可以通过诱导免疫原性细胞死亡(ICD)来增强疗效和刺激免疫反应。ICD通过促进树突状细胞(DCs)的成熟和T细胞的活化,显著增强T细胞介导的抗肿瘤免疫。光敏剂(PSs)具有在癌细胞内诱导氧化应激的潜能,从而触发ICD。ICD诱导的免疫应答的效力与活性氧(ROS)的产生有着错综复杂的联系。然而,不同成分的组合固有的复杂性使协同治疗过程变得复杂和持久,可能增加体内毒性副作用。在这种情况下,迫切需要开发能够在单一激发波长下协调PDT和PTT的多功能单组分治疗药物。
聚集诱导发射(AIE)已成为生物光子学领域的一个开创性概念,尤其是在癌症治疗学中 。AIE发光体(AIEgens)表现出独特的特征可最大限度地减少分子间相互作用和分子迁移率。这些代理通过精心设计,能够整合PDT和PTT的双重角色。此外,AIEgens还提供多模态成像功能,这些成像技术为肿瘤生物学和微环境提供了互补的观点,并有助于准确的肿瘤检测和治疗反应监测。综上所述,AIEgens可以在多模态成像引导下利用PDT和PTT的协同效应实现高效的ICD,使它们成为肿瘤治疗的重要工具。尽管AIEgens具有增强荧光和光稳定性等强大特性,但酸性、低氧和异常血管肿瘤微环境会阻碍药物递送,导致肿瘤内出现治疗耐药性和免疫抑制。此外,全身给药的AIEgens缺乏肿瘤细胞特异性,可能对健康组织构成毒性风险。因此,提高AIEgens的肿瘤靶向能力和疗效是一个有待解决的重大挑战。
近年来,生物载体在肿瘤治疗中引起了相当大的关注,因为它们能够自然靶向并在肿瘤组织内蓄积。其中,细菌介导的癌症治疗是一种非常有前途的生物治疗策略。 某些细菌属表现出靶向肿瘤的天然倾向,选择性地在肿瘤组织内积累。大肠杆菌Nissle1917(EcN)以其抗菌特性、肠道微生物群调节和兼性厌氧性质而闻名。作为Mutaflor®药物的基石,它已被用于治疗炎症性肠病和胃肠道肿瘤。然而,细菌治疗受到剂量依赖性毒性和需要仔细控制剂量的阻碍,这可能会损害治疗效果。因此,仅依靠细菌抑制肿瘤往往无法达到预期的治疗效果。因此,将AIEgens与细菌相结合提供了一种有前途的解决方案,通过增强肿瘤靶向和实现治疗剂的受控释放,最终提高癌症治疗的疗效,同时最大限度地减少副作用。
在这项工作中提出了一种创新概念,即“AIEgen细菌混合仿生机器人”(EcN@INX-2),它将AIEgen与EcN集成在一起,以实现多模式光疗效果 。通过策略性调控AIEgen的分子结构,研究成功合成了INX-PF6−(INX-2),表现出AIE特性、NIR吸收、NIR-II发射、卓越的光热和光声特性。此外,EcN@INX-2将这些独特特性与EcN的肿瘤靶向能力相结合。静脉给药后,由于EcN的天然缺氧靶向能力,杂交仿生机器人优先定位于肿瘤组织内。体内多模态成像有助于以高灵敏度区分肿瘤和正常组织,从而实现肿瘤治疗的精确靶向。通过PDT光诱导的ROS生成进一步促进了肿瘤细胞中的ICD,增强了抗肿瘤免疫反应。 这项研究将机器人技术与生物系统无缝集成,为EcN细菌注入光疗诊断学AIEgen特性,以制造完全运动的生物混合微型机器人。它强调了通过部署光疗诊断AIEgen来增强细菌介导的抗肿瘤免疫疗法的潜力。
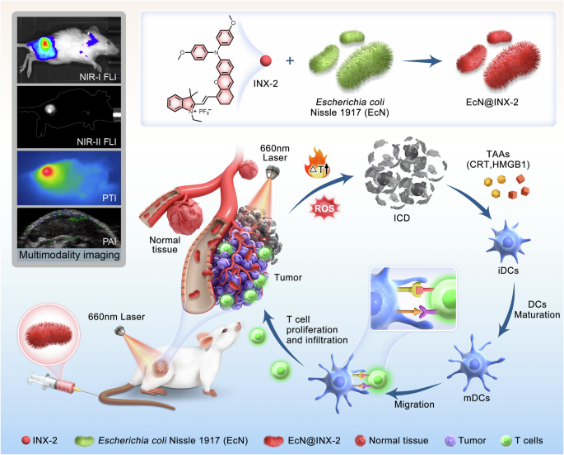
图1 AIEgen细菌混合仿生机器人EcN@INX-2的示意图(摘自 Nature Communications )
参考消息:
https://doi.org/10.1038/s41467-025-57533-y

— END —
链接:http://www.lewenyixue.com/2025/04/07/Nat%20Commun%E4%B8%A8%E6%9D%8E%E8%8E%B9-%E5%94%90%E6%9C%AC%E5%BF%A0-%E6%9D%8E%E5%9B%BD/




 知道|国家药品不良反应监测年度报告(2024年)
知道|国家药品不良反应监测年度报告(2024年)
赶快来坐沙发