前沿分享 | Nature:癌症免疫治疗新突破,阻断GDF-15攻克实体瘤耐药难题
引言
近年来,癌症免疫治疗取得了重大突破,PD-1/PD-L1抑制剂已成为多种肿瘤的标准治疗方案。然而,治疗耐药性仍然是一个关键挑战。在 Nature 上发表的“ Neutralizing GDF-15 can overcome anti-PD-1 and anti-PD-L1 resistance in solid tumours ”表明,生长分化因子15( GDF-15 )可能是导致耐药的关键因素,而靶向中和GDF-15可以增强PD-1/PD-L1治疗的疗效,这为攻克免疫耐药提供了新的思路。
研究背景
PD-1/PD-L1抑制剂通过解除T细胞的“刹车”功能,使其能够更有效地攻击肿瘤。然而,并非所有患者都对该治疗产生反应,且许多患者在一段时间后会出现耐药性,导致肿瘤复发或进展。
科学家们发现,GDF-15是一种肿瘤微环境中的免疫抑制因子,它可以减少肿瘤组织中的T细胞浸润,抑制T细胞功能,最终降低免疫治疗的效果。因此,研究人员提出:如果能够抑制GDF-15,是否能让PD-1/PD-L1治疗重新生效?
研究数据和特征
1.患者数据
研究聚焦对之前抗PD-1或抗PD-L1治疗耐药的晚期患者,重点关注非小细胞肺癌和尿路上皮癌患者。非小细胞肺癌队列27例患者中,男性20例、女性7例,非鳞状细胞癌占77.8%。尿路上皮癌队列27例可评估患者,之前治疗中位线数为3。
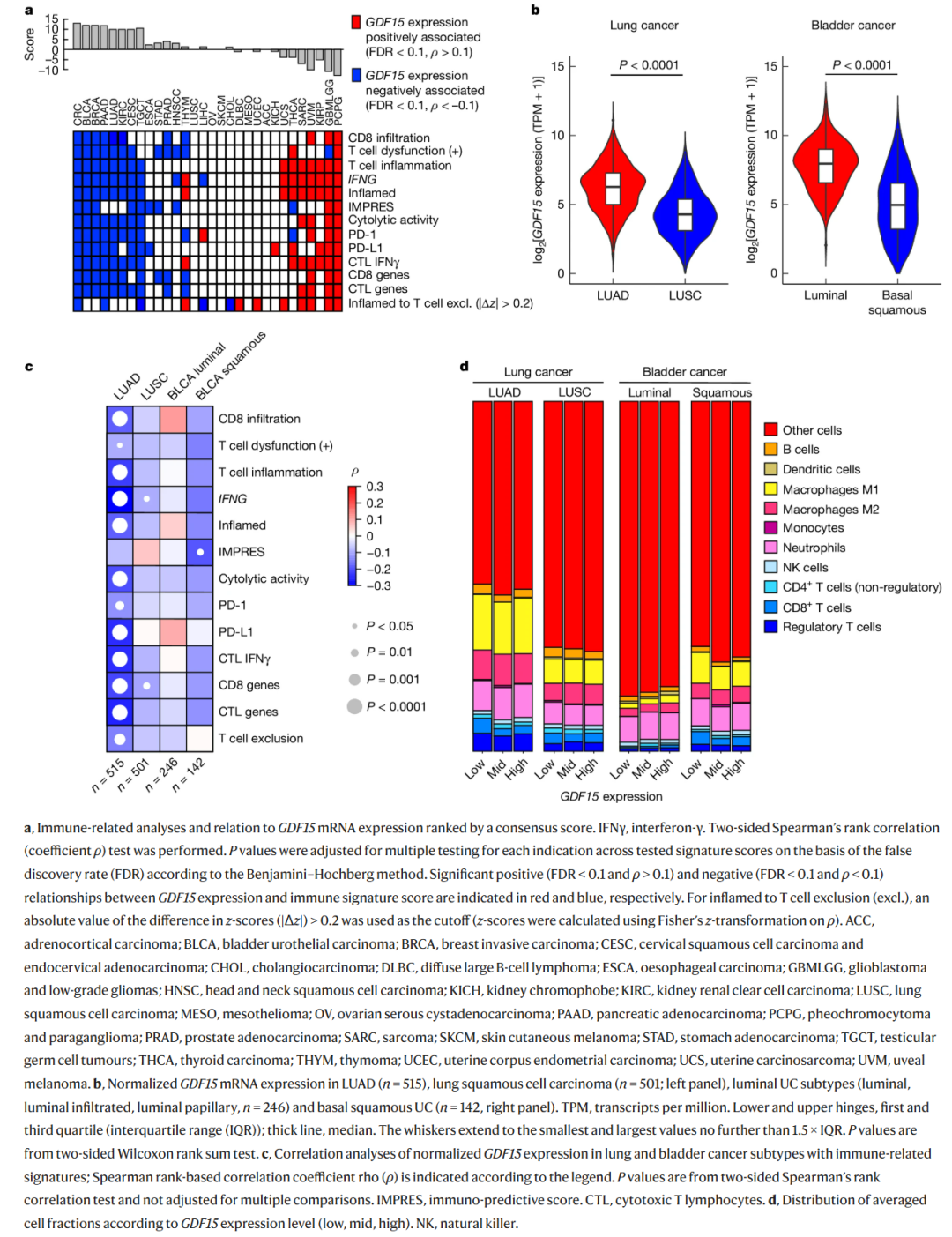
分析约10000例肿瘤样本(33种癌症类型)数据发现,GDF15在多种实体瘤高表达。在肺腺癌、基底鳞状尿路上皮癌中,GDF15 mRNA表达与T细胞转录组特征呈负相关,即GDF15高表达时,CD8+T细胞数量减少(见 图1)。
研究方法
临床试验: 开展GDFATHER-1/2a临床试验。1期采用“3+3”剂量递增设计,25例晚期转移性混合实体瘤患者接受5种剂量的visugromab(中和性抗GDF-15抗体)与nivolumab(抗PD-1抗体)联合治疗,前3位患者先单药治疗1周期,评估安全性和耐受性。2a期针对非小细胞肺癌和尿路上皮癌,依药代动力学和药效学建模,确定10 mg/kg visugromab每两周一次联合标准剂量nivolumab为2期推荐方案,探索抗肿瘤活性。
实验室检测:治疗中多次对患者肿瘤进行活检。用免疫组化分析T细胞变化,RNA测序检测基因表达,ELISA试剂盒检测血清趋化因子浓度,探究GDF-15阻断对免疫的影响。
结果与讨论
1.安全性和耐受性良好:
部分患者治疗效果好。非小细胞肺癌队列客观缓解率为14.8%(非鳞状亚组19.0%),尿路上皮癌队列客观缓解率为18.5%。部分患者缓解持续时间长,非小细胞肺癌患者均值为15.3个月、中位值为16.6个月,3例仍在缓解;尿路上皮癌患者均值为16.4个月、中位值为14.4个月,1例完全缓解超20个月。
阻断GDF-15后,肿瘤组织多种T细胞数量增加,如CD4+FOXP3-T细胞、CD8+T细胞等(见 图2 )。这增强了免疫细胞浸润和活化,提升免疫治疗效果。
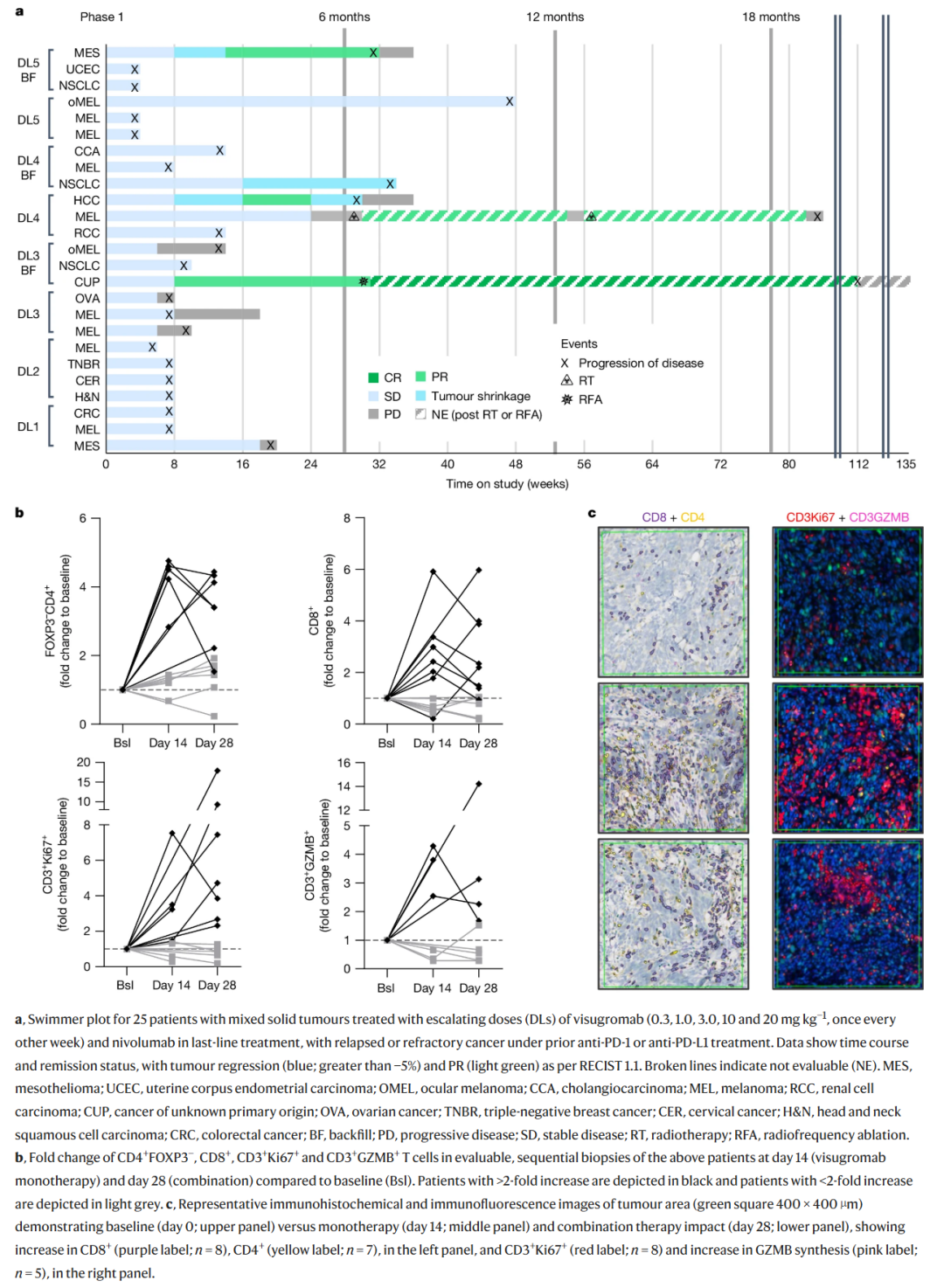
图2 visugromab联合nivolumab的1期剂量递增试验
4.免疫相关基因和信号通路激活
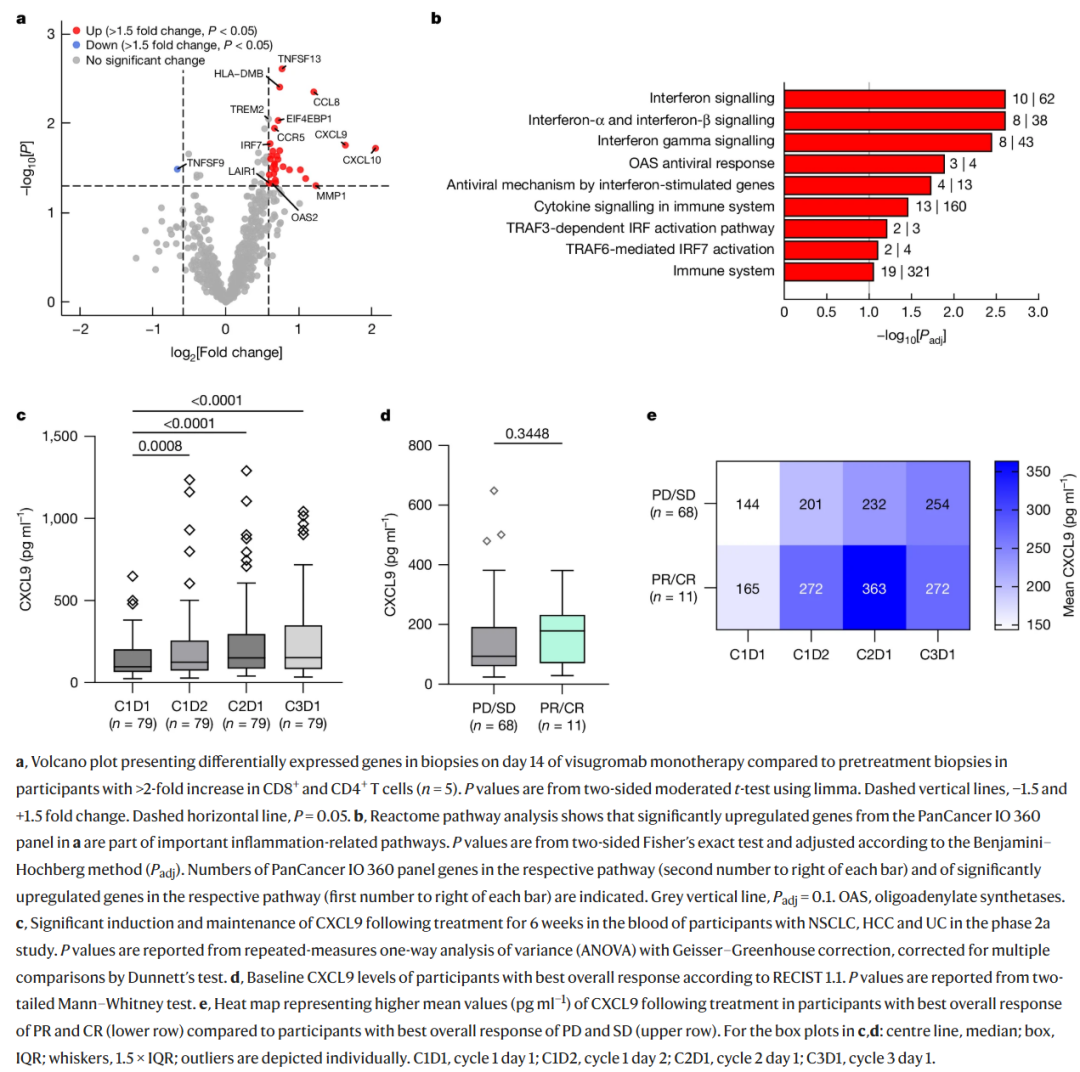
visugromab单药治疗14天后,肿瘤组织炎症基因及相关通路被激活,血清中趋化因子CXCL9和CXCL10水平上升。缓解患者治疗期间这两种趋化因子暴露量更高,进一步证实联合治疗能增强免疫反应。结果见 图3 。
图3 部分抗PD-1和PD-L1治疗复发或难治的晚期癌症患者中干扰素-γ信号通路的诱导情况
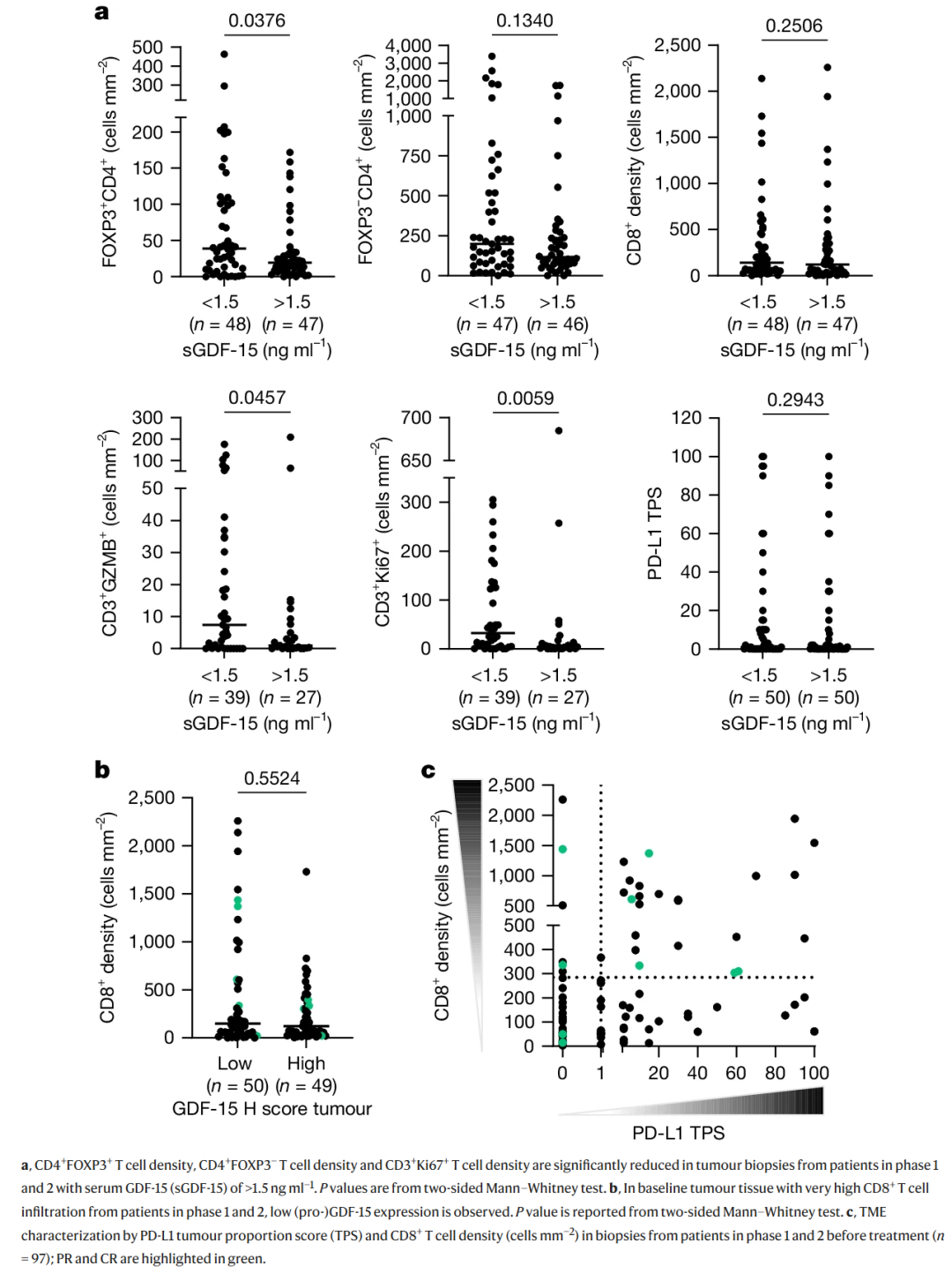
基线血清GDF-15水平大于1.5 ng/ml时,肿瘤内多种免疫细胞密度降低。且CD8+T细胞浸润高的肿瘤组织,GDF-15表达低,说明GDF-15抑制免疫细胞功能,促进肿瘤免疫逃逸。结果见 图4。
研究亮点
1.发现新的耐药靶点
2.联合治疗效果显著
3.揭示免疫调节机制
4.潜在的临床应用价值
文献来源
Melero, I., de Miguel Luken, M., de Velasco, G. et al. Neutralizing GDF-15 can overcome anti-PD-1 and anti-PD-L1 resistance in solid tumours. Nature637, 1218–1227 (2025). https://doi.org/10.1038/s41586-024-08305-z
原文链接
https://www.nature.com/articles/s41586-024-08305-z
分享者简介
重庆大学智能肿瘤学教育部医药基础 研究创新中心2024级基础医学硕士
编辑|曾海蓉
审核 | 李 劲
链接:http://www.lewenyixue.com/2025/04/02/%E5%89%8D%E6%B2%BF%E5%88%86%E4%BA%AB%20%7C%20Nature%EF%BC%9A%E7%99%8C%E7%97%87%E5%85%8D%E7%96%AB%E6%B2%BB%E7%96%97/







赶快来坐沙发