Nature子刊重磅!癌症晚期患者多吃这些食物,能让免疫治疗效果更好!
为何有些患者对免疫治疗治疗无响应?这一临床难题背后隐藏着怎样的机制?或许,答案就藏在我们日常饮食中那些习以为常的饮食中。最近一项研究发现,饮食中的一些物质可重塑肠道微生物群,进而影响免疫治疗效果。
01▼饮食如何重塑肠道微生物群以增强免疫治疗效果?
免疫检查点抑制剂如抗PD-L1抗体已成为多种晚期癌症的标准治疗方案,然而在临床应用中存在显著的个体差异。部分患者对治疗无响应,导致治疗效果受限。研究表明,肿瘤微环境中的免疫抑制机制,如PD-L1的高表达,是导致免疫治疗耐药的关键因素之一。此外,肿瘤细胞通过上调PD-L1表达,逃避宿主免疫系统的识别和攻击,从而减少肿瘤浸润性淋巴细胞的活性。尽管免疫治疗在某些患者中取得了显著的疗效,但仍需提高治疗的响应率和持久性。
近年来,肠道微生物群对免疫治疗效果的影响已逐渐被认识。现有研究多集中于单一因素对肠道微生物群的影响,而忽略了生活及饮食过程中多种因素的综合作用,如植物源性纳米颗粒(PNP)。PNP富含于很多常见食物中,如生姜、大蒜、芦荟、柠檬、葡萄柚、菠菜、西兰花、杏仁、亚麻籽、姜黄、迷迭香、绿茶和蓝莓等,作为一种天然的纳米载体,能够携带多种生物活性分子,如脂质、蛋白质和小RNA,这些分子可能通过调节肠道微生物群的代谢产物,进而影响宿主的免疫反应。然而,PNP如何通过选择性地被特定肠道细菌摄取,并调节其代谢产物以增强免疫治疗效果,目前仍缺乏分子机制的研究。
2025年2月,Nature Communications杂志发表了一篇题为“Plant-nanoparticles enhance anti-PD-L1 efficacy by shaping human commensal microbiota metabolites”的研究,聚焦于植物源性纳米颗粒(PNP)对肠道微生物群及其代谢产物的影响,并探索其在增强抗PD-L1免疫治疗中的潜在机制。研究提出,生姜来源的外泌体样纳米颗粒(GELN)能够增加多不饱和脂肪酸(如DHA)的积累,而DHA水平的升高能够结合PD-L1启动子,抑制肿瘤细胞中PD-L1的表达,从而增强抗PD-L1免疫治疗的效果。
02▼多组学研究:探索植物纳米颗粒对肠道微生物群及免疫治疗的影响
本研究是一项多组学研究,旨在探索植物源性纳米颗粒(PNP)对肠道微生物群及其代谢产物的影响,并进一步研究其在增强抗PD-L1免疫治疗中的潜在机制。研究纳入了健康志愿者的粪便样本,分离并培养其中的肠道细菌,并将其移植到无菌(GF)C57BL/6J小鼠中,构建了人类化肠道微生物群的小鼠模型。按接受不同植物源性纳米颗粒(如生姜、大蒜、芦荟和柠檬)处理的组别进行分组,并设置对照组。
主要评价指标为肠道微生物群的组成变化、代谢产物的差异以及抗PD-L1免疫治疗的疗效,次要评价指标包括肿瘤生长抑制率、生存率等。通过16S rRNA测序分析肠道微生物群的组成,利用2D-LC-MS/MS技术检测代谢产物的变化,并结合流式细胞术等方法评估免疫治疗效果。
03▼植物纳米颗粒重塑肠道微生物群代谢产物,显著增强抗PD-L1免疫治疗效果
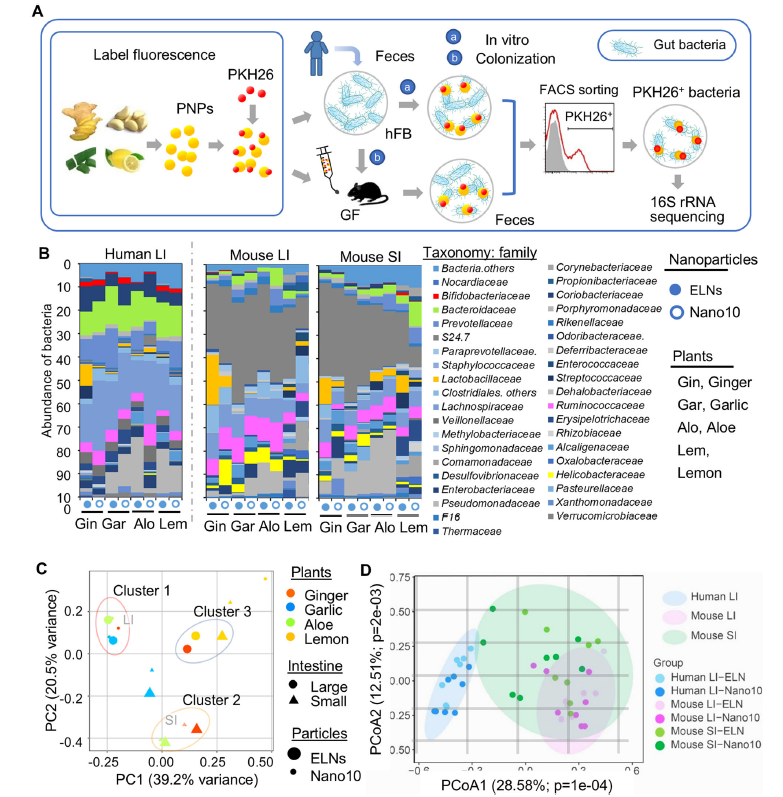
植物纳米颗粒被特定肠道细菌摄取,调节微生物群组成研究发现,生姜来源的GELN能够被特定肠道细菌家族优先摄取,其中Lachnospiraceae和Lactobacillaceae表现出显著的摄取偏好。通过16S rRNA测序分析,研究者发现GELN处理的小鼠GF小鼠中,肠道微生物群的组成发生了显著变化,Lachnospiraceae和Lactobacillaceae的相对丰度显著增加(分别为21.48%±5.38%和13.01%±2.40%),而其他细菌家族如Ruminococcaceae的丰度则相对较低(4.92%±2.01%)。这表明,GELN能够通过特定的脂质和氨基酸信号,选择性地被这些细菌摄取,从而调节肠道微生物群的组成。
注:A. PNP处理、用PKH26荧光标记以及给小鼠定植人类粪便细菌;B. 从健康受试者收集的粪便细菌汇集在一起,并与PKH26标记的PNP在厌氧室孵育2小时(标记为“人类LI”);C. C 不同来源和不同类型的PNP的主成分分析(PCA);D. 根据属分类水平的Bray-Curtis差异,对人类LI、hFB小鼠LI和SI的个体PNP-PKH26+肠道微生物群组成进行主坐标分析(PCoA)测试。图1 PNP被人类肠道细菌摄取
GELN通过抑制细菌PLC表达增加DHA积累
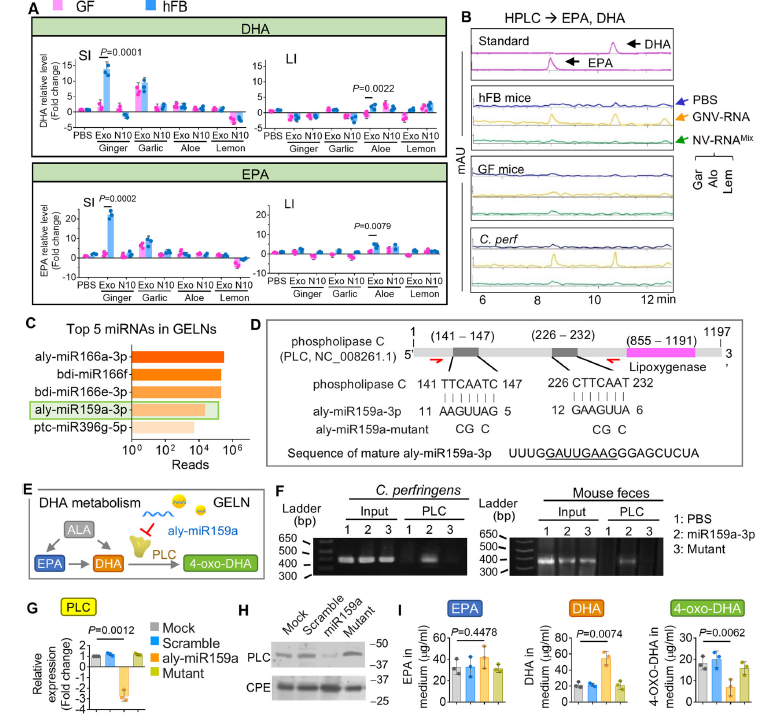
GELN中的aly-miR159a-3p通过靶向细菌磷脂酶C(PLC)基因,抑制其表达,进而影响DHA的代谢。PLC是DHA代谢的关键酶,能够将DHA转化为4-氧代-DHA。研究通过体外实验和基因敲除实验验证了这一机制。在体外实验中,GELN处理的肠道细菌培养液中DHA水平显著增加(P=0.0074),而PLC基因敲除的细菌中DHA水平进一步升高(P=0.003 4),4-氧代-DHA水平则显著降低(图2)。这表明PLC在DHA代谢中的关键作用,GELN通过抑制PLC的表达,导致DHA在肠道细菌中积累。
注:A. HPLC分析GF和hFB小鼠的LI和SI中DHA和EPA的相对水平;B. HPLC分析GF和hFB小鼠的粪便以及Clostridium perfringens(C.perf)培养基中的DHA和EPA水平;C. GELN中高丰度的miRNA序列;D. GELN miRNA aly-miR159a-3p潜在靶向PLC的示意图;E. DHA代谢途径的示意图;F. ChIP分析aly-miR159a-3p与PLC基因的相互作用;G. 使用qPCR分析C.perf中PLC基因的表达;H. Western blot分析PLC蛋白的表达;I. HPLC分析C.perf中EPA(左图)、DHA(中图)和4-氧代-DHA(右图)的水平。图2 GELN富含的aly-miR159a-3p通过靶向PLC调节细菌中的DHA代谢
GELN显著增强抗PD-L1免疫治疗效果,抑制肿瘤生长和转移
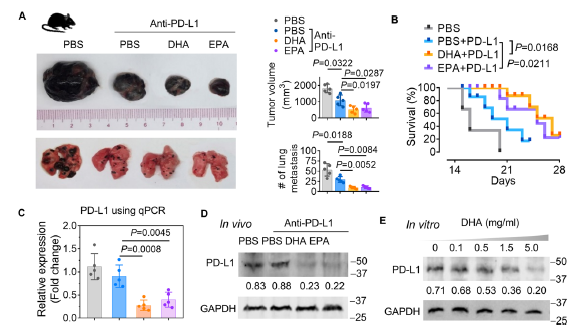
在小鼠模型中,GELN处理的小鼠表现出显著的肿瘤生长抑制和肺转移减少。与对照组相比,GELN处理的小鼠肿瘤体积显著减小(P=0.038 6),肺转移结节数量显著减少(P=0.005 5)。生存率也显著提高(P=0.033)。此外,GELN处理的小鼠肿瘤组织中PD-L1的表达水平显著降低(P=0.000 7),进一步证实了DHA在抑制PD-L1表达中的作用。研究还发现,GELN处理的小鼠肿瘤组织中PD-L1的mRNA水平也显著降低(P=0.001 6,图3),表明DHA通过转录水平抑制PD-L1的表达。
注:A. 肿瘤负荷的hFB小鼠代表性B16F10黑色素瘤原发肿瘤(左上图)和肺部(左下图)图像;B. 图A中小鼠的生存率;C. 使用qPCR分析B16F10黑色素瘤异种移植小鼠肿瘤中PD-L1的表达;D. 代表性免疫印迹分析B16F10黑色素瘤异种移植小鼠肿瘤中PD-L1的表达;E. Western blot分析经DHA(0–5.0 mg/ml)处理2小时的B16F10细胞中PD-L1的表达。图3 DHA通过抑制PD-L1表达改善抗PD-L1免疫疗法对黑色素瘤的疗效
DHA水平与免疫治疗响应相关,临床样本分析揭示潜在机制
在临床样本分析中,研究发现PD-L1表达水平较高的肿瘤组织中,DHA水平较低,且与免疫治疗无响应的患者相关。对61例黑色素瘤患者的肿瘤组织进行分析,发现PD-L1表达水平在免疫治疗无响应的患者中显著更高(P=0.0007),而DHA水平则显著更低(P=0.002 5)。此外,肠道微生物群中PLC表达水平在免疫治疗无响应的患者中也更高(P=0.000 6),表明PLC活性的增加可能加速DHA的代谢,从而促进PD-L1的表达,导致免疫治疗效果不佳。
GELN通过调节免疫细胞功能,增强抗肿瘤免疫反应
研究还发现,GELN能够被肿瘤浸润的免疫细胞摄取,并增强其功能。在B16F10黑色素瘤小鼠模型中,GELN处理的小鼠肿瘤组织中CD8+ T细胞的干扰素-γ(IFN-γ)水平显著增加(P=0.0072),表明GELN能够增强肿瘤浸润T细胞的活性。此外,GELN处理的小鼠肿瘤组织中CD8+ T细胞的凋亡率显著降低(P=0.012 1),进一步证实了GELN在增强抗肿瘤免疫反应中的作用。研究还发现,GELN处理的小鼠肿瘤组织中CD8+ T细胞的增殖率显著增加(P=0.006 3),表明GELN不仅增强了T细胞的活性,还促进了其增殖。
04▼总结
本文通过多组学研究揭示了植物纳米颗粒(PNP)通过调节肠道微生物群代谢产物增强抗PD-L1免疫治疗的新机制。研究不仅阐明了PNP在调节肠道微生物群中的作用,还发现了其在免疫治疗中的潜在应用价值。这一发现为开发基于饮食调节的个性化癌症治疗方案提供了理论基础,也为未来的研究和临床应用提供了新的方向。通过进一步探索PNP与肠道微生物群的相互作用,有望为癌症患者提供更有效的治疗选择。
链接:http://www.lewenyixue.com/2025/04/01/Nature%E5%AD%90%E5%88%8A%E9%87%8D%E7%A3%85%EF%BC%81%E7%99%8C%E7%97%87%E6%99%9A%E6%9C%9F%E6%82%A3%E8%80%85%E5%A4%9A%E5%90%83%E8%BF%99/






赶快来坐沙发