Epcam 靶点 : 癌细胞转移“帮凶”
前 言
研究表明,Epcam(epithelial cell adhesion molecule,上皮细胞黏附分子)参与了肿瘤干细胞、细胞增殖、代谢、血管生成、上皮向间充质转化(EMT)、转移、化疗/放射抵抗和免疫调节等过程。在肿瘤发展过程中,EPCAM会与许多关键信号通路如Wnt/β-catenin、转化生长因子-β/SMAD、Epex/EGFR、PI3K/Akt/mTor和P53等发生串扰,诱导肿瘤细胞产生生物学变化。
例如增强Epcam表达能通过阻止细胞间黏附、促进免疫逃逸或激活白血病和结肠癌的下游致癌基因来促进癌症侵袭。在早期食道癌中,发现EpCAM表达减少会诱导EMT(上皮-间叶细胞转化过程),加速新陈代谢。所以Epcam在癌症发展过程扮演的角色“敌友难辨”鉴于其在癌症过程的复杂作用,EpCAM已成为癌症治疗中充满前景的靶点。并可作为监测CTCs(循环肿瘤细胞)和CSCs(肿瘤干细胞)的生物标志物。因此本文集中讨论了Epcam的结构特征和生物学功能。
01
EpCAM 的结构特征
Epcam(epithelial cell adhesion
molecule)亦称CD326,隶属GA733蛋白家族,是一种I型跨膜糖蛋白和同型Ca2+非依赖性细胞粘附分子,在多种正常上皮细胞的基底膜中低水平表达(结肠表达水平最高),而在癌细胞膜上广泛表达,尤其是鳞癌和腺癌。 同时Epcam也是当前全球首个进入靶向CAR-T细胞疗法相关临床研究的靶点
相关研究发现Epcam会参与细胞黏附过程,但其粘附性与钙粘附素相比更弱。值得注意的是,借助EpCAM的细胞黏附会受到CD44结合的claudin-7影响。EPCAM与两个claudin-7 和cLaudin-1分子相互作用,通过阻止其降解,来调节紧密连接的功能。当敲除EPCAM基因后,claudin-7和 claudin-1都会减少,紧密连接增加,细胞更不容易裂解,证明EpCAM在肿瘤侵袭和扩散中起着重要作用。

图1:Epcam结构示意图
02
肿瘤生物学中扮演角色
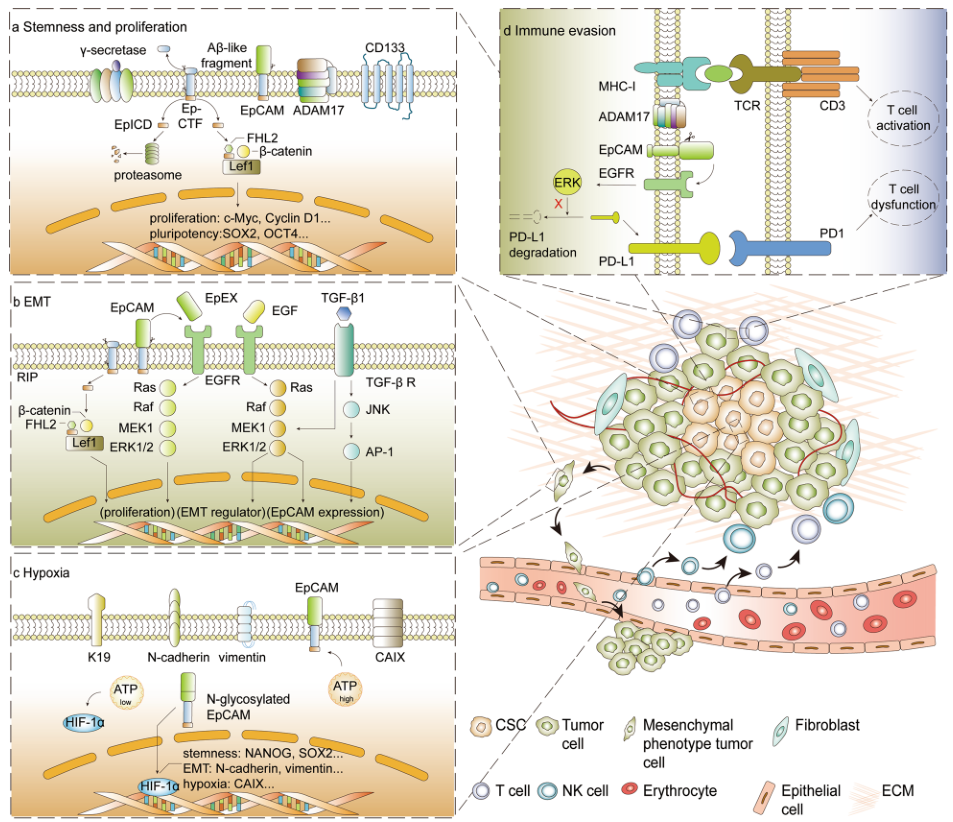
图2 EpCAM在肿瘤发生发展中的作用
一
癌症干细胞
先前研究表明,EpCAM会在人类胚胎干细胞上广泛表达,并在分化过程中发挥关键作用。Kuan 等人研究发现,Epex和EpCAM可以提高OCT4、SOX2、KLF4和c-myc的重编程效率,并通过STAT和HIF-2α诱导成纤维细胞向多能干细胞分化。
在癌症治疗领域,EpCAM是一个非常经典的CSCs(肿瘤干细胞)标志物。表达EpCAM的肿瘤细胞展现出更强的癌变能力,和更强的干细胞特性(化疗/放射抵抗、增强的成瘤性、血管生成、耐缺氧和转移集落形成能力)。
二
细胞代谢与血管生成
比较四种表达EpCAM和AFP的肝癌,发现EpCAM+/AFP+人群的微血管密度和EGF表达水平较高。此外,Sankpal 等人发现EPCAM可调节IL-8和NF-κB转录因子在BC侵袭和血管生成中的活性。针对VEGFR2/EpCAM的双抗的增强效应及通过降低IL-8和IL-6对血管生成的调节表明EpCAM可能是预防肿瘤进展中血管生成的理想靶点。
三
免疫逃避和调节
EpCAM会参与肿瘤免疫调节,Park等人推断EpCAM含量较高的肝癌会通过上调癌胚抗原相关细胞黏附分子1来抵抗NK细胞介导的细胞毒作用。
与之类似,EpCAM+CD45+卵巢癌细胞通过过度表达主要组织相容性复合体I类抗原(MHC-I)来逃避NK细胞介导的免疫监控。
四
EMT过程中的动态表达和背景依赖性
EpCAM在EMT(上皮细胞-间充质转化)过程中处于动态并具有背景依赖性(图2D)。鉴于EpCAM是一种黏附分子,推测EpCAM的表达下调是为了提高癌细胞迁移率,但细胞黏附分子通过干扰α-连环蛋白和F-肌动蛋白之间的联系而减弱E-钙粘附素介导的细胞间黏附作用。
此外,EPCAM与EMT相关基因的表达呈正相关。在不同的研究中得到的结果并不一致。在TGF-β1诱导的食管癌细胞内皮细胞转化过程中,Epcam在细胞膜表面的表达显著减少,细胞的迁移、侵袭和扩散能力得到了提高。而低表达的EpCAM增强了癌细胞的EMT,并与子宫内膜癌的晚期肿瘤分期和淋巴转移发生相关。

03
EpCAM在临床肿瘤学中的应用
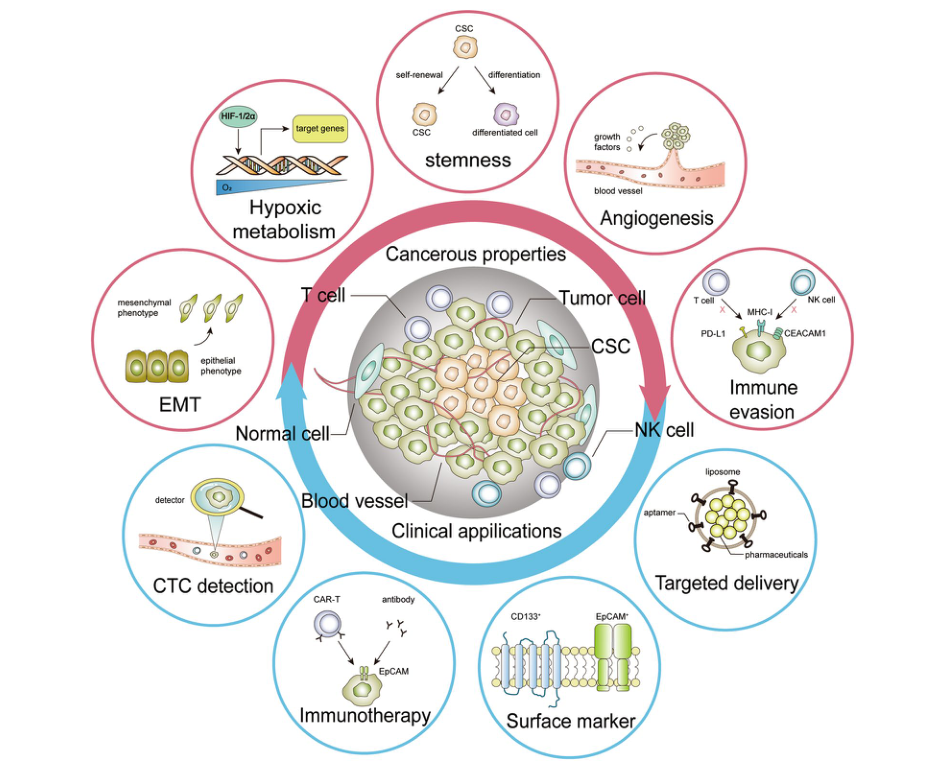
图3 EpCAM的功能和应用
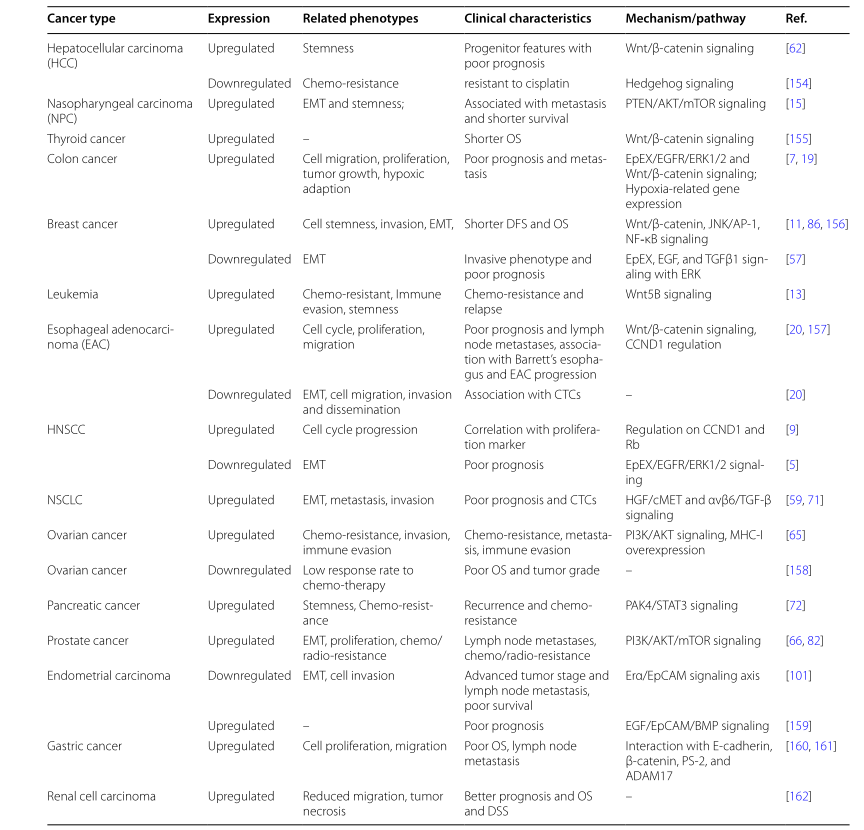
EpCAM仅在上皮性肿瘤中表达,在外胚层或中胚层肿瘤中不表达。但EPCAM在乳腺癌、肝癌和胰腺癌中的表达水平与预后不良相关,而在甲状腺和肾癌中过度表达则预后较好。但在食道癌和结直肠癌中,EpCAM过度表达与患者生存之间的相关性仍然存在争议,这表明EpCAM对癌症或抑制或促进作用其实更取决于肿瘤微环境和癌症类型。但Epcam在肾癌中的表达有很高的预后价值。
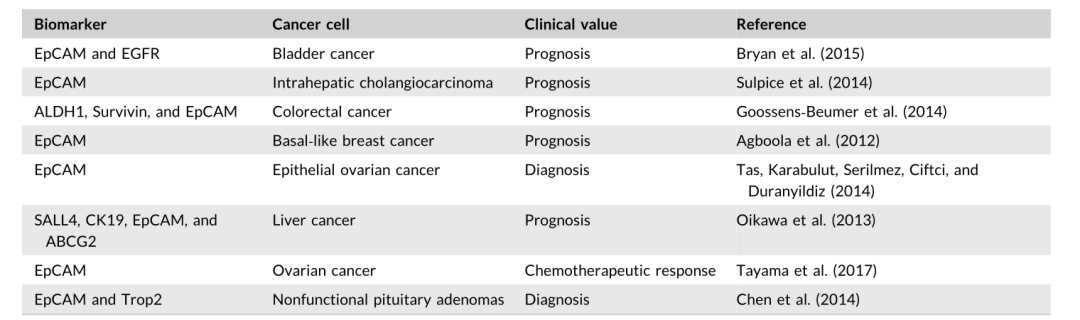
表1 :EpCAM与其他生物分子联合检测对肿瘤预后和诊断的作用
一
肿瘤中表达及预后价值
EpCAM参与了癌症多个进程。除了其在预测转移和检测CTCs方面的诊断和预后价值外,它在癌症中的独特表达模式使其成为诊断和预后的生物标记物,详见表2
表2: EpCAM在肿瘤治疗中的免疫治疗应用
二
基于EpCAM的CTC检测与诊断方法
CTCs(肿瘤循环细胞)是检测癌症转移的重要标志。CTC在肿瘤转移过程中起主要作用,是多种癌症的预后指标。CTCs是非常罕见的细胞(每毫升患者血液中有1-10个CTCs),其中只有少数具有转移能力。测量外周血中的这些细胞,除了更准确地确定疾病的阶段外,对病人的伤害也较小。 但值得注意的是epcam不会在CTCS表面表达。
但epcam会在大多数上皮源性癌症高度表达,因此是检测CTCs的一个标志物。然而,通过EpCAM检测CTCs的方法存在不足之处。传统的基于EpCAM的CTC检测策略仅限于EpCAM阳性的CTC,并且由于EMT,还可能忽视最具侵袭性的肝癌CTC亚群的风险,导致循环中CTC的总数偏小。
三
化学修饰和靶向治疗
先前研究表明,EpCAM在人类胚胎干细胞上广泛表达,并在分化过程中发挥关键作用。Kuan 等与传统的抗体介导的肿瘤治疗相比,可以用核酸适配体来提高药物递送的特异性和亲和力。由于EpCAM在肿瘤细胞上高度表达,尤其是CSCs,靶向EpCAM的适配体被广泛应用于癌症治疗。与双特异性抗体类似,用双特异性适配子同时靶向CD44和EpCAM比单适配子效果更好。此外,该适配子对寄主无毒性,对天然免疫无激活作用。

04
EpCAM在免疫治疗中的应用
一
单抗
临床上已报道了许多有希望用于癌症治疗的EpCAM抗体(表3)。
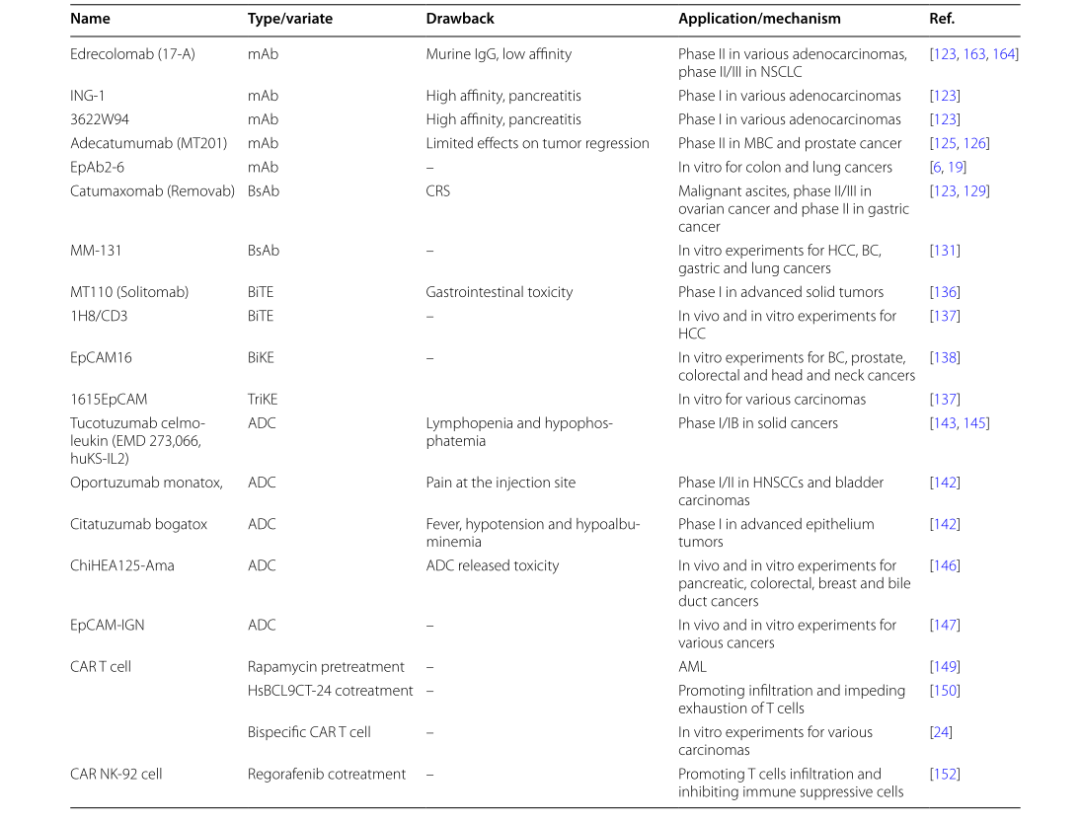
表3 EpCAM在肿瘤治疗中的免疫治疗应用
第一个单克隆EpCAM抗体edrecolomab(17-1A)是从小鼠腹水中提取的IgG2a,但在多种腺癌中的治疗效果有限,这可能是因为它和肿瘤的亲和力较低。随后开发了抗体工程和人源化抗体ING-1和3622W94,并在腺癌中进行了测试。
这两种抗体与EpCAM具有较高的亲和力,但耐受性较低,并会诱发胰腺炎。激素难治性前列腺癌患者的I期研究和EpCAM阳性复发或难治性晚期乳腺癌的IB期研究证实了adecatumab的有效性。EpAb2-6则是一种新的EpCAM中和抗体,它通过抑制EpicD/β-连环蛋白复合体的核转位和诱导结肠癌细胞凋亡发挥抗肿瘤作用。此外,EpAb2-6通过提高A2表达所需温度和降低PD-L1蛋白水平来增强CD8+T细胞的细胞毒活性来阻止肿瘤进展。
二
EpCAM双特异性抗体及其变体
已开发双特异性或嵌合抗体来增强抗肿瘤疗效(上表3)。Catumaxomab(Removab)具有两个抗原结合位点(EpCAM和CD3)和一个Fc结构域,在体外可启动T细胞介导的杀伤、细胞因子相关的细胞毒作用、抗体依赖的细胞介导的细胞毒(ADCC)性和补体依赖的细胞毒性(CDC)。在II/III期研究的恶性腹水患者中,Catumaxomab治疗组的总生存期(OS)显著延长。MM-131是一种抗EpCAM/Met双特异性抗体,对Met信号通路既有依赖又有非依赖性抑制作用,对Met诱导的肝癌、BC、胃癌和肺癌的增殖均有抑制作用。
双特异性T细胞结合抗体(BITE)通过将T细胞与癌细胞联系起来,刺激T细胞活化、肿瘤杀伤和细胞因子的产生,从而增强患者对肿瘤的免疫反应。Solitomab(MT110)是一种与EpCAM和CD3结合的双特异性T细胞结合抗体(BITE),可有效治疗原发性子宫和卵巢癌肉瘤。MT110的作用机制主要依赖于T细胞活化后穿孔素和颗粒酶的释放。但由于其胃肠道毒性,solitomab最终被停用。
EpCAM反义寡核苷酸1H8/CD3成功地抑制了肝癌移植瘤的生长,并降低了大多数CSC生物标志物的表达。为了降低T细胞活化引起的有害细胞因子毒性,开发了靶向NK细胞上的CD16和肿瘤细胞上的EPCAM的双特异性NK细胞活化子(Bike),以此介导ADCC对EPCAM+HT-29结肠癌细胞的杀伤作用。经白介素15交联剂修饰的三特异性NK细胞激活剂(TRIKE)与BIKE相比,对NK细胞的激活、增殖和存活均有改善。
三
EpCAM ADC
EpCAM抗体-药物结合物(ADC)也在应用于EpCAM+癌症治疗(表3)。Oportuzumab monatox由抗EpCAM单链可变区和假单胞菌外毒素A(ETA)片段组成,在ADC内化和ETA释放后发挥抗瘤作用。与之类似,Citatuzumab bogatox是由抗EpCAM Fab和非免疫原性九重葛毒素组成。针对各种癌症的I期和II期临床试验表明,它们对癌症治疗都具有良好的耐受性和有效性。Tucotuzumab celmoleukin(EMD 273,066,Huks-IL2)是通过将白细胞介素2(IL-2)基因融合到人源化的抗EpCAM单抗上而产生的一种免疫细胞因子,这种基于抗体的新疗法可能通过IL-2激活淋巴细胞。
此外,Tucotuzumab celmoleukin与射频消融联合应用可增强小鼠结肠癌的抗肿瘤作用和免疫记忆。Tucotuzumab celmoleukin对癌症患者的安全性和有效性在I期和IB期研究中得到证实。体外细胞系分析和体内动物实验证明,更多ADC有望用于癌症治疗。ChiHEA125-AMA是α-Amanitin与嵌合的抗EPCAM单抗的偶联物,在胰腺癌、乳腺癌和其他癌症中展现出抑制肿瘤的潜力。相应地,吲哚苯二氮二聚体(IGN)与EpCAM(EpCAM-IGN)抗体的结合显示出剂量依赖性的抗肿瘤活性。
四
CAR-T
除了抗体介导的治疗外,细胞免疫,特别是T细胞治疗,在癌症治疗中展示出一定前景。最近一项研究表明,异位表达miR-200C和EpCAM的CD8+T细胞会降低细胞凋亡,并增强抗瘤反应。靶向EpCAM的CAR - T疗法已取得了一定成功(表2),与EpCAM−急性髓系白血病细胞相比,EpCAM+急性髓系白血病细胞具有更强的致瘤性和化疗耐药性,因为正常骨髓细胞和外周血单核细胞均不表达EpCAM。因此,靶向EpCAM的CAR -T是治疗AML的理想方法。此外,雷帕霉素可抑制mTORC1活性,上调CXCR4,从而促进EpCAM Car T细胞在骨髓中的迁移和穿透能力,治愈急性髓系白血病(AML)。

结语
随着基础研究的进步,EpCAM被发现在癌症进展中起着多方面的作用。除其在细胞黏附中的作用外,EpCAM还会通过调节胞外和胞内的细胞信号来实现多种功能,EpCAM通过调节细胞特性,如增殖、干细胞、移动性、化疗/放射治疗来调控癌症的进展。但其实无法断言Epcam扮演的是致癌角色或肿瘤抑制角色。但从临床角度来看,EpCAM对癌症患者的诊断和预后有很大的潜在价值。靶向EpCAM的抗体已应用于临床,随着研发人员对epcam了解的不断深入,未来在癌症治疗中将更具价值。
关于仁域
成都仁域生物目前搭建了全面优化国际一流的噬菌体展示抗体文库技术平台、拥有超万亿级全人源抗体库(scFv/Fab)、万亿级天然骆驼纳米抗体库(VHH)、以及现代化骆驼/羊驼养殖免疫基地,能根据客户蛋白特点提供高通量、个性化的优质候选抗体开发服务,更高的性价比和效率。
注:以上图片均来自参考文献
链接:http://www.lewenyixue.com/2025/04/01/Epcam%20%E9%9D%B6%E7%82%B9%20%3A%20%E7%99%8C%E7%BB%86%E8%83%9E%E8%BD%AC%E7%A7%BB%E2%80%9C%E5%B8%AE%E5%87%B6%E2%80%9D/





赶快来坐沙发