人工智能助力寻找抗癌药物!复旦团队突破传统筛选技术局限
近日,复旦大学药学院王建新教授团队联合上海交通大学郑双佳长聘教轨助理教授及星药科技李成涛博士,在 Nano Today 发表题为" Geometric-aware deep learning enables discovery of bifunctional ligand-based liposomes for tumor targeting therapy "的研究成果。该研究通过整合几何感知深度学习算法与生物实验验证体系, 建立了天然产物功能预测与验证的双向研究平台 。
研究团队运用自主开发的深度学习模型对30+天然产物分子库进行高通量筛选,成功鉴定出兼具脂质膜调控(LMR)与葡萄糖转运蛋白1(Glut1)靶向功能的天然化合物,并构建了新型双功能脂质体载药系统,在小鼠模型中展现出显著的肿瘤靶向与治疗增效作用。该研究探索了“人工智能深度学习预测+实验验证”的交叉研究方法体系,为智能药物递送系统设计提供了新的范式。
传统脂质体肿瘤靶向能力有限,从而影响其临床疗效。虽然配体修饰的脂质体在提升肿瘤靶向效率方面展现出潜力,但工艺复杂,临床转化难。项目组前期研究发现某些天然产物兼具脂质体膜调控与肿瘤靶向功能,有望无需配体合成,简单替换脂质体中的胆固醇为该类天然产物即实现肿瘤靶向。
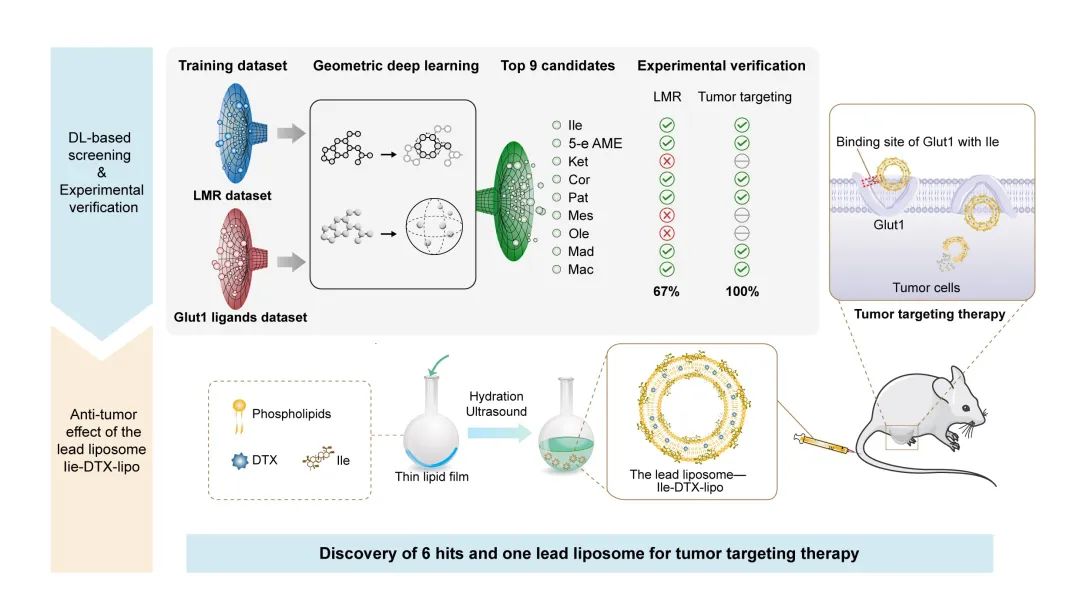
但天然产物多达30多万种,传统试错法筛选该类双功能天然产物耗时费力。该研究提出将人工智能深度学习算法模型与湿实验相结合,快速发现新型双功能天然产物。通过数据集收集、几何感知深度学习模型构建、性能预测及湿实验验证, 从超30万种天然产物中高效筛选出6个双功能天然产物。 其中,基于冬青苷元A(Ile)构建的脂质体在肿瘤靶向能力和抗肿瘤效果最优,证实了深度学习技术在设计智能靶向药物递送系统中的巨大潜力。
▲机器学习辅助新型双功能天然产物挖掘工作流程图及基于双功能天然产物的肿瘤靶向脂质体示意图 (图片来源:原始论文[1])
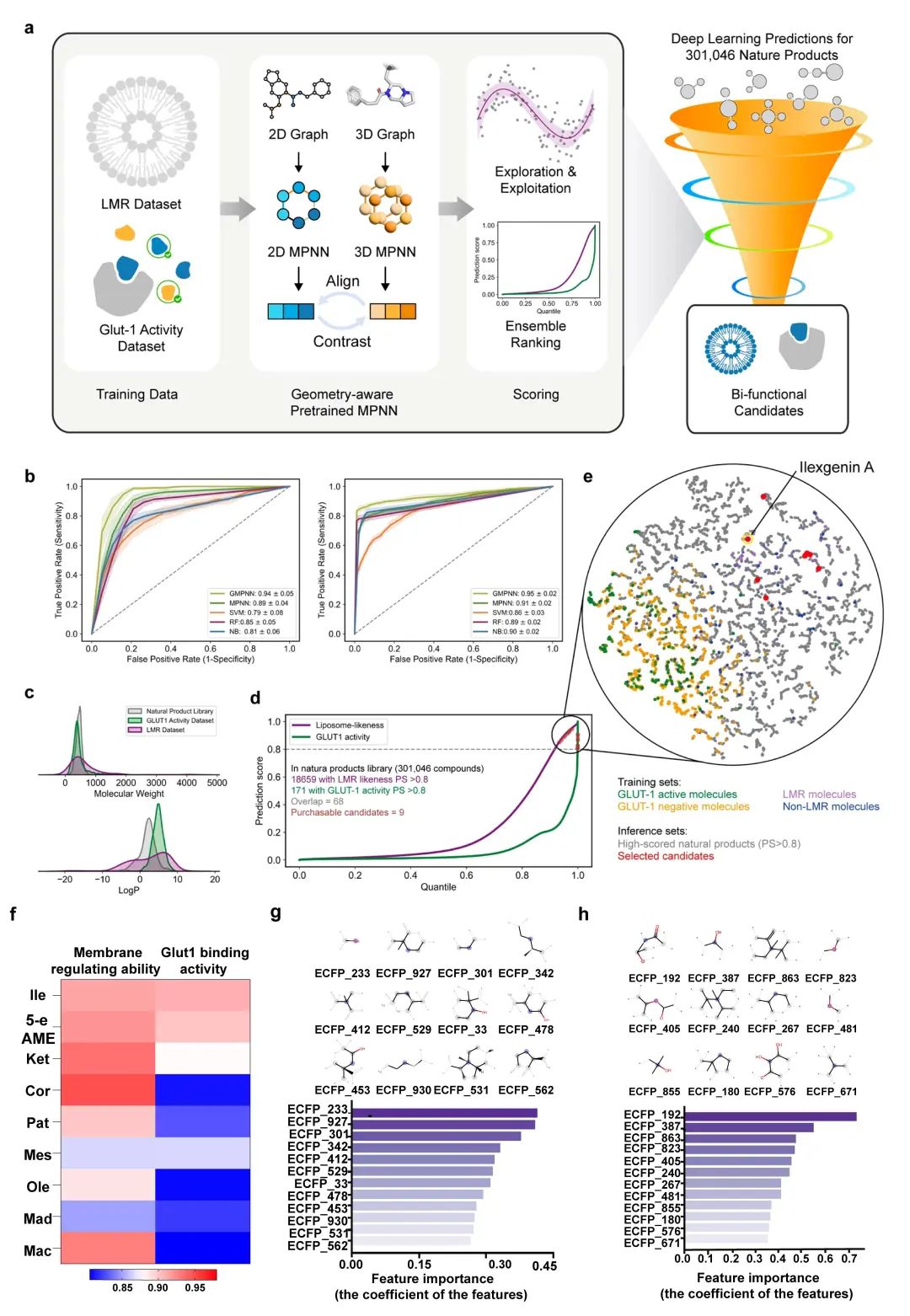
研究团队开发了一种几何感知消息传递神经网络(GMPNN),通过对比学习策略,从分子二维结构中推断三维构象信息,克服了传统深度学习模型对大数据集的依赖及几何特征建模的不足。该模型经收集的LMR及肿瘤靶标葡萄糖转运体(Glut1)配体数据集训练后,在LMR预测和Glut1结合活性预测任务中表现优异,显著优于支持向量机(SVM)、随机森林(RF)等传统方法。基于该模型,团队对天然产物库(DNP)中30余万种分子进行虚拟筛选,结合结构多样性与相似性分析,最终选出9种候选分子。
▲GMPNN算法模型构建及候选双功能天然产物挖掘 (图片来源:原始论文[1])
湿实验验证结果表明,GMPNN优选出的9个候选物中的6个均可代替胆固醇作为LMR制备粒径均一(约100 nm)、稳定性良好的脂质体。 上述具LMR功能的候选物均表现出显著的Glut1介导的肿瘤靶向能力,其制备而成的脂质体肿瘤靶向作用均优于传统胆固醇脂质体。 此外,Ile脂质体(Ile-lipo)的肿瘤靶向作用最优 。
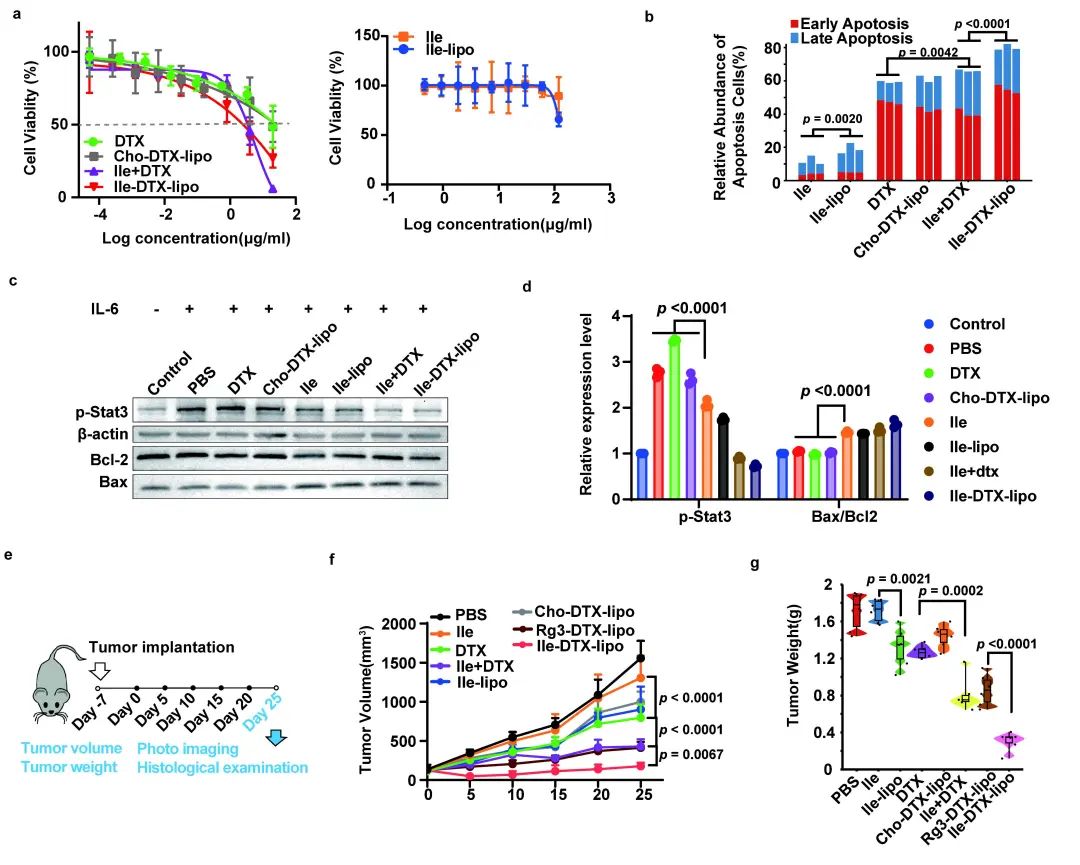
最终,包载化疗药物多西他赛(DTX)的Ile脂质体(Ile-DTX-lipo)凭借其优异的肿瘤靶向作用表现出显著的抗肿瘤作用,是具有开发潜力的肿瘤靶向药物递送系统。
▲Ile-DTX-lipo的抗肿瘤作用Ile-DTX-lipo的抗肿瘤作用 (图片来源:原始论文[1])
该研究首次将几何感知深度学习应用于双功能配体的高效发现,突破了传统筛选的局限性,显著提高了功能材料的筛选成功率。筛选得到的Ile脂质体因其简易制备工艺、优异靶向性及免疫调节功能,具有良好的临床转化前景。且这一策略可为其他疾病靶点的靶向递送系统开发提供参考借鉴。
链接:http://www.lewenyixue.com/2025/03/27/%E4%BA%BA%E5%B7%A5%E6%99%BA%E8%83%BD%E5%8A%A9%E5%8A%9B%E5%AF%BB%E6%89%BE%E6%8A%97%E7%99%8C%E8%8D%AF%E7%89%A9%EF%BC%81%E5%A4%8D%E6%97%A6%E5%9B%A2%E9%98%9F%E7%AA%81%E7%A0%B4%E4%BC%A0/






赶快来坐沙发