中国医学科学院:肿瘤治疗新靶点A1,免疫疗效翻倍的秘密

【导读】 免疫检查点阻断疗法(ICB)给癌症治疗带来了革命性的变化,但治疗反应却具有高度异质性,这凸显了开发预测性生物标志物和克服ICB耐药性的必要性。
2025年3月17日,中国医学科学院肿瘤医院的研究团队在期刊《Signal Transduction and Targeted Therapy》上发表了题为“Targeting tumor-intrinsic S100 calcium-binding protein A1 augments antitumor immunity and potentiates immunotherapy efficacy”的研究论文。

https://www.nature.com/articles/s41392-025-02190-2
文章强调了通过靶向肿瘤内在特征(如S100A1)来重塑TME,增强免疫治疗效果的潜力,并提出了GM-CSF与ICI联合治疗作为一种新型免疫治疗策略的可能性。
01
研究背景
越来越多的证据表明,肿瘤细胞通过改变Ca 2+稳态促进多种恶性生物学行为,如肿瘤生存、增殖和免疫逃避等。S100A1对调节细胞内Ca 2+信号传导和平衡至关重要。最近的研究表明,S100A1在多种类型的实体瘤中异常表达,参与细胞周期调控、细胞凋亡、恶性侵袭和转移等生物学过程。S100A1不仅是一种细胞内信号分子,还是一种分泌蛋白,这使治疗方法变得更加复杂。S100A1-靶标复合物及其功能,尤其是在调节TME和抗肿瘤免疫以及增强癌症免疫疗法方面的功能,尚未完全明确。
02
GM-CSF引物可增强S100A1高表达肿瘤的抗PD-1疗效
最近的研究表明,用GM-CSF引导 “冷 ”PyMT肿瘤可增强对ICB的反应性。这一效应归因于肿瘤血管的正常化,从而降低了肿瘤的缺氧。这些研究结果突显了在设计免疫疗法策略时仔细考虑GM-CSF的背景的重要性。GM-CSF引物提高了S100A1高表达的LLC异种移植物的抗PD-1敏感性。在S100a1OE MC38异种移植物中也得到了类似的结果。 这些观察结果揭示了S100A1在预测ICB反应和患者预后方面的潜力,以及S100A1/USP7/p65调节轴在调节GM-CSF表达方面的作用。S100A1高表达的肿瘤的GM-CSF引物逆转了免疫学上 “冷 ”的TME,从而增强了免疫疗法的疗效。
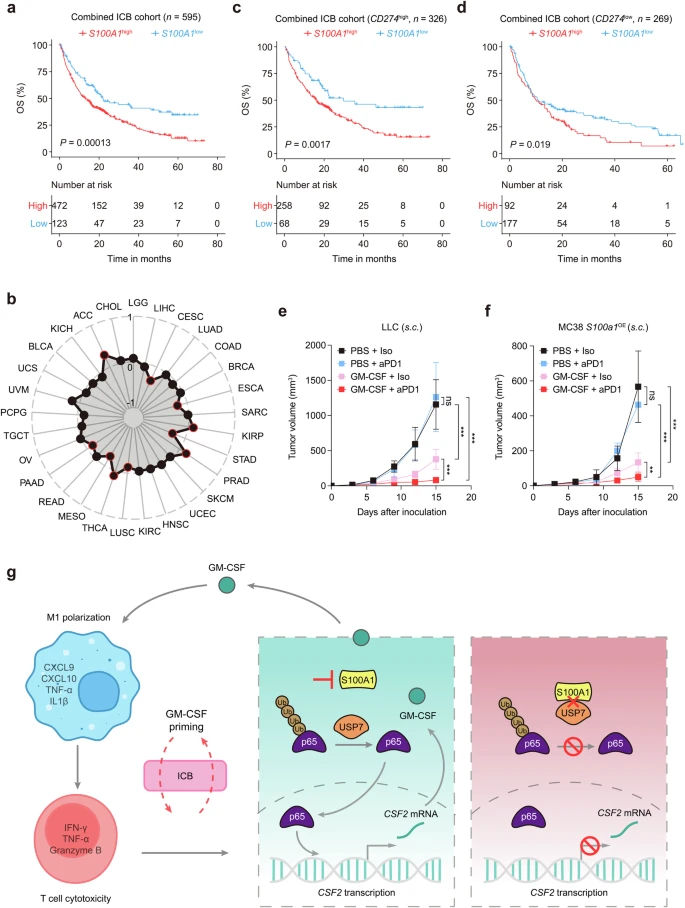
GM-CSF可增强S100A1高肿瘤小鼠的抗PD-1疗效。
03
总结
1. 重塑TME的策略:通过靶向肿瘤内在特征(如信号通路失调、代谢重编程等),可以将TME从支持肿瘤的状态重新编程为抑制肿瘤的状态,从而提高免疫治疗的效果。
2. S100A1的作用:研究发现,抑制肿瘤内在的S100A1可以通过激活GM-CSF信号传导,将巨噬细胞重编程为M1样极化状态,并促进T细胞介导的免疫反应,从而增强免疫治疗的疗效。
3. GM-CSF的潜在应用:GM-CSF与ICI联合使用可能有助于将免疫抑制性的“冷”TME重塑为炎症表型,增强抗肿瘤免疫反应。临床试验表明,GM-CSF与ICI联合治疗在某些癌症中显示出协同作用。
4. S100A1作为生物标志物的潜力:S100A1可能作为一种预测性生物标志物,用于分层患者对ICB与GM-CSF联合治疗的反应。
5. 未来研究方向:需要进一步研究S100A1调节的信号通路、其分泌机制以及与免疫治疗反应和耐药机制相关的钙信号作用。

参考资料:
1.Sanmamed, M. F. & Chen, L. A paradigm shift in cancer immunotherapy: from enhancement to normalization. Cell 175, 313–326 (2018).
2.Morad, G., Helmink, B. A., Sharma, P. & Wargo, J. A. Hallmarks of response, resistance, and toxicity to immune checkpoint blockade. Cell 184, 5309–5337 (2021).
链接:http://www.lewenyixue.com/2025/03/18/%E4%B8%AD%E5%9B%BD%E5%8C%BB%E5%AD%A6%E7%A7%91%E5%AD%A6%E9%99%A2%EF%BC%9A%E8%82%BF%E7%98%A4%E6%B2%BB%E7%96%97%E6%96%B0%E9%9D%B6%E7%82%B9A1%EF%BC%8C%E5%85%8D%E7%96%AB/





赶快来坐沙发