Science | 最新研究揭示:罕见胚系结构变异增加儿童实体瘤风险,预计可解释1.1%-5.6%的儿童癌症易感性
儿童实体瘤占每年新诊断儿童癌症病例的三分之一,是儿童发病率和死亡率的一个主要原因。胚系遗传因素被认为在儿童实体瘤发病机制中起重要作用,但目前公认的相关易感基因仅占所有诊断的10%-15%。因此,确定更多的胚系风险因素将有助于加深对儿童实体瘤的生物学理解,进而为临床管理和治疗提供支持。
文章通讯作者、哈佛医学院Broad研究所和Dana-Farber癌症研究所研究员Eliezer Van Allen表示:“总的来说, 该研究结果表明,跨越编码和非编码位点的罕见胚系SV是儿童实体瘤的重要风险因素。该研究支持将胚系SV分析整合到与儿童实体瘤易感性相关的临床实践和研究工作中。”
研究团队使用一种基于云的流程GATK-SV对1765名儿童实体瘤患者进行了全基因组测序分析,以寻找相关的罕见胚系SV,其中包括789例尤文氏肉瘤患者、690例儿童神经母细胞瘤患者和286例骨肉瘤患者。 同时,943名未受影响父母和6665名成人对照也进行了胚系基因组测序。 研究比较了儿科患者和成人对照中罕见胚系SV的模式。
研究发现,每个基因组中平均有7275个胚系SV。总体而言, 神经母细胞瘤、尤文氏肉瘤和骨肉瘤的新生胚系SV发生率与普通人群相当(约0.2个/基因组),并且新生SV明显大于遗传SV,更有可能造成基因破坏 。分析显示,超过1 Mb的超稀有胚系缺失或重复是儿童实体瘤性别偏好的风险因素,在男性患者中的富集是无癌症对照的4倍。通过实施全类别关联研究框架,研究发现突变约束基因的胚系SV在神经母细胞瘤患者中富集,而影响DNA损伤修复基因的SV在尤文氏肉瘤和神经母细胞瘤中均有富集。将这些基因破坏性SV与基因表达数据交叉对比发现, 患者的SV倾向于破坏其癌源组织中高表达的基因 ,这些SV导致的异常表达在患者的肿瘤中表现出来。
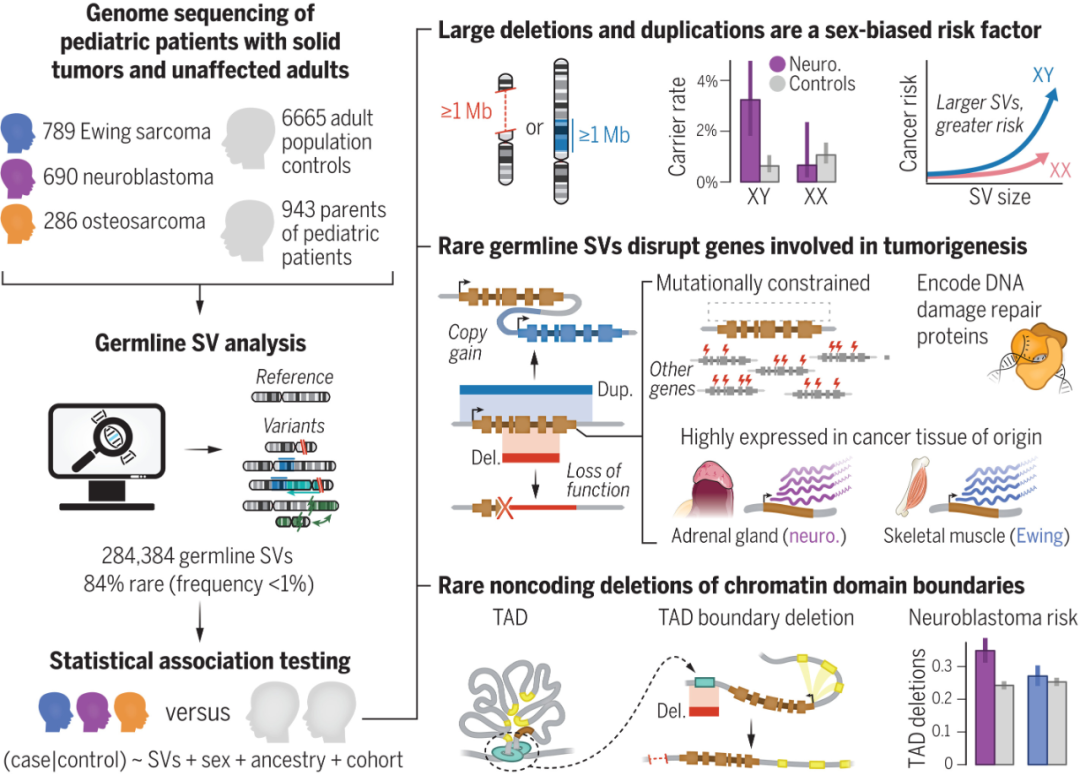
图:罕见胚系SV是儿童实体瘤的风险因素。
此外,研究人员 还发现了数十个影响癌症易感基因的胚系SV ,如神经母细胞瘤中的PHOX2B和BARD1,以及Ewing肉瘤中的Fanconi贫血基因,表明胚系SV分析可以在个体患者基因组中揭示新的临床相关发现。最后,研究发现与成人对照相比,神经母细胞瘤中重叠染色质结构域边界的超稀有SV富集,尤文氏肉瘤没有这种情况。这意味着 蛋白质编码基因外的罕见非编码SV亚群可能与一些儿童实体瘤的发病机制有关。
总之,该研究证实,跨越编码和非编码位点的罕见胚系SV是儿童实体瘤的重要风险因素。其中,SV在神经母细胞瘤中的作用高于尤因肉瘤,这与神经母细胞瘤发病年龄明显较早一致。 研究预计罕见胚系SV可解释1.1%-5.6%的儿童癌症易感性。
研究团队表示,在其他儿童癌症患者中进行的胚系WGS工作将进一步推广和复制该研究的发现,以及发现其他疾病特异性风险因素。该研究未来的工作重点是对同一患者中具有SNV和Indel的SV进行全基因组综合评估,这将使人们更全面地了解导致儿童癌症发展的胚系因素,进而更好地了解导致这些恶性肿瘤风险的中心致癌程序。
同时, Science 发表了一篇针对该研究的观点文章,西班牙国家癌症研究中心的Geoff Macintyre和荷兰马克西玛公主儿科肿瘤学中心的Jayne Hehir-Kwa认为:“该研究结果表明 胚系SV可能会导致这些儿童实体瘤的早期基因组不稳定,并可能为靶向治疗的设计提供信息 。采用更精确、更有针对性的方法治疗儿童实体瘤不仅可以提高治疗效果,而且可以减少儿童患者因长期毒性引起的晚期影响,并降低与传统疗法相关的继发恶性肿瘤的风险。”
https://www.science.org/doi/10.1126/science.adq0071
链接:http://www.lewenyixue.com/2025/01/10/Science%20%7C%20%E6%9C%80%E6%96%B0%E7%A0%94%E7%A9%B6%E6%8F%AD%E7%A4%BA%EF%BC%9A%E7%BD%95%E8%A7%81%E8%83%9A/





 知道|国家药品不良反应监测年度报告(2024年)
知道|国家药品不良反应监测年度报告(2024年)
赶快来坐沙发