【AJH】PI3Kδ抑制剂和CD20单抗治疗R/R CLL可降低肿瘤负荷但会诱导耐药
CD20单抗及BCR信号通路和BCL2信号通路的小分子抑制剂极大地改善了进展性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL)患者的治疗,但并不能实现治愈,而且疗效可能受到副作用和获得性耐药的影响,特别是对于无限期治疗方案。为了解决这些问题,学者在复发/难治性(R/R)CLL患者中评估了一种有限期三联方案(包含CD20单抗ublituximab [UBL]、PI3Kδu抑制剂umbralisib [UMB]和BCL2抑制剂维奈克拉;简称U2-VEN),近日发表于《American Journal of Hematology》。

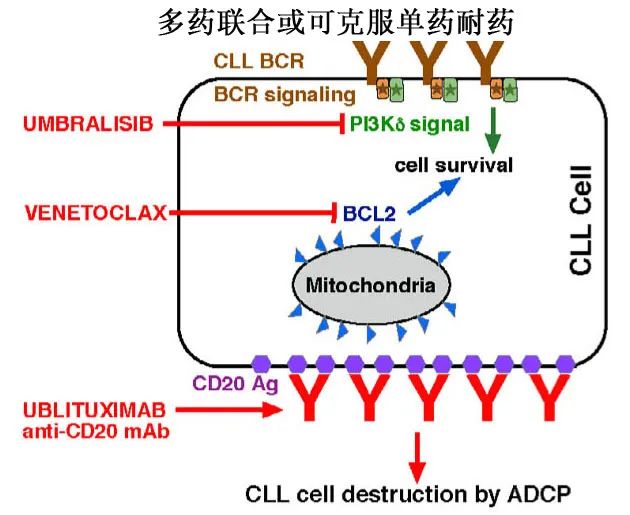
三种药物具有不同作用机制的药物,可能会增加疗效并降低耐药的可能性。ublituximab (UBL)是糖工程嵌合单克隆抗体,靶向CLL细胞表面CD20抗原(Ag)上的独特表位,主要通过抗体依赖性细胞吞噬(ADCP)破坏CLL细胞;umbralisib (UMB)是新型小分子BCR信号抑制剂,对磷酸肌肽3-激酶δ (PI3Kδ)和酪蛋白激酶1 epsilon具有高度选择性,可通过阻止细胞存活信号导致CLL细胞死亡;维奈克拉(VEN)可阻断BCL2促进的细胞存活,阻止线粒体启动凋亡。
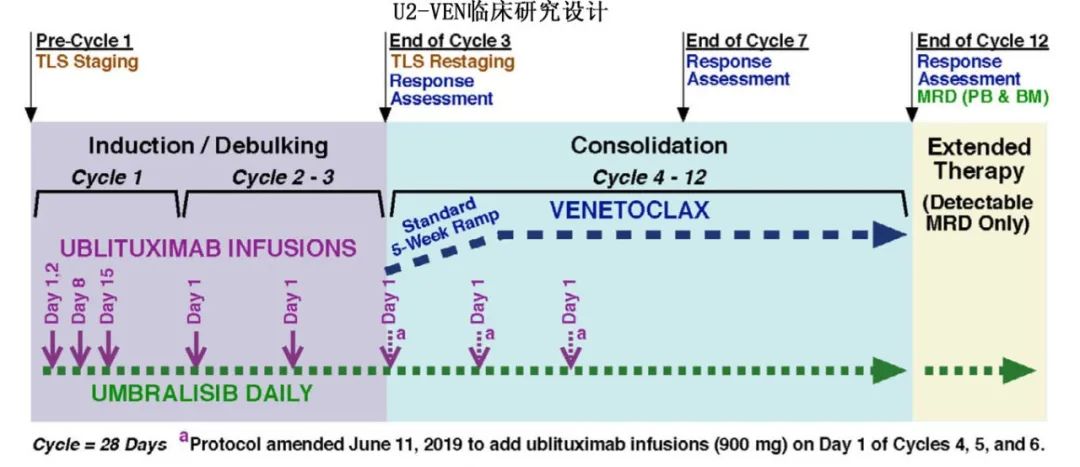
治疗方案:最初使用UBL和UMB治疗12周,使BCR信号抑制药物动员CLL细胞进入循环,使其更容易受到单抗细胞毒性的影响,从而减少CLL肿瘤负荷和VEN诱导的肿瘤溶解综合征的风险;VEN在13周加入。
共纳入25例R/R CLL患者,大多数患者为Rai晚期,具有高危遗传学特征,并且既往2线治疗均失败。
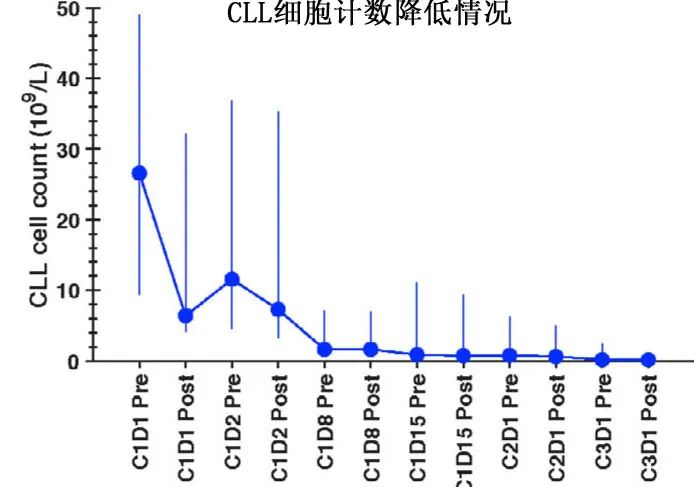
UMB和UBL治疗CLL后肿瘤负荷迅速下降。基线治疗前(C1D1 Pre, n=25) CLL细胞计数中位值为26.6×10 9/L。在第一次给药UMB(每12小时口服800mg)和UBL (150mg IV)后,CLL计数中位数从基线下降到6.4×10 9/L,下降了60%。在第2天(C1D2),治疗前中位CLL细胞计数反弹到基线的62% (11.5×10 9/L),然后在第二次UBL给药(750mg IV)后下降到基线的44% (7.3×10 9/L)。中位CLL细胞计数从第8天(C1D8)的1.6×10 9/L(基线的9%)逐渐下降到治疗8周(C3D1)后的0.16×10 9/L(基线的1.2%)。
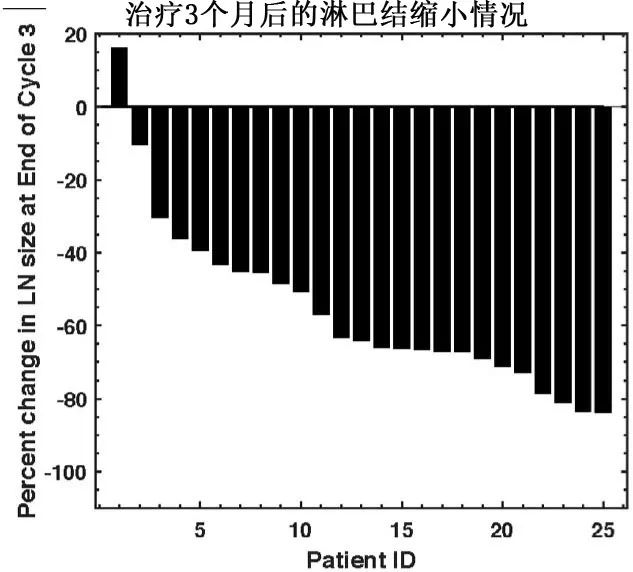
连续CT扫描显示,治疗12周后,24例患者计算淋巴结体积减少(中位数64%)。
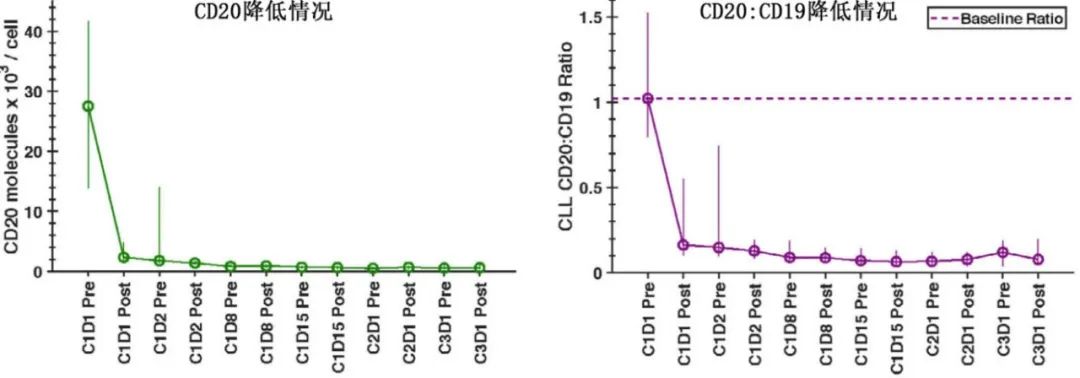
UMB和UBL治疗也与CLL表面CD20水平的快速和持续下降有关。给药150mg UBL后,CLL细胞膜CD20的中位基线水平(27500分子/细胞C1D1 Pre,n=18)降至2330分子/细胞(基线的8%)。且随着时间的推移,CD20水平中位数继续下降,C1D2 Pre为1783分子/细胞,C1D2 Post为1374分子/细胞,C1D8为820分子/细胞,C3D1为528分子/细胞。相比之下,CLL细胞膜CD19水平并未因治疗而降低。CLL CD20抗原水平的严重下降可能会降低UBL治疗的有效性。
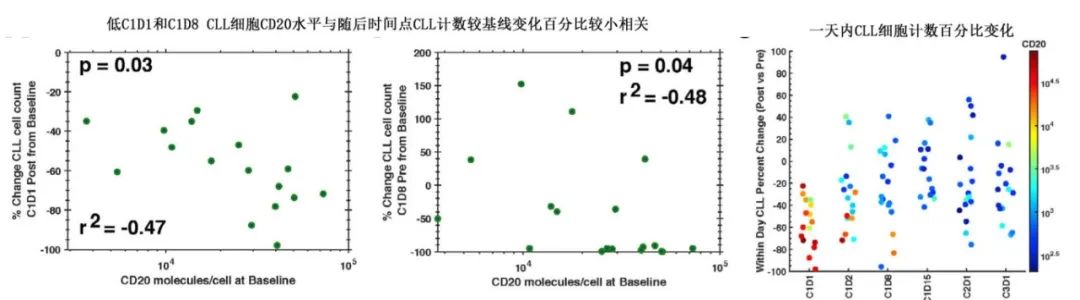
治疗前CLL细胞中CD20水平最高,治疗第一天后CLL细胞与基线相比清除率最大。治疗前CD20水平较高与治疗反应较大存在显著关联。CD20水平越高,计数下降的幅度越大。C1D8后CLL细胞CD20水平普遍较低,每次输注UBL后变化最小。这些数据表明,CD20水平在这些较晚时间点下降到UBL不再有效的程度。

该研究证实,UMB和UBL联合开始治疗迅速达到减少肿瘤负荷和降低维奈克拉诱导的肿瘤溶解综合征风险的预期目的。但也发现,UBL在减少循环CLL细胞方面的功效仅限于前两次给药,后续的额外CLL细胞清除量极小。由于UMB退出市场和决定不再进一步开发UBL,该研究产生的直接价值不高,但对于设计CLL的未来临床试验仍很重要,相关临床试验可能使用CD20单抗单药或联合BCR信号抑制剂(如BTK或PI3Kδ抑制剂)。具体而言,CD20单抗联合BCR通路抑制剂的治疗效果可以通过设计最小化CLL细胞表面CD20损失的治疗方案来优化。
参考文献
Bruno, J.E., Herne, C.A., Baran, A.M., VanDerMeid, K.R., Barr, P.M., Williams, A.R., Quataert, S.A., Mosmann, T.R., Zent, C.S. and Chu, C.C. (2025), Treatment of Relapsed/Refractory CLL Patients With PI3Kδ Inhibitor and Anti-CD20 Antibody Rapidly Decreases Tumor Burden but Could Induce Resistance. Am J Hematol. https://doi.org/10.1002/ajh.27569
链接:http://www.lewenyixue.com/2025/01/07/%E3%80%90AJH%E3%80%91PI3K%CE%B4%E6%8A%91%E5%88%B6%E5%89%82%E5%92%8CCD20%E5%8D%95%E6%8A%97/






赶快来坐沙发