Cell子刊:宋尔卫院士团队最新临床研究,靶向细胞自噬+CDK4/6抑制剂,治疗晚期乳腺癌

编辑丨王多鱼
排版丨水成文
对于接受 细胞周期蛋白依赖激酶4/6抑制剂 (CDK4/6i) 治疗后发生疾病进展的激素受体阳性/人表皮生长因子受体2阴性 (HR + /HER2 - ) 乳腺癌患者,治疗需求尚未得到满足,这一问题仍不明确。
2024年12月27日,中山大学孙逸仙纪念医院 宋尔卫 院士团队在 Cell 子刊 Med 上发表了题为: Targeting autophagy plus high-dose CDK4/6 inhibitors in advanced HR + HER2 - breast cancer: A phase 1b/2 trial 的临床研究论文。
这项1b/2期临床试验结果表明,对于 CDK4/6抑制剂 一线治疗失败的 晚期 HR + /HER2 - 乳腺癌 患者, 羟氯喹 (HCQ) 与大剂量 CDK4/6抑制剂 (哌柏西利) 联合用药,显示出可接受的毒性作用及有前景的治疗效果。

羟氯喹 (HCQ,一种自噬抑制剂) 曾用于防治疟疾,现在通常用于治疗类风湿性关节炎、系统性红斑狼疮等自身免疫疾病。首先,研究团队在临床前研究中证实了 羟氯喹 (HCQ) 与 大剂量 CDK4/6抑制剂 (哌柏西利) 联合用药的潜力,能够增强抗肿瘤作用,同时降低毒性作用。
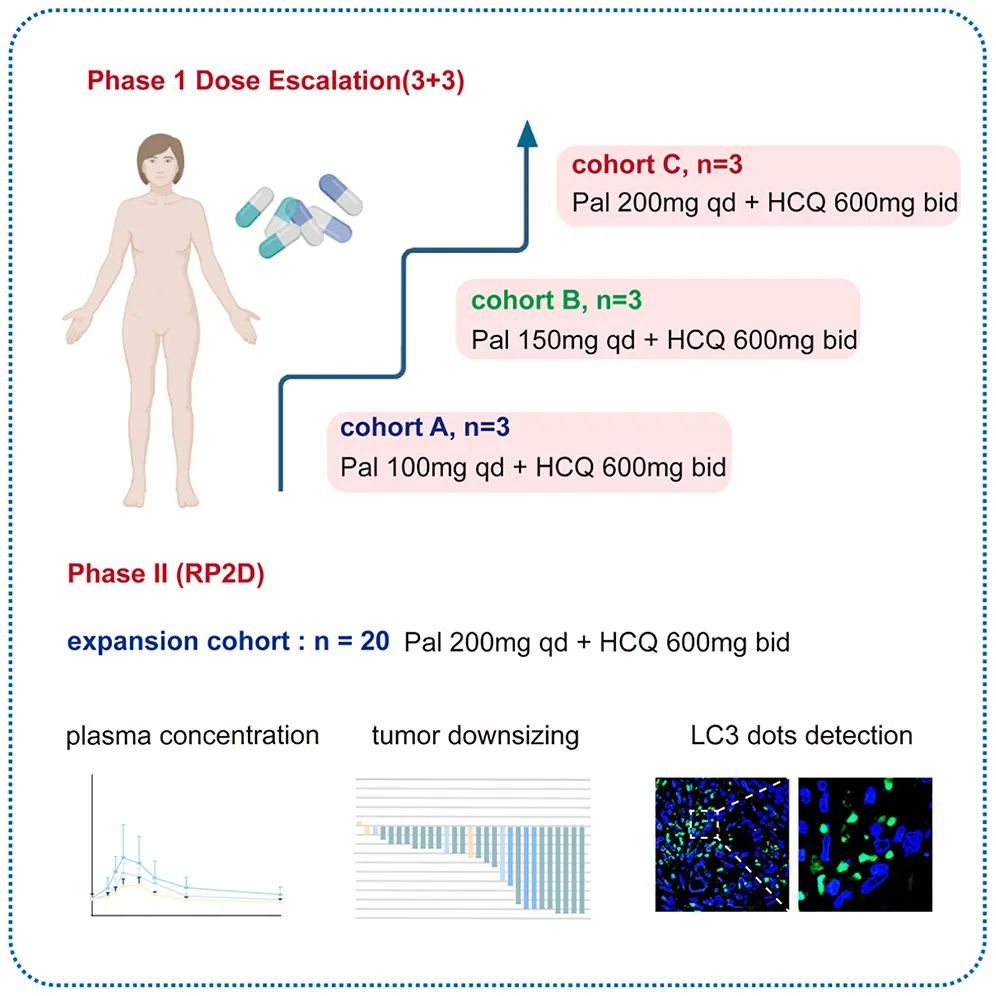
接下来,研究团队在 CDK4/6抑制剂治疗失败的 激素受体阳性/人表皮生长因子受体2阴性 (HR + /HER2 - ) 乳腺癌患者中评估了 羟氯喹+CDK4/6抑制剂联合用药的疗效和耐受性 。
-
抑癌因子PTEN被P62选择性自噬降解,加速了乳腺癌细胞对CDK4/6抑制剂的耐药; -
羟氯喹联合大剂量CDK4/6抑制剂在晚期 HR + /HER2 - 乳腺癌患者中显示出有前景的结局; -
羟氯喹联合大剂量CDK4/6抑制剂的毒性可控。
https://www.cell.com/med/abstract/S2666-6340(24)00453-7
链接:http://www.lewenyixue.com/2024/12/30/Cell%E5%AD%90%E5%88%8A%EF%BC%9A%E5%AE%8B%E5%B0%94%E5%8D%AB%E9%99%A2%E5%A3%AB%E5%9B%A2%E9%98%9F%E6%9C%80%E6%96%B0%E4%B8%B4%E5%BA%8A%E7%A0%94%E7%A9%B6/