NEJM | 贝林妥欧单抗改善新确诊标准风险B-ALL患者预后
撰文 | 周叶斌
B细胞急性淋巴细胞白血病 (B-ALL) 是最常见的儿童癌症。急性淋巴细胞白血病 (ALL)的治愈率在过去五十年中急剧增加。然而,近年来进展已经放缓,多次尝试强化传统化疗药物未能进一步提高治愈率。尽管总体治愈率很高,但复发性B-ALL仍然是儿童癌症相关死亡的主要原因。因此,仍然需要探索新的B-ALL治疗方案。
Blinatumomab(贝林妥欧单抗)是一种双特异性抗体,靶向B系细胞表面CD19抗原的同时让CD3+ T细胞重定向进行CD19选择性裂解。Blinatumomab已被证明可改善复发性B-ALL儿童的预后。过往试验表明在标准化疗中加入Blinatumomab可改善新诊断疾病成人的无复发生存率和总生存率。但加入Blinatumomab能否改善新确诊B-ALL儿童患者预后尚不清楚。
近日,多国联合研究团队在 The New England Journal of Medicine 上发表题为 Blinatumomab in Standard-Risk B-Cell Acute Lymphoblastic Leukemia in Children 的论文, 展示了一项新诊断标准风险儿童B-ALL患者3期临床试验结果。该试验中的儿童具有平均或较高的复发风险,而在联合化疗中加入 Blinatumomab 可显著提高他们的无病生存期(disease free survival)。

这项名为AALL1731的试验是一项3期随机对照试验,在澳大利亚、加拿大、新西兰和美国的多个医学中心进行,招募新诊断的标准风险B-ALL患者。所有患者均接受三种药物联合诱导治疗。诱导治疗后,标危患者根据复发风险分为三组:良好、平均和高。被归类为具有良好复发风险的患者被非随机分配接受单独标准化疗。在诱导治疗结束时,根据MRD对被归类为具有平均复发风险的患者进一步分层。检测不到MRD的患者接受单独化疗,其他患者随机分配接受单独化疗或化疗加两个非序贯周期的Blinatumomab。主要终点是无病生存期。
2019年6月到2024年6月,研究人员共招募入组4264例标危B-ALL患者。其中总共有1440名复发风险平均或较高的标准风险B-ALL患者接受了随机分组,并被纳入意向治疗疗效分析。随机分配的患者的中位年龄为 4.3 岁,52.6% 是男孩。
2024年7月,在发生了194个预期事件中的81个(41.8%)后,数据和安全监测委员会审查了第一次计划的中期疗效分析结果(数据截止日期2024年6月30日)。当时,1440 名能够接受评估的合格患者接受了随机分组(占计划接受随机分组的患者人数的 64%),中位随访时间为2.5年。
接受Blinatumomab和化疗的患者估计随机分组后3年无病生存率为 96.0±1.2%,而随机分配接受单独化疗的患者为87.9±2.1%。据此分析,标准化疗中加入Blinatumomab显著提高了无病生存期,限制性平均生存时间差异72天,95%置信区间为36-108; P<0.001),超过预先指定的停止标准(P<0.0044)。
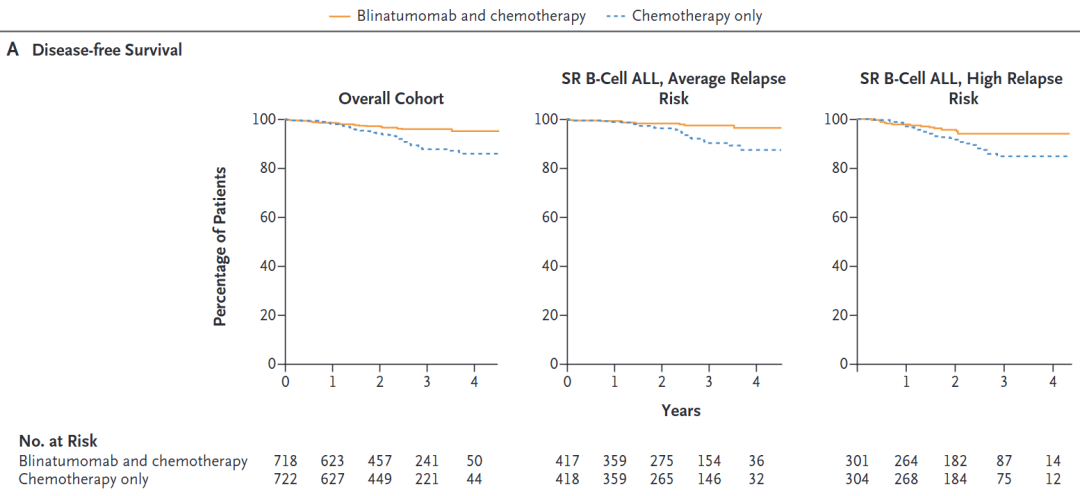
附图1. Blinatumomab联合治疗组与化疗组的无病生存差异
因此数据和安全监测委员会建议提前终止随机化。随机分组后Blinatumomab联合化疗组的估计3年总生存率为98.4±0.9%,单独化疗为97.1±1.1%。
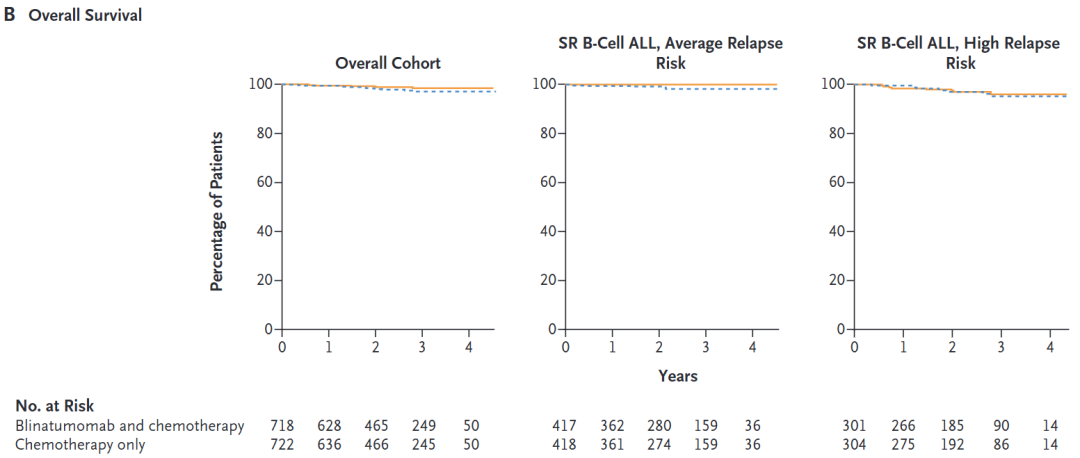
附图2. Blinatumomab联合治疗组与化疗组的总体生存率比较
按年龄、性别、白细胞计数、细胞遗传学风险组、CNS 状态、诱导治疗第8天评估的 MRD、诱导治疗结束时评估的MRD以及种族或族裔群体调整后,添加Blinatumomab 仍然显著提高了无病生存率(调整后限制性平均生存时间的差异为74天,95%CI为38 -110)。Blinatumomab联合化疗组估计的3年累积复发率为3.3±0.8%,单独化疗为11.8±1.6%。

附图3. 亚组分析下Blinatumomab联合治疗组与化疗组的比较
在具有平均复发风险的患者中,Blinatumomab联合化疗的3年无病生存率为 97.5±1.3%,单独化疗为90.2±2.3%(限制性平均生存时间差异67天,95%CI,24- 110)。
而在复发风险高的患者中,Blinatumomab联合化疗组估计3年无病生存率为 94.1±2.5%,单独化疗组84.8±3.8%(限制性平均生存时间差异79天,95% CI,17-140)。
在安全性方面,Blinatumomab联合治疗的患者更可能出现脓毒症和3级以上的导管相关感染(14.8%对5.1%,P<0.001),但4级感染性不良事件的发生率较低,不同治疗组间没有差别。而且细胞因子释放综合征、癫痫发作和3级以上脓毒症在Blinatumomab治疗周期中很少见。未来研究或许可以探索接受Blinatumomab治疗的患者是否会受益于增强的支持性治疗,降低之后出现感染类不良事件的风险。
总之,这项B-ALL标准风险儿童患者的3期临床试验显示 在标准化疗中加入Blinatumomab可显著改善无病生存期。 这种改善在各种患者、疾病特征亚组中一致。尤其值得注意的是Blinatumomab联合治疗取得的预后结果与先前在具有最有利风险特征的患者中观察到的预后相似,这为B-ALL标准风险患儿进一步改善治疗结果,降低复发风险带来了希望。
撰文

制作
排版 | 车洁 校对 | uu
▼滑动查看更多▼
Background: B-cell acute lymphoblastic leukemia (B-cell ALL) is the most common childhood cancer. Despite a high overall cure rate, relapsed B-cell ALL remains a leading cause of cancer-related death among children. The addition of the bispecific T-cell engager molecule blinatumomab (an anti-CD19 and anti-CD3 single-chain molecule) to therapy for newly diagnosed standard-risk (as defined by the National Cancer Institute) B-cell ALL in children may improve outcomes.
Methods: We conducted a phase 3 trial involving children with newly diagnosed standard-risk B-cell ALL who had an average or high risk of relapse. Patients were randomly assigned to receive chemotherapy alone or chemotherapy plus two nonsequential 28-day cycles of blinatumomab. The primary end point was disease-free survival.
Results: The data and safety monitoring committee reviewed the results from the first interim efficacy analysis, which included 1440 patients who had undergone randomization (722 to chemotherapy alone and 718 to blinatumomab and chemotherapy) and recommended early termination of randomization. At a median follow-up of 2.5 years, the estimated 3-year disease-free survival (±SE) was 96.0±1.2% with blinatumomab and chemotherapy and 87.9±2.1% with chemotherapy alone (difference in restricted mean survival time, 72 days; 95% confidence interval, 36 to 108; P<0.001 by stratified log-rank test). The estimated 3-year disease-free survival among patients with an average relapse risk was 97.5±1.3% with blinatumomab and chemotherapy and 90.2±2.3% with chemotherapy alone; among those with a high relapse risk, the corresponding values were 94.1±2.5% and 84.8±3.8%. Cytokine release syndrome, seizures, and sepsis of grade 3 or higher were rare during blinatumomab cycles, but the overall incidence of nonfatal sepsis and catheter-related infections was significantly higher among patients with an average relapse risk who had been assigned to receive blinatumomab and chemotherapy than among those assigned to receive chemotherapy alone.
Conclusions: Adding blinatumomab to combination chemotherapy in patients with newly diagnosed childhood standard-risk B-cell ALL of average or high risk of relapse significantly improved disease-free survival. (Funded by the National Institutes of Health and others; AALL1731 ClinicalTrials.gov number, NCT03914625.).
DOI: 10.1056/NEJMoa2411680
版权声明:本文为“乐问号”作者或机构在乐问医学上传并发布,仅代表该作者或机构观点,不代表乐问医学的观点或立场,不能作为个体诊疗依据,如有不适,请结合自身情况寻求医生的针对性治疗。
链接:http://www.lewenyixue.com/2024/12/18/NEJM%20%7C%20%E8%B4%9D%E6%9E%97%E5%A6%A5%E6%AC%A7%E5%8D%95%E6%8A%97%E6%94%B9%E5%96%84%E6%96%B0%E7%A1%AE%E8%AF%8A%E6%A0%87%E5%87%86/
THE END










赶快来坐沙发