STTT:复旦大学孟志强/解婧/黄胜林报道“三重阻断”联合疗法治疗晚期胆道系统肿瘤及胰腺癌的临床数据

编辑丨王多鱼
排版丨水成文
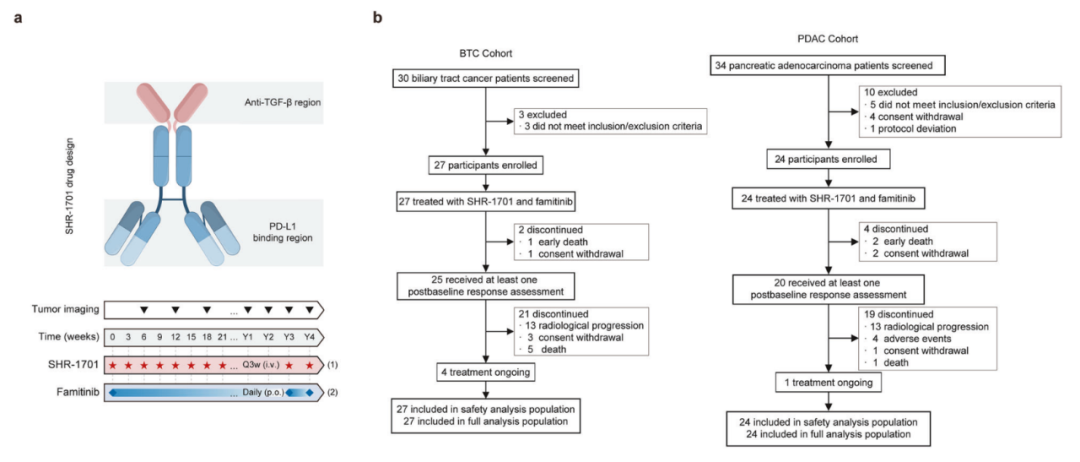
晚期 胆道系统肿瘤 (BTC) 和 胰腺导管腺癌 (PDAC) 的后线治疗选择有限,患者预后差。 SHR-1701 是一种双特异性融合蛋白,由抗PD-L1抗体与TGF-β受体II的胞外段融合而成,能同时阻断 PD-L1 和 TGF-β 信号通路。而 法米替尼 (famitinib) 则是一种口服的多靶点酪氨酸激酶抑制剂,主要抑制肿瘤血管生成相关的激酶如VEGFR2/3等。两者联用有望产生协同抗肿瘤作用。
近日,复旦大学附属肿瘤医院 孟志强 、 解婧 、 黄胜林 团队在 Signal Transduction and Targeted Therapy 发表了题为: Clinical and biomarker analyses of SHR-1701 combined with famitinib in patients with previously treated advanced biliary tract cancer or pancreatic ductal adenocarcinoma: a phase II trial 的临床研究论文。
该论文报道了双功能融合蛋白 SHR-1701 联合 法米替尼 (famitinib) ,在治疗既往一线标准治疗失败的晚期 胆道系统肿瘤 (BTC) 和 胰腺导管腺癌 (PDAC) 患者中的 II期 临床试验数据,表现出良好的疗效和安全性。
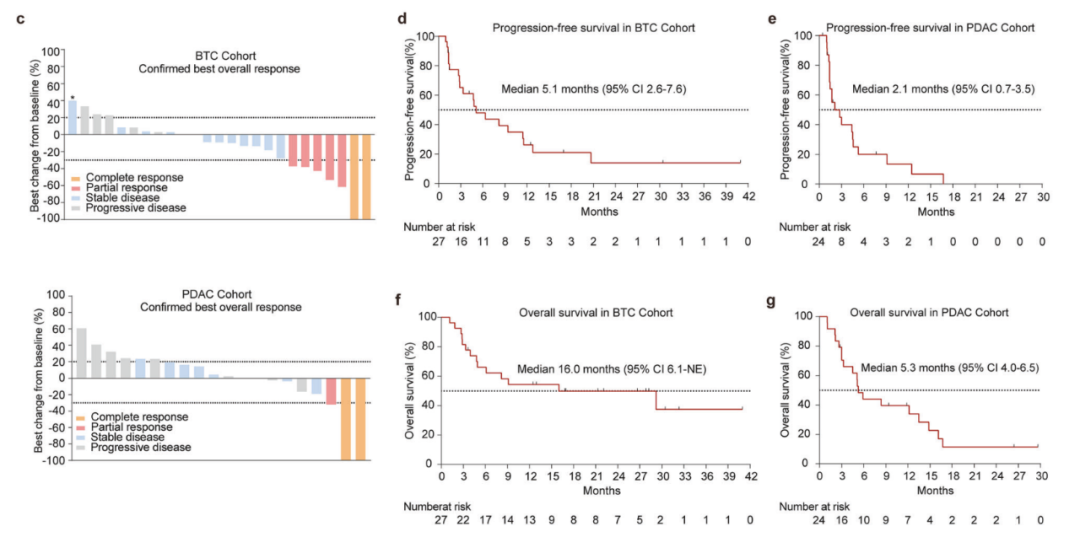
这项II期临床试验共入组了51例难治性晚期BTC和PDAC患者。结果显示,在BTC队列中,28%的患者获得客观缓解 (2例完全缓解) ,80%的患者获得疾病控制,中位无进展生存期为5.1个月,中位总生存期达16个月。而在PDAC队列中,15%的患者获得客观缓解 (2例完全缓解) ,60%的患者获得疾病控制。总体上,3-4级治疗相关不良事件发生率为29.4%,未见5级事件报告。
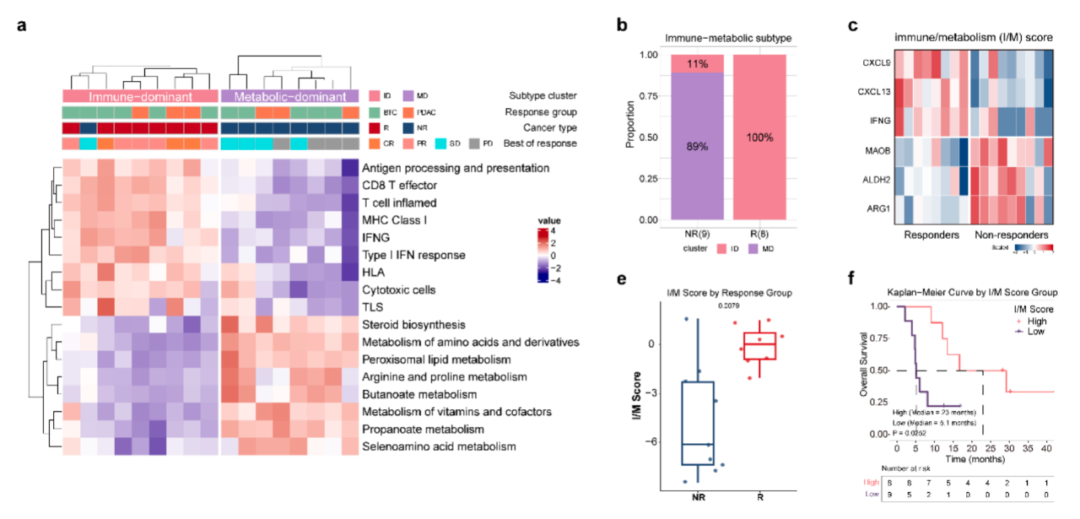
进一步探索性分析发现,既往原发灶手术切除史、外周血免疫表型变化以及独特的免疫-代谢谱特征与治疗获益相关。他们基于转录组6个基因开发的免疫/代谢评分,可在多个队列中预测免疫治疗疗效,以指导筛选最有可能从该治疗方案中获益的患者。
综上,这是该“三重阻断”的靶向治疗联合免疫治疗方案在实体瘤的初次尝试,为胆胰恶性肿瘤提供了一种潜在的新型联合治疗策略。研究团队认为, 对于未能从标准治疗中获益的患者, PD-L1 、 TGF-β 和 血管生成途径 的三重阻断有望成为他们的后线治疗选择。同时,研究团队指出,该疗法尚需在更大规模的随机对照临床试验中进一步验证。
复旦大学附属肿瘤医院中西医结合科 孟志强 教授和 解婧 教授、复旦大学生物医学研究院黄胜林研究员为论文通讯作者。复旦大学研究生 易丽夏 等为论文共同第一作者。该研究得到复旦大学肿瘤医院陈震教授、复旦大学基础医学院汪振天教授以及江苏恒瑞医药公司的大力支持。
https://www.nature.com/articles/s41392-024-02052-3
版权声明:本文为“乐问号”作者或机构在乐问医学上传并发布,仅代表该作者或机构观点,不代表乐问医学的观点或立场,不能作为个体诊疗依据,如有不适,请结合自身情况寻求医生的针对性治疗。
链接:http://www.lewenyixue.com/2024/12/16/STTT%EF%BC%9A%E5%A4%8D%E6%97%A6%E5%A4%A7%E5%AD%A6%E5%AD%9F%E5%BF%97%E5%BC%BA-%E8%A7%A3%E5%A9%A7-%E9%BB%84%E8%83%9C%E6%9E%97%E6%8A%A5/
THE END