Lancet | 疗效显著!软组织肉瘤免疫联合治疗最新结果出炉!
III期四肢和肢带软组织肉瘤 是一组多样化的间叶性恶性肿瘤,通常采用手术和放疗进行治疗。约50%的患者患有大于5厘米的高分级局限性(III期)软组织肉瘤,这些患者最终会发展为转移性疾病。一旦发生转移,患者通常接受化疗,但中位生存期仅为12–24个月。因此,极需新的治疗策略,以减少高风险局限性软组织肉瘤患者发生转移性疾病的风险。
部分转移性软组织肉瘤患者对免疫检查点抑制治疗有反应。在之前的研究中,接受抗PD-1单克隆抗体帕博利珠单抗治疗的患者中,23%未分化多形性肉瘤和10%的多形性或去分化脂肪肉瘤患者出现了客观缓解。
近日,由 David G Kirsch 团队发表于 Lancet 题为 Safety and efficacy of pembrolizumab, radiation therapy, and surgery versus radiation therapy and surgery for stage III soft tissue sarcoma of the extremity (SU2C-SARC032): an open-label, randomised clinical trial 的文章, 通过对III期未分化多形性肉瘤或脂肪肉瘤患者中随机临床试验(SU2C-SARC032), 揭示了在术前放疗和手术治疗加入帕博利珠单抗,可以显著改善III期未分化多形性肉瘤和多形性或去分化脂肪肉瘤患者的两年无病生存期,为这些患者确立了一种新的有前景的治疗选择。

SU2C-SARC032这项开放性随机临床试验中招募了年龄≥12岁、可切除的cT2N0M0(依据第7版美国癌症联合委员会分期标准定义为肿瘤>5 cm)的患者。患者招募自澳大利亚、加拿大、意大利和美国的20家学术机构。招募的143名患者里,患者按照1:1的比例随机分配至以下两组(根据肿瘤分级分层),具体分析人群见图一。
-
对照组(72名):接受术前影像引导的外照射放疗,然后进行手术。
-
实验组(71名):接受术前帕博利珠单抗联合放疗,然后进行手术,并在术后继续帕博利珠单抗治疗。
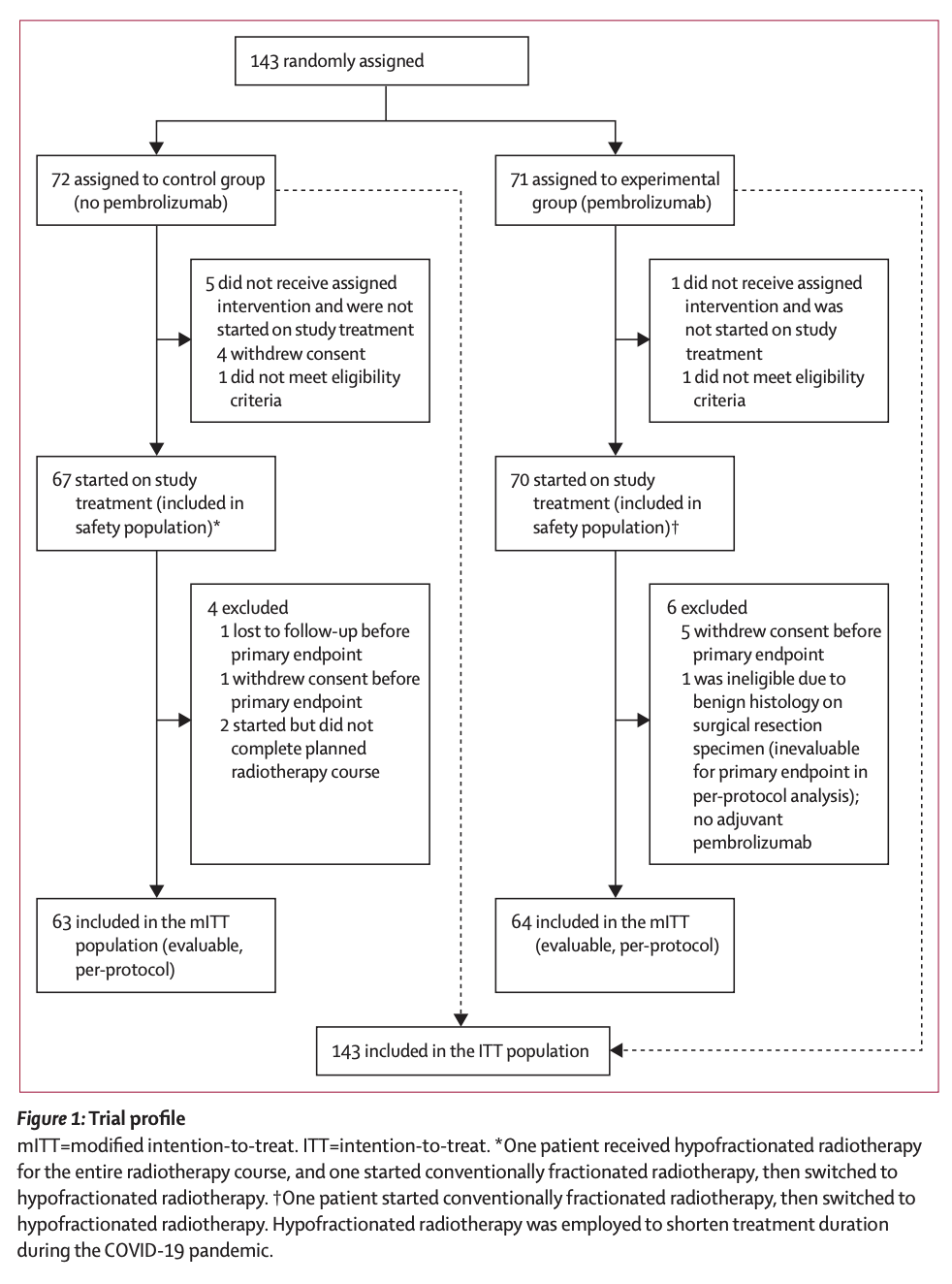
实验组患者接受帕博利珠单抗(200 mg)的静脉注射,每3周一次,共三次剂量(分别在放疗前、放疗期间和放疗后)完成后进行手术;手术安排在第3次帕博利珠单抗治疗后3至6周内进行。术后最多可继续接受14次帕博利珠单抗治疗(最多17个周期)。帕博利珠单抗的首次剂量在入组后7天内给药,放疗在入组后14天内开始(对照组)或在首次帕博利珠单抗给药后1至14天内开始(实验组)。
试验 主要研究终点是无病生存期。次要研究终点 包括远处无病生存期、局部无复发生存期、总生存期、不良事件和伤口并发症等。
127名的mITT分析患者里,共观察到 56例无病生存事件 :对照组32例, 实验组24例。 实验组的无病生存期显著优于对照组 (p=0.035,风险比(HR)= 0.61 ):实验组2年无病生存率为67% > 对照组52%。(见图二A)
该试验细分患者做亚组分析:按肿瘤分级(Grade 2 vs Grade 3)。在Grade 2组(n=42),实验组与对照组在无病生存期上无显著差异(图二B)。在 Grade 3组 (n=85), 实验组无病生存期更长,接近显著 (图二C)。次要研究终点分析发现在远处无病生存期(DDFS)和总生存期(OS),实验组表现优于对照组,虽未达到统计学显著性。
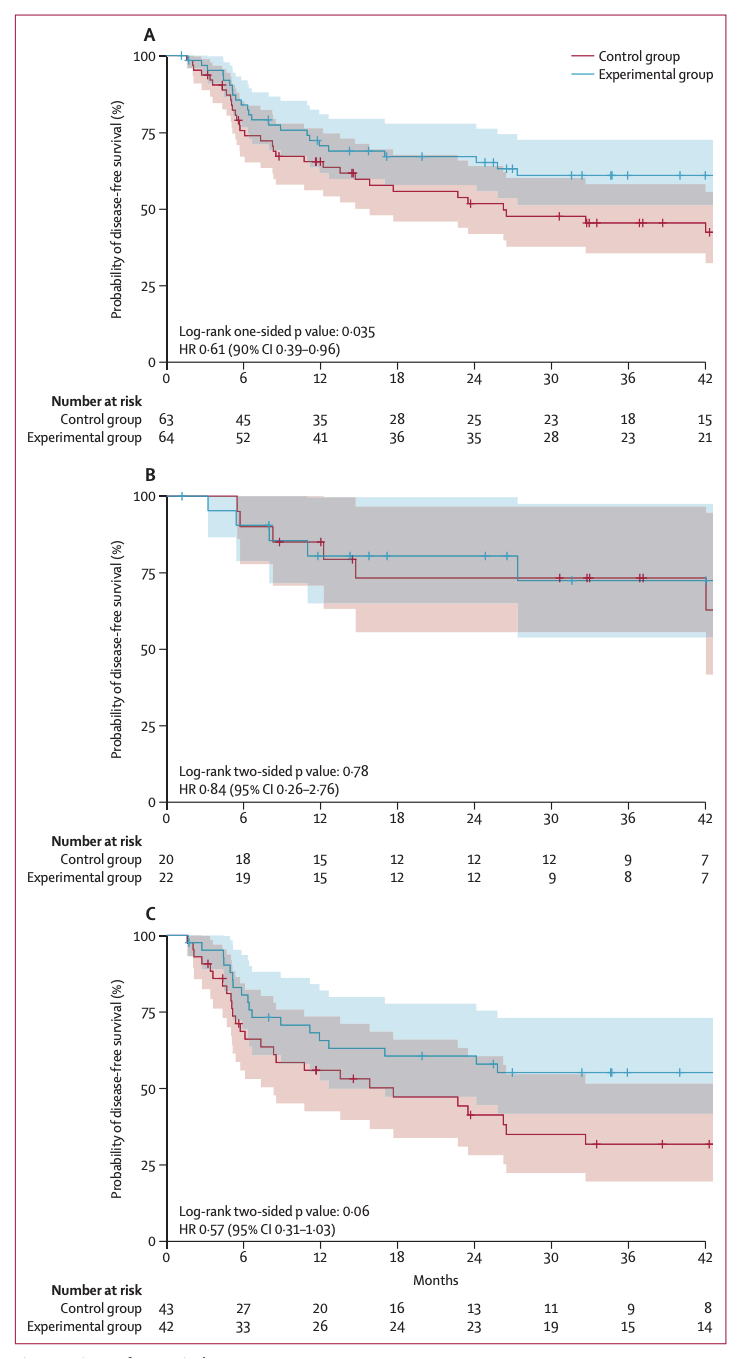
该试验接下来对于安全性和敏感性进行分析。在137名ITT分析患者里,实验组(n=70)里 有39人发生至少一次3级或4级不良事件、 33 人发生至少一次严重不良事件、54人发生与帕博利珠单抗相关的不良事件。比起对照组(n=67人)里,仅有21人发生至少一次3级或4级不良事件、 13 人发生至少一次严重不良事件 , 实验组的不良事件(特别是3级或4级不良事件和严重不良事件)发生率高于对照组,大多数与帕博利珠单抗相关。对于敏感性分析,ITT人群的分析结果与mITT人群一致(图二A),进一步支持实验组的无病生存期优势。
该试验接下来来探讨了 帕博利珠单抗的潜在作用与现有研究的比较 ;在本研究中mITT人群中没有患者接受术后辅助化疗。在之前的辅助化疗的研究中,包括迄今规模最大的研究EORTC 62931试验,分析表明辅助化疗可能改善总生存期; 在局部复发、远处复发和总生存期上的疗效仅为 边际改善 。然而,这种获益需要权衡化疗带来的短期和长期毒性。相比之下,在本试验中,新辅助和辅助帕博利珠单抗虽然导致3级或以上不良事件的发生率增加,但其急性和长期毒性特征优于以阿霉素为基础的联合化疗。结合帕博利珠单抗显著改善的无病生存期,毒性可接受性使其成为治疗高风险局限性II级或III级未分化多形性肉瘤和脂肪肉瘤患者的 有吸引力的全身治疗选择 。
虽然本研究SU2C-SARC032仍然有局限性: 样本量小,没有探讨化疗与免疫治疗的潜在相互作用 , 但其临床意义表明在高风险局限性未分化多形性肉瘤和脂肪肉瘤患者中,加入新辅助和辅助帕博利珠单抗联合术前放疗和手术,可显著改善无病生存期。 过去数十年中,这类患者的预后变化有限 ,而 SU2C-SARC032的结果提供了一个潜在的突破,为高风险软组织肉瘤患者提供了新的治疗选择,其良好的毒性特征与显著的DFS改善使其成为未来临床实践的重要补充。
撰文

责编

制作
排版 | 车洁 校对 | uu
▼滑动查看更多▼
Background:Approximately half of patients with localised, high-risk soft tissue sarcoma of the extremity develop metastases. We aimed to assess whether the addition of pembrolizumab to preoperative radiotherapy and surgery would improve disease-free survival.
Methods:We completed an open-label, randomised clinical trial in patients with grade 2 or 3, stage III undifferentiated pleomorphic sarcoma or dedifferentiated or pleomorphic liposarcoma of the extremity and limb girdle. Patients were enrolled at 20 academic institutions in Australia, Canada, Italy, and the USA. Patients were randomly assigned to preoperative radiotherapy then surgery (control group) or preoperative pembrolizumab with radiotherapy (initiated 1-14 days after the first dose of pembrolizumab) then surgery and postoperative pembrolizumab (experimental group). Pembrolizumab (200 mg intravenously every 3 weeks) was administered as three neoadjuvant cycles (before, during, and after radiotherapy) and 14 or less adjuvant cycles. Primary endpoint was disease-free survival. This study is registered with ClincialTrials.gov ( NCT03092323 ).
Findings:Between Nov 18, 2017, and Nov 14, 2023, 143 participants were randomly assigned to treatment. A modified intention-to-treat analysis of 127 patients with median follow-up of 43 months showed that the experimental group (n=64) had significantly longer disease-free survival than the control group (n=63; log-rank one-sided p=0·035; hazard ratio [HR] 0·61; 90% CI 0·39-0·96). The 2-year disease-free survival increased by 15% with addition of pembrolizumab: 52% (90% CI 42-64) and 67% (90% CI 58-78) for the control and experimental groups, respectively. Disease-free survival was similarly improved with pembrolizumab for the intention-to-treat patient population (HR 0·61 [90% CI 0·39-0·95]). Grade 3 or higher adverse events occurred more frequently in the experimental group (56%) than the control group (31%).
Interpretation:Addition of pembrolizumab to preoperative radiotherapy and surgery improves disease-free survival for patients with stage III undifferentiated pleomorphic sarcoma and pleomorphic or dedifferentiated liposarcoma of the extremity, which establishes a promising new treatment option for these patients.
Funding:Stand Up to Cancer and Merck Sharp & Dohme.
DOI: 10.1016/S0140-6736(24)01812-9
 点击此处,直达原文
点击此处,直达原文
版权声明:本文为“乐问号”作者或机构在乐问医学上传并发布,仅代表该作者或机构观点,不代表乐问医学的观点或立场,不能作为个体诊疗依据,如有不适,请结合自身情况寻求医生的针对性治疗。
链接:http://www.lewenyixue.com/2024/12/07/Lancet%20%7C%20%E7%96%97%E6%95%88%E6%98%BE%E8%91%97%EF%BC%81%E8%BD%AF%E7%BB%84%E7%BB%87%E8%82%89%E7%98%A4%E5%85%8D/
THE END
 点击此处,直达原文
点击此处,直达原文 









赶快来坐沙发