前沿分享 | 基于深度学习技术的多模态响应预测病理完全缓解在乳腺癌新辅助治疗中的应用
分享者导读
近日, Nature Communications杂志刊登了题为“An explainable longitudinal multi-modal fusion model for predicting neoadjuvant therapy response in women with breast cancer”的研究,这篇文献介绍了一种多模态响应预测(MRP)系统的新模型,该模型利用深度学习对女性乳腺癌患者的新辅助治疗(NAT)反应进行预测。MRP系统通过整合跨模态知识挖掘和时间信息嵌入策略,处理缺失模态数据,并适应不同的NAT临床场景。该研究通过多中心研究和多国乳腺放射科专家研究验证了MRP系统的稳健性,并发现其在预测病理完全缓解(pCR)方面的性能优于放射科医生。此外,该系统在处理缺失模态数据和适应不同NAT场景方面表现出了较强的适应性,对于NAT的选择和确定手术范围有一定指导意义。研究结果支持MRP系统在真实世界临床环境中的潜在应用,为乳腺癌治疗的个性化管理提供了新的工具。
研究背景和目的
乳腺癌作为全球女性中最常见的癌症,其新辅助治疗(NAT)是否达到病理完全缓解(pCR)是评估治疗效果和预测患者预后的关键指标。然而,准确评估NAT在不同治疗阶段的响应是一个复杂任务。尽管已有研究探索了血清学或遗传生物标志物来预测pCR,但这些方法因成本高和大规模验证有限而未广泛用于临床实践。此外,基于深度学习的模型在预测pCR方面显示出潜力,但现有研究往往忽视了对临床路径实际情况的适应性,以及在不同医疗中心的实用性和整体泛化能力。因此,该研究提出了基于深度学习技术的多模态响应预测(MRP)系统,旨在通过整合放射学、组织病理学、临床和个人多模态信息,模拟现实世界中医生对NAT反应的评估,并在多中心和多国乳腺放射科专家研究中验证了其稳健性,以提高预测pCR的准确性,并可能对NAT的临床决策产生深远影响。
研究方法和数据集
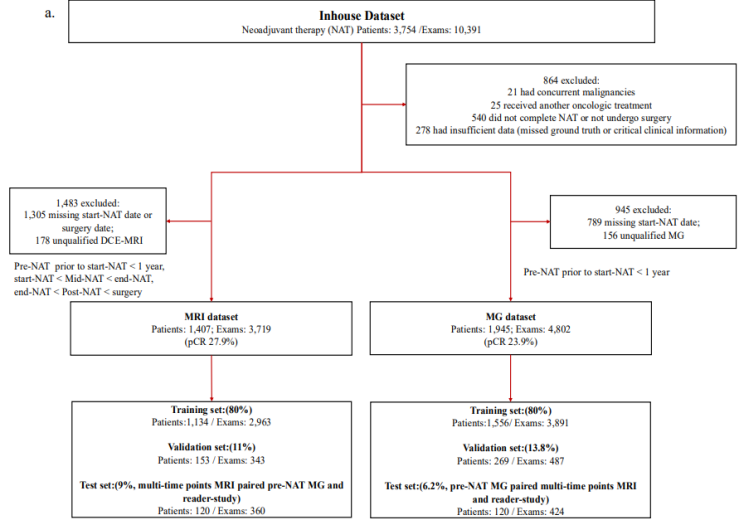
(1)数据集(见图1、图2):
图1 内部数据集处理流程图
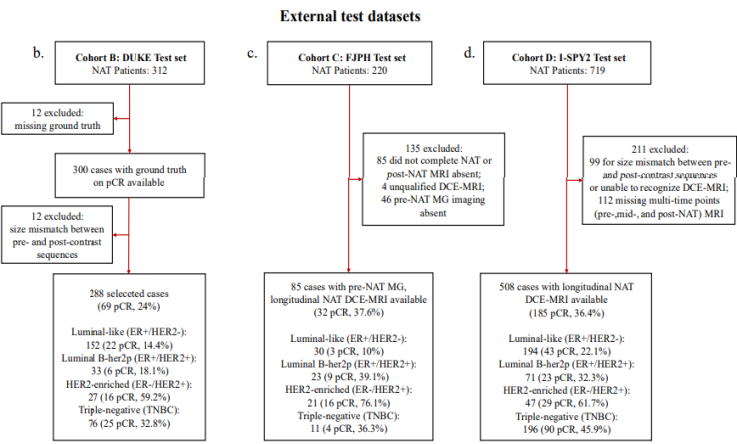
图2 外部数据集处理流程图
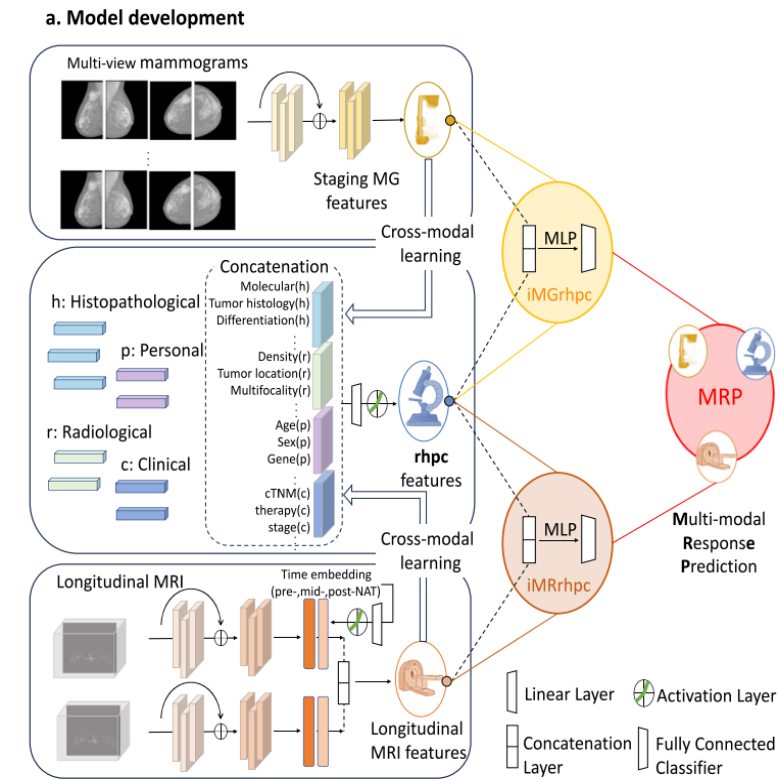
(2)模型的开发(见图3):
图3 模型开发示意图
(3)评估模型性能:
研究结果与结论
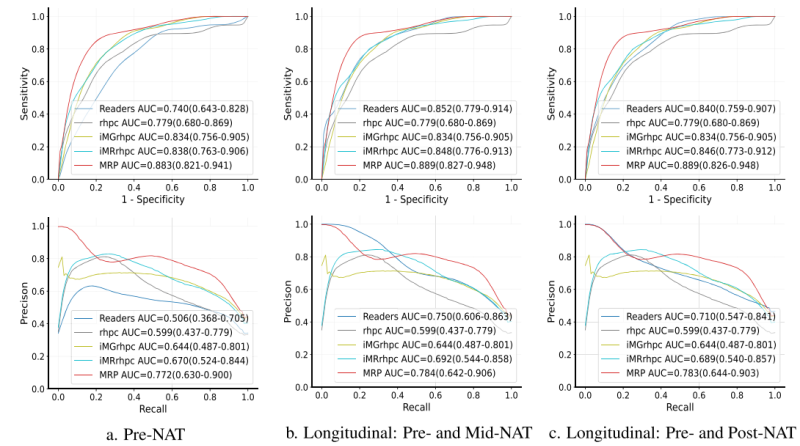
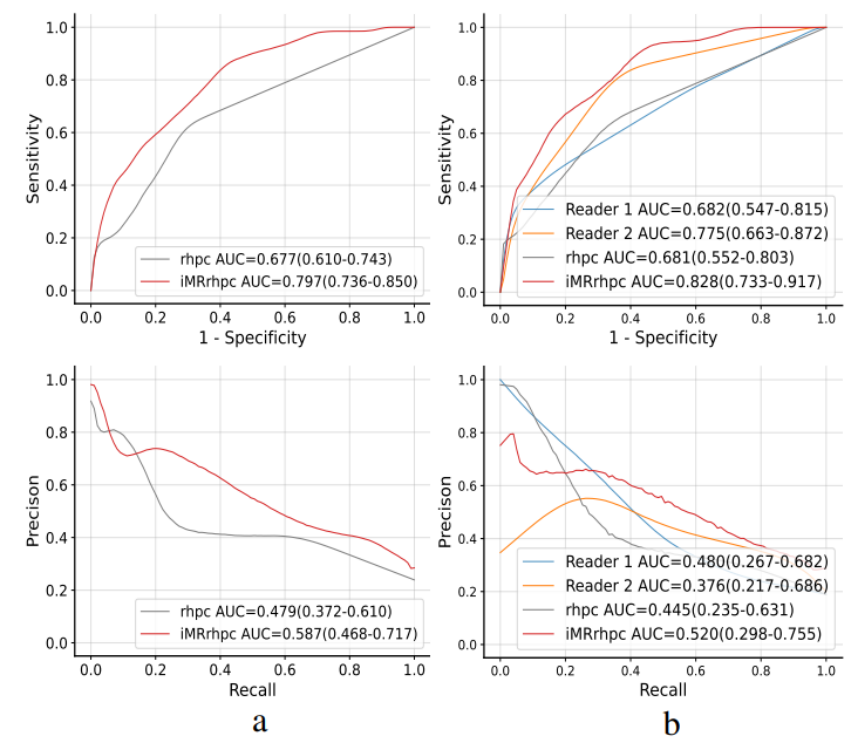
(1)MRP系统在预测pCR方面表现出与乳腺放射科医生相当的鲁棒性,并在Pre-NAT阶段的预测中优于人类,ΔAUROC在内部和外部数据集上分别提高了14% (图4) 和10% (图5) ;
图5 在外部测试集B上基线模型与iMRrhpc模型以及两个放射科专家在Pre-NAT阶段的表现
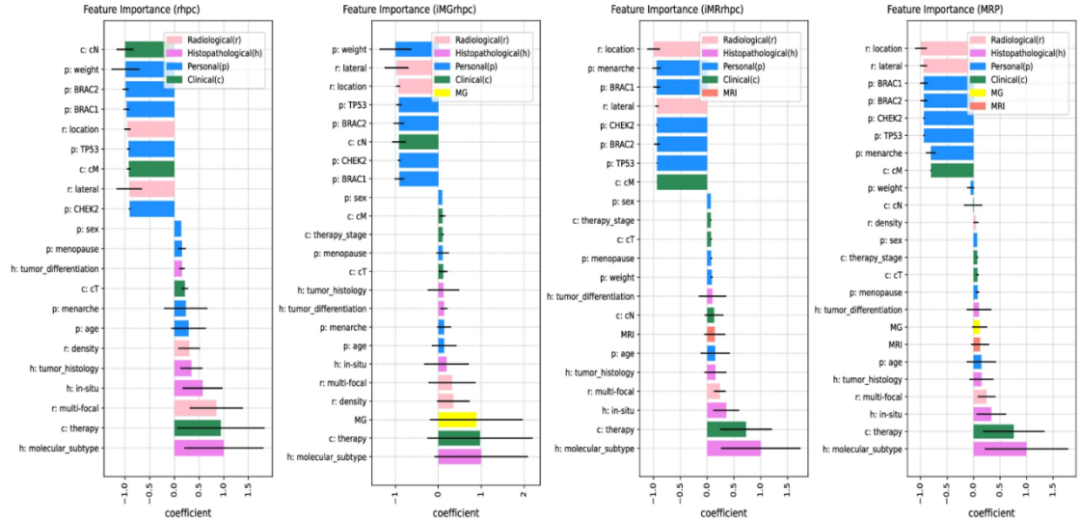
图6 模态贡献分析
研究启发
(1)研究者可以探索更多种类的多模态数据(如数字病理切片、超声等)在乳腺癌治疗反应预测中的应用,以提高模型的准确性和泛化能力;
(2)未来可开展前瞻性临床试验来验证MRP模型的临床效果,特别是在不同人群和医疗环境中的适用性;
(3)进行经济学评估,分析引入MRP模型可能带来的成本效益,为医疗决策提供更多维度的支持;
(4)研究如何使MRP模型能够适应新的治疗策略和不断变化的临床实践,保持模型的时效性和相关性。
这些启发不仅有助于推动乳腺癌治疗预测模型的发展,也为其他癌症类型和疾病领域的研究提供了新的思路和方法。

文献来源:
Gao,Y. , Ventura-diaz,S. , Wang,X. , He,M. , Xu,Z. , Weir,A. , Zhou,H. , Zhang,T. , Van duijnhoven,F.H. ,& Han , L.(2024).An explainable longitudinal multi-modal fusion model for predicting neoadjuvant therapy response in women with breast cancer.Nature Communications,15(1),. https://doi.org/10.1038/s41467-024-53450-8
原文链接:
https://www.nature.com/articles/s41467-024-53450-8

分享者简介

魏梦姣
本硕就读于山东大学齐鲁医学院—临床医学5+3一体化专业(研究方向为甲状腺乳腺疾病的临床及基础研究); 博士在读于重庆大学智能肿瘤学教育部医药基础研究创新中心(研究方向为乳腺肿瘤学)。 曾参与省重点研发项目,目前已发表文章2篇,以第一作者身份发表文章1篇。
编辑|曾海蓉 李劲
链接:http://www.lewenyixue.com/2024/12/03/%E5%89%8D%E6%B2%BF%E5%88%86%E4%BA%AB%20%7C%20%E5%9F%BA%E4%BA%8E%E6%B7%B1%E5%BA%A6%E5%AD%A6%E4%B9%A0%E6%8A%80%E6%9C%AF%E7%9A%84%E5%A4%9A%E6%A8%A1%E6%80%81%E5%93%8D/








赶快来坐沙发