Nature万字综述:癌细胞代谢与抗肿瘤免疫
越来越多的证据表明,恶性细胞的代谢重组不仅提供癌细胞更强的增殖潜力和更好的适应不利微环境条件的能力,还通过促进癌细胞的免疫逃避来促进肿瘤的发生发展。今天小编给大家带来 2024年4月22日发表在Nature 上的高分综述解读,在本文中,作者回顾了癌细胞内在和外在的机制,这些机制通过恶性细胞代谢的改变干扰先天和适应性免疫功能,从而支持疾病进展的加速。此外,该综述还讨论了如何针对这些改变以增强抗癌免疫用于治疗目的的潜力。

鉴于这是一篇全文一万+字数的宝藏综述,小编准备了目录供小伙伴们参考,以方便查询阅读!
目录
一、背景
二、葡萄糖、乳酸和三羧酸循环
(1)葡萄糖
(2)乳酸
(3)三羧酸循环
三、脂质代谢
(1)脂肪酸氧化
(2)脂质合成
(3)类二十烷酸合成
四、其他代谢通路
(1)核苷酸
(2)谷氨酰胺
(3)蛋氨酸
(4)色氨酸
(5)赖氨酸
五、靶向代谢干预手段
(1)葡萄糖和乳酸靶点
(2)谷氨酸靶点
(3)色氨酸靶点
(4)核苷酸靶点
(5)脂肪酸靶点
(6)类二十烷酸靶点
背景
恶性转化和肿瘤进展伴随着许多代谢途径的改变,这些改变出现于至少三种不同概念(但不互相排斥)的情景中。
-
第一,代谢物可能因酶编码基因的突变而积累,这些突变是肿瘤发生的主要驱动因素。例如,异柠檬酸脱氢酶(NADP+)1(IDH1)或IDH2的功能获得突变常见于患有胶质母细胞瘤(GBM)和白血病的患者,这会导致2-羟基戊二酸(2HG)的积累,这种物质具有真正的肿瘤促进活性。
-
第二,驱动肿瘤发生的已确立的癌蛋白或癌抑制因子的遗传或表观遗传改变也可以直接影响代谢。实际上,多个癌症起始事件,如KRAS的激活突变和肿瘤蛋白p53(TP53)的遗传或表观遗传失活,已被证明直接影响分解代谢或合成代谢。
-
第三,癌细胞在肿瘤进展过程中响应微环境条件的时空变化而获得代谢改变,而这些改变是肿瘤内和肿瘤间异质性的主要驱动因素之一。例如,位于血管不近旁的恶性细胞通过缺氧诱导因子1α(HIF1α)来应对缺氧,进行全球代谢重组。
癌症代谢领域由德国生理学家奥托·H·沃伯格在一个世纪前启动,他观察到恶性细胞摄取的葡萄糖比正常细胞更多。该领域揭示了恶性转化和肿瘤进展涉及超越所谓“沃伯格效应”的细胞范围内的代谢重组。
实际上,癌细胞通常表现出复杂的代谢改变,这些改变还影响氧化磷酸化(OXPHOS)、三羧酸循环(TCA循环)、多条生物合成级联反应和诸如自噬等全局分解代谢途径。这些改变通常还涉及肿瘤基质,为恶性细胞提供了所需的代谢底物,以促进细胞生长和分裂,包括(但不限于)核苷酸、脂类和氨基酸。此外,绝大多数(如果不是全部的话)癌细胞的代谢重组使其具备了更强的适应变化微环境条件的能力,从而促进了肿瘤的进化和多样化。
越来越多的数据表明,恶性细胞中的代谢变化也能抵消宿主-肿瘤共同进化中的一个主要选择压力,即抗癌免疫监视。事实上,现在广泛接受的观点是,肿瘤发生不仅是由支持恶性肿瘤的遗传和/或表观遗传改变驱动的癌细胞内在现象,还涉及显著的癌细胞外在成分,驱动癌细胞获得表型、分泌和行为特征,使其能够逃避宿主免疫系统的识别和杀伤。
葡萄糖、乳酸和三羧酸循环
癌细胞为了满足自身增加的能量需求,其通常表现出加速和多样化的生物能量代谢,包括通过糖酵解增加葡萄糖流量以及三羧酸循环的改变。所有这些代谢变化都会对肿瘤靶向免疫反应产生影响(图1)。
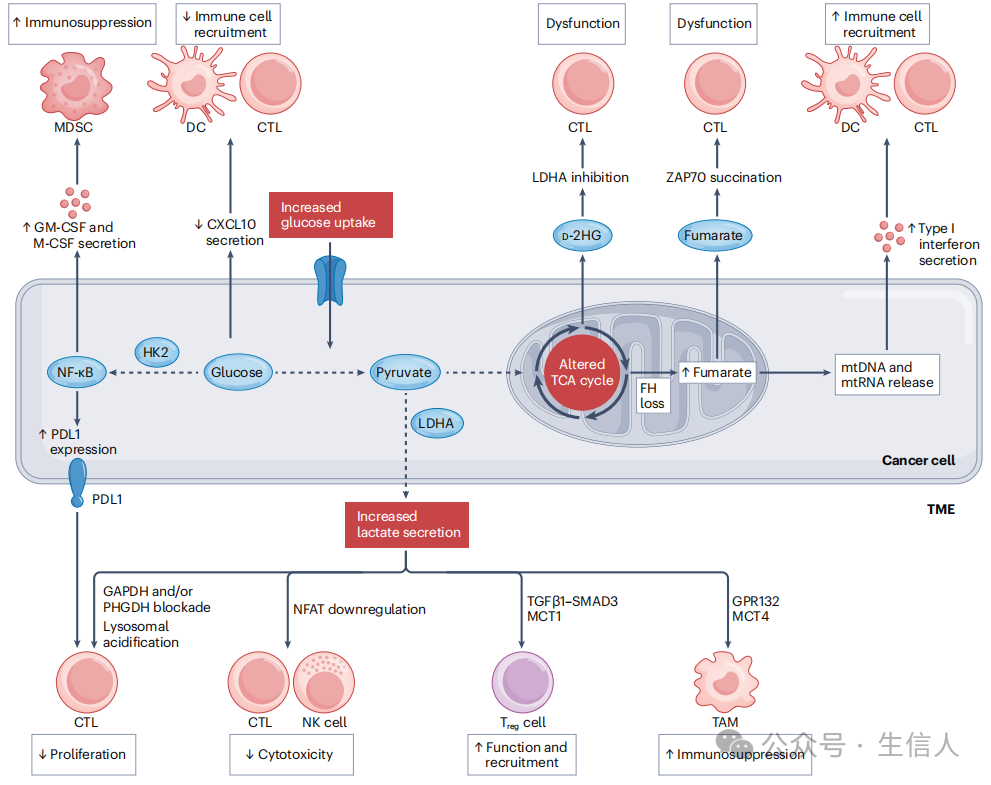
图1. 葡萄糖、乳酸和三羧酸循环对抗肿瘤免疫的影响
(1)葡萄糖
恶性细胞将葡萄糖用于生物能量目的,包括转换为丙酮酸、线粒体摄取和进入三羧酸循环(TCA循环),以及通过戊糖磷酸途径和丝氨酸合成途径用于合成代谢目的。 因此,在某些恶性肿瘤中,癌细胞可能与肿瘤微环境(TME)中的免疫细胞,特别是CD8+细胞毒性T淋巴细胞(CTL),在葡萄糖摄取方面存在竞争,正如在免疫健全的小鼠肉瘤模型中所显示的。然而,似乎免疫细胞通常比癌细胞消耗更多的葡萄糖,并且对TME中恶性与免疫区室而言,谷氨酰胺(一种可作为TCA循环的替代底物的氨基酸)而非葡萄糖本身是限制性营养素。黑色素瘤细胞中增加的糖酵解流量与涉及CTL招募的趋化因子(如CXC趋化因子配体10(CXCL10))的表达减少相关。与这一观察一致的是,糖酵解的基因特征与黑色素瘤和非小细胞肺癌(NSCLC)患者的免疫细胞浸润呈负相关,尤其是在对过继性T细胞转移无反应的患者中。
此外,肿瘤细胞增加的葡萄糖摄取与六磷酸己糖激酶2(HK2)依赖的NF-κB介导的转录反应的激活相关,这在胶质母细胞瘤(GBM)模型中导致了PDL1(也称为CD274)的表达,PDL1是T细胞上PD1的共同抑制配体。最后,增加的糖酵解流量与三阴性乳腺癌(TNBC)细胞中巨噬细胞集落刺激因子(M-CSF,也称为CSF1)和粒细胞-巨噬细胞集落刺激因子(GM-CSF,也称为CSF2)的过表达相关,这导致TME重新极化为由骨髓来源的抑制细胞(MDSC)主导的免疫抑制状态。有趣的是,在来自METABRIC公共数据集的TNBC患者中,乳酸脱氢酶A(LDHA,这种酶编码厌氧糖酵解的最终酶,将丙酮酸从线粒体摄取转换为乳酸并分泌)表达增加的患者发现其基因特征与MDSC相关的基因特征丰富,与代表T细胞浸润的基因特征低代表性相关,这些患者的疾病预后较差。
与糖酵解在癌细胞中的免疫抑制作用一致,几种抑制糖酵解的药理或遗传策略已被证明具有免疫刺激作用,并在临床前肿瘤模型中至少部分恢复免疫监视。例如,通过删除编码质膜葡萄糖通道的Glut1(也称为Slc2a1)或编码催化葡萄糖-6-磷酸和果糖-6-磷酸相互转化的异构酶的Gpi1,遗传抑制小鼠路易斯肺癌细胞和小鼠胰腺癌(Panc02)细胞中的糖酵解,已被证明增加了恶性细胞对CTL的敏感性。在机制上,这种免疫敏感化是由于增加了氧化磷酸化(OXPHOS)和过度产生的活性氧(ROS),以及对肿瘤坏死因子(TNF)驱动的细胞死亡的敏感性增加所致。
总之,癌细胞的葡萄糖代谢可能对肿瘤微环境(TME)具有免疫抑制作用。值得注意的是,葡萄糖依赖的免疫抑制至少部分来源于乳酸的分泌,这可能比糖酵解本身更适合作为治疗干预的靶点。
(2)乳酸
乳酸在大多数实体肿瘤中丰富,不仅具有“滋养功能”,还引发多种免疫抑制机制。 例如,乳酸已被证明在黑色素瘤和结直肠癌(CRC)的小鼠移植模型中,通过限制丙酮酸羧化酶补充三羧酸循环中间体来抑制CTL介导的细胞毒性,这导致丙酮酸脱氢酶活化、琥珀酸分泌减少,从而通过琥珀酸受体1减少促炎性自分泌和旁分泌信号传导。
乳酸还通过阻止甘油醛-3-磷酸脱氢酶(GAPDH)和磷酸甘油酸脱氢酶(PHGDH)的活性,抑制效应T细胞增殖,导致GAPDH后的糖酵解中间体和丝氨酸水平减少,以及促进溶酶体酸化,干扰二酰甘油依赖的蛋白激酶Cθ信号传导。与此概念一致的是,在免疫健全的同系宿主中皮下建立的LDHA缺乏B16黑色素瘤小鼠,乳酸分泌水平降低,其生长速度比其野生型对照慢。这些肿瘤的免疫控制增加与干扰素-γ(IFNγ)产生的CTL和自然杀伤(NK)细胞的浸润增加相关。
与上述发现相反,高剂量、每日腹腔内注射乳酸已被证明可以控制在免疫健全的同系小鼠中皮下建立的小鼠I3TC乳腺癌和MC38结直肠癌的生长。此外,据报道,皮下注射乳酸在免疫健全的同系小鼠中引发CTL依赖的MC38肿瘤控制,这归因于CD8+ T细胞干性的增加。这些后来的发现表明,乳酸对抗癌免疫的不利影响可能至少部分是由乳酸依赖的TME酸化引起的。
与效应T细胞相反,CD4+CD25+FOXP3+调节性T细胞对乳酸的抗增殖作用显著耐受,至少部分是由于FOXP3引发的代谢重编程,这种重编程抑制活性糖酵解,转而支持NADH氧化和氧化磷酸化(OXPHOS)。Treg细胞似乎通过溶质载体MCT1(也称为SLC16A1)大量摄取细胞外乳酸,在小鼠黑色素瘤和结直肠癌(CRC)的免疫健全模型中,通过一种依赖核因子活化T细胞细胞质1(NFATC1)的机制,导致程序性死亡受体1(PD1)表达增加。在相同的模型中,以及在可移植的头颈部鳞状细胞癌模型中,MCT1表达似乎是肿瘤内(而非循环)Treg细胞保持其免疫抑制和促肿瘤功能所必需的,至少部分反映了细胞内乳酸积累促进ezrin乳酸化,从而通过SMAD3支持免疫抑制性转化生长因子-β1(TGFβ1)信号传导。值得注意的是,组蛋白乳酸化也被认为在可移植的小鼠黑色素瘤(B16)、可移植的结直肠癌(MC38)以及致癌物诱导的小鼠CRC的髓样区室中介导免疫抑制和因此的促肿瘤效应。然而,这些观察结果的转化相关性仍需定义。
有趣的是,在天然糖酵解或经过基因工程改造以增加糖酵解的小鼠黑色素瘤、肝细胞癌和结直肠癌中,PD1阻断积极促进Treg细胞的免疫抑制活性,因此没有治疗效果,这种抗性表型可以通过药理学或遗传抑制LDHA以降低乳酸水平成功逆转。相比之下,糖酵解活性降低的小鼠三阴性乳腺癌(TNBC)已被证明对特异性细胞毒性T淋巴细胞相关蛋白4(CTLA4)的免疫检查点抑制剂(ICIs)有反应,这与肿瘤浸润Treg细胞的不稳定化及其向分泌TNF和IFNγ的效应样状态转变有关。然而,细胞外乳酸与葡萄糖可用性对这些后续观察结果的相对贡献仍需明确定义。
值得注意的是,乳酸对肿瘤内髓样细胞也有影响。例如,乳酸似乎通过G蛋白偶联受体132(GPR132)向肿瘤相关巨噬细胞(TAMs)传递信号,导致它们重新极化为免疫抑制的“M2样”表型,这种表型与小鼠TNBC模型中增加的转移扩散相关。支持这些临床前观察结果的临床相关性研究表明,在一组TNBC患者中,GPR132水平与M2样TAMs的遗传特征、增加的转移扩散和不良疾病结果呈正相关。在由丝氨酸/苏氨酸激酶11(Stk11)缺失驱动的肺癌临床前模型中也得到了类似的结果,尽管在这种情况下,细胞外乳酸在溶质载体MCT4(也称为SLC16A4)过表达下游积累,并似乎通过GPR81(也称为HCAR1)向TAMs(和CTLs)传递信号。尽管导致这种明显差异的原因尚未阐明,但不同肿瘤(如TNBC和肺癌)中浸润的TAMs可能表达不同的乳酸敏感受体或其信号传导因子的可能性是合理的,这反映了TAMs的一般异质性的公认现象。
总之,这些观察结果表明,失调的葡萄糖代谢至少部分地通过肿瘤内乳酸的积累产生免疫抑制效应。
(3)三羧酸循环
三羧酸循环(TCA循环)在细胞代谢中起着至关重要的作用,不仅提供用于氧化磷酸化(OXPHOS)的NADH和琥珀酸等还原当量,还调节许多具有代谢和信号功能的代谢物库,如乙酰辅酶A、柠檬酸、富马酸、α-酮戊二酸(α-KG)和琥珀酸本身。
毫不奇怪,这些代谢中间产物中的许多也具有直接或间接的免疫调节作用。例如,无论糖酵解是否发生潜在变化,缺乏TCA循环酶富马酸水合酶(FH)的小鼠B16黑色素瘤具有增加的肿瘤内富马酸水平,导致T细胞受体相关蛋白激酶70(ZAP70)ζ链的非酶促琥珀酸化,进而导致急性T细胞功能障碍。此外,工程化的CD19特异性嵌合抗原受体(CAR)T细胞过表达FH已被证明在免疫缺陷小鼠中对人类表达CD19的白血病细胞具有增加的治疗效力。在遗传性平滑肌瘤病和肾细胞癌的临床前模型中,FH的丧失也通过一种依赖分拣连接蛋白9(SNX9)的机制使线粒体网络不稳定,促进含有线粒体核酸的小囊泡的释放。在这种情况下,线粒体DNA(mtDNA)和线粒体RNA(mtRNA)释放到细胞质中,显示通过激活DNA传感环磷酸鸟苷-腺苷合成酶(cGAS)-干扰素反应cGAMP交互因子1(STING1)通路和RNA传感视黄酸诱导基因I(RIG-I)来驱动I型干扰素分泌。干扰素分泌促进了免疫细胞向肿瘤的募集,但也可能导致慢性炎症反应,在免疫监视受损的情况下可能支持致癌作用。
最近的研究表明,通过介导氧化磷酸化(OXPHOS)的线粒体呼吸复合体中的正常电子流动能够限制细胞毒性T淋巴细胞(CTLs)识别黑色素瘤细胞。这种免疫抑制效应源于呼吸复合体II将琥珀酸转化为富马酸的能力,从而防止了一种琥珀酸依赖的表观遗传机制的激活,该机制会导致癌细胞上调MHC I类分子和其他抗原呈递机制的成分。这些发现表明,在肿瘤进化过程中,一些癌细胞中可能出现的线粒体电子流动缺陷可能会增加抗原呈递,从而成为宿主免疫系统负选择压力的靶点。
尽管如此,小鼠三阴性乳腺癌(TNBC)细胞中的琥珀酸积累,由肿瘤相关巨噬细胞(TAM)分泌的TGFβ1驱动,被证明可以促进糖酵解,从而导致总体上免疫抑制的表型。尽管这种琥珀酸在免疫刺激或免疫抑制效应之间表面上存在矛盾的原因尚未明确,但可能存在特异于肿瘤的机制,超越了糖酵解,解释了琥珀酸积累在TNBC而非黑色素瘤细胞中的免疫抑制效应,可能包括琥珀酸依赖的HIF1α的积累。
2HG(2-羟基戊二酸)在结构上与三羧酸循环(TCA循环)中间产物α-酮戊二酸(α-KG)相似,通过表观遗传机制具有真正的致癌功能,尤其是(但不仅限于)通过抑制多种α-KG依赖的二氧化酶、脯氨酸羟化酶和组蛋白去甲基化酶。此外,2HG的d-对映体(而不是其l-对映体)可以被肿瘤浸润的淋巴细胞主动摄取,导致免疫能力正常的小鼠黑色素瘤和结直肠癌(CRC)模型中剂量依赖性和完全可逆的增殖和效应功能(包括IFNγ分泌)的抑制。这种免疫抑制效应至少部分源于d-2HG抑制乳酸脱氢酶A(LDHA)的能力,导致向氧化磷酸化(OXPHOS)的代谢转变,驱动线粒体对丙酮酸的摄取增加和NAD+与NADPH比率的降低,并破坏NFATC1活性和多胺合成。
相比之下,另一种抑制α-KG依赖二氧化酶的代谢中间产物戊二酸显示出对T细胞功能的正面效应而非负面效应。具体来说,使用细胞可渗透的戊二酸前体乙二酯戊二酸与增加小鼠B16黑色素瘤和SKOV3卵巢癌细胞下游T细胞介导的细胞毒性有关,这是由于丙酮酸脱氢酶的戊酰化及其对OXPHOS的抑制,转而有利于厌氧糖酵解。这些发现指出戊二酸代谢作为改善T细胞依赖的抗癌免疫反应的潜在靶点。值得注意的是,TCA循环中间产物反酸也同样在多种细胞类型中,包括免疫细胞中具有一系列免疫抑制作用。实际上,细胞可渗透的反酸前体依赖的NFE2样bZIP转录因子2(NFE2L2;最常被称为NRF2)的激活已被证明在培养的人类NSCLC A549细胞中通过STING1激活下游抑制I型干扰素反应。然而,癌细胞来源的反酸对携带同基因肿瘤的免疫能力正常的小鼠抗癌免疫反应的确切影响仍有待正式研究。
总结来说,多种与癌症相关的代谢改变,包括葡萄糖、乳酸和TCA循环,已被证明会引发微环境扰动,进而对免疫监视产生负面影响。
脂质代谢
癌变细胞的增殖显著依赖于增强的脂质代谢,这不仅为通过脂肪酸氧化(FAO)驱动的氧化磷酸化(OXPHOS)提供额外的能量来源,还作为细胞膜和其他脂质的来源,下游是脂肪酸合成。与癌症相关的FAO和脂肪酸合成的改变会影响肿瘤靶向的免疫反应(图2)。
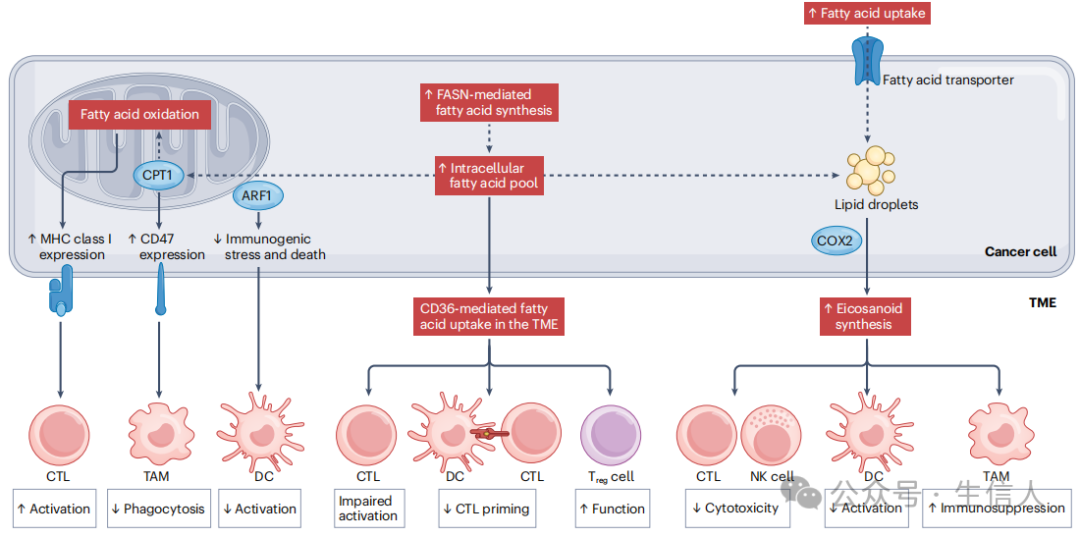
图2. 脂肪酸代谢对抗癌免疫的影响
(1)脂肪酸氧化
FAO(脂肪酸氧化)由长链脂肪酸的分解代谢成乙酰辅酶A组成,作为TCA循环的底物以提供OXPHOS的能量。多种癌症类型如GBM(胶质母细胞瘤)具有增加的FAO速率,这支持了疾病的进展。在这种情况下,多种FAO相关酶如肉碱棕榈酰转移酶1A(CPT1A)、CPT2和酰基辅酶A脱氢酶家族成员9(ACAD9)的上调似乎与GBM细胞膜上“不要吃我”信号CD47的暴露增加一起发生。这导致髓系细胞吞噬作用的强效抑制和放射抗性,机制上反映了FAO衍生的乙酰辅酶A驱动抗凋亡NF-κB信号的能力。
值得注意的是,乙酰辅酶A还是自噬的强效抑制剂,自噬本身具有强效的免疫调节活性,这可能将自噬调节牵涉到FAO的免疫学效应中。CPT1A的表达似乎还通过促进抗凋亡信号促进癌细胞对CTL衍生的IFNγ的抗性。
脂质动员上游的FAO,由ADP核糖基化因子1(ARF1)介导,被认为与癌症干细胞的强免疫逃避特性有关。具体而言,在一种遗传工程模型的CRC中删除Arf1已显示出显著减缓疾病的发生和进展,这是由于在癌症干细胞区中免疫原性应激和细胞死亡途径的激活,从而导致树突状细胞(DC)依赖的肿瘤靶向免疫反应的激活。
总之,这些观察结果展示了FAO在癌细胞中对TME免疫构造和癌症对免疫治疗敏感性的影响。
(2)脂质合成
脂肪酸合酶(FASN)是de novo脂质生物合成的限速酶,其表达水平通常与癌症晚期和转移扩散有关。在卵巢癌患者中,FASN的高水平与肿瘤的T细胞浸润减少相关,这不仅是由于脂肪酸在肿瘤微环境(TME)中积累,并通过CD36依赖的T细胞摄取直接介导的T细胞抑制,还因为脂质驱动的树突状细胞(DCs)在T细胞交叉引导中的缺陷,以及调节性T细胞(Treg细胞)功能的促进。与CD36介导的脂肪酸摄取的免疫抑制作用一致,CD36表达的CD8+ T细胞的肿瘤浸润在接受免疫原性化疗的非小细胞肺癌(NSCLC)患者中与较差的疾病预后有关。
(3)类二十烷酸的合成
FASN 活性的增加还促进了细胞内脂滴的积累,这与前列腺素内过氧化物合酶 2 相关,这是一种在类二十烷酸合成中的关键酶。PGE2 对恶性细胞具有直接的促分裂效应,同时还具有各种免疫抑制效应。这些效应包括通过前列腺素 E 受体 2 (PTGER2) 和 PTGER4 信号传导以及增加细胞内环AMP水平导致的树突状细胞 (DC) 功能障碍,抑制 NK 细胞的细胞毒性和分泌活动(这也影响需要抗原交叉呈递给 T 细胞的 I 型常规 DC 的招募),以及通过 NF-κB 介导的 PD1 上调导致的 T 细胞抑制。这种效应由于 PGE2 能够在髓样细胞上上调 PDL1 表达而加剧。
值得注意的是,PGE2 类似于缺氧(缺氧也具有一系列免疫抑制效应),能够在 TME 的髓样细胞上促进外核苷酸酶 CD73 的上调,这有助于核苷酸代谢的免疫抑制效应(见下文)。有趣的是,溶血磷脂酰胆碱转运蛋白 MFSD2A 已被证明在人体和小鼠胃癌细胞中作为内源性 COX2 抑制剂,从而减少 PGE2 和免疫抑制性细胞因子 TGFβ1 的生成和释放。在这种情况下,恶性细胞过表达 MFSD2A 已被证明能够规避对 PD1 阻断的抵抗,并且与 TME 中 CD8+ CTL 活性的改善迹象相关。
总的来说,这些观察结果突出了TME中脂肪酸代谢和免疫细胞功能之间复杂的相互作用。对这些机制的进一步理解将为开发新的治疗策略以提高免疫治疗的疗效提供有价值的见解。
在恶性转化背景下改变的其他代谢通路
在恶性转化的背景下,其他被改变的代谢通路也已被证明会影响抗癌免疫监视。这些包括(但不限于)参与核苷酸和各种氨基酸代谢的生化级联反应(图3)。
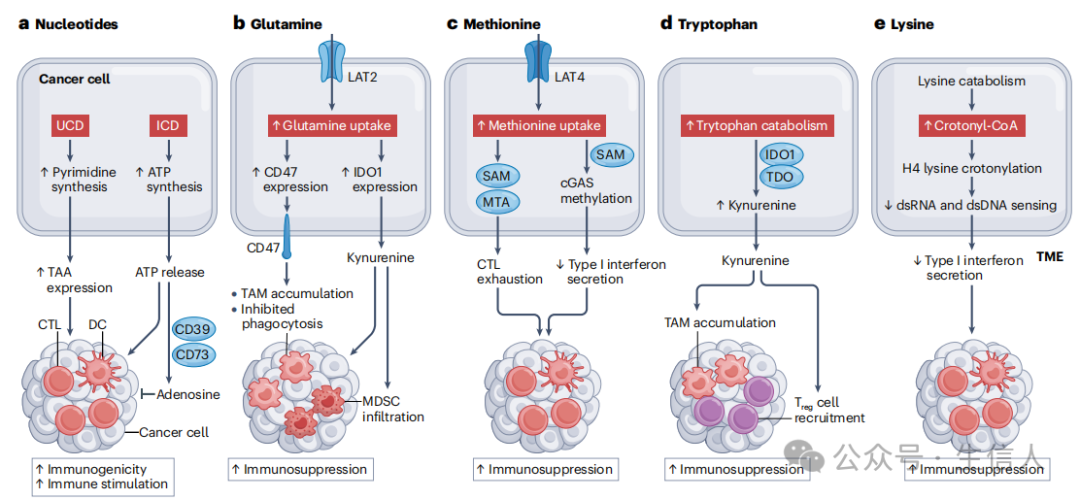
图3. 核苷酸和氨基酸代谢对抗癌免疫的影响
(1)核苷酸
癌细胞相比其正常对应物具有增加的核苷酸合成,这对抗癌免疫有显著影响。例如,癌细胞中尿素循环酶的改变导致尿素循环失调(UCD),这将氮流重定向至酶类碳酰基磷酸合成酶2、天冬氨酸转氨甲酰酶和二氢乳清酸酶(CAD)。这导致过量的嘧啶合成,促进一种独特的基因组特征,其特点是嘌呤向嘧啶的转化,并与黑色素瘤患者对ICIs的敏感性增加有关。在驱动UCD的CRC的临床前模型中也得到了类似的发现。此外,受压和死亡的恶性细胞释放的核苷酸对TME的免疫结构和免疫系统对癌细胞死亡的反应有重大影响。例如,胞外ATP可以通过嘌呤能受体P2Y2(P2RY2)被包括DC及其前体在内的髓样细胞检测到,促进趋化性,从而吸引髓样细胞到死亡细胞的附近。ATP还可以结合P2RX7,促进DC通过炎性体信号传导和IL-1β分泌来激活。ATP的这种免疫刺激作用通过CD39和CD73的顺序活性降解ATP而被积极对抗,它们共同促进腺苷的生成,这是一种强效的免疫抑制分子。因此,CD39和CD73的肿瘤内水平(不仅在不同肿瘤之间存在显著差异,而且在同一肿瘤的不同细胞区室中也存在显著差异)是决定胞外ATP的免疫刺激(低CD39和CD73表达)与免疫抑制(高CD39和CD73表达)效应的关键因素。
综上所述,这些观察结果表明,通过靶向癌细胞的核苷酸代谢以实现免疫治疗效果是可行的,这一方法正在临床试验中进行研究,并取得了有希望的结果。
(2)谷氨酰胺
肿瘤微环境(TME)中的谷氨酰胺是快速增殖的癌细胞和免疫细胞的重要能量和中间代谢物来源。大多数癌细胞以高于葡萄糖的速率消耗谷氨酰胺,并且至少在一定程度上对谷氨酰胺的可用性具有非癌基因依赖性。支持这一代谢适应的免疫抑制功能的证据显示,人类基底样乳腺癌具有高转录签名的谷氨酰胺代谢特征,似乎免疫浸润较少,这与不良的疾病预后相关。因此,从小鼠三阴性乳腺癌(TNBC)细胞中删除谷氨酰胺酶(Gls)——谷氨酰胺代谢的第一个酶——已被证明能通过T细胞依赖机制促进体内肿瘤控制。值得注意的是,通过一种在TME中优先活化的前药(JHU083)对GLS的药理学抑制似乎在携带MC38结直肠癌(CRC)的小鼠中驱动了强效抗癌反应,通过抑制癌细胞的氧化和糖酵解代谢,同时促进OXPHOS,从而在CTLs中引发持久的激活表型。这些发现指出了在有效靶向癌细胞谷氨酰胺代谢的同时保留肿瘤内CTLs的治疗策略的潜力。
癌细胞中的谷氨酰胺代谢也影响髓样细胞的募集和激活。例如,用药理学药剂抑制GLS已被报道限制肿瘤浸润的髓样抑制细胞(MDSCs),并在TNBC的临床前模型中促进TAMs向免疫刺激性的M1样表型的重新极化。这至少部分源于恶性(和免疫)细胞中吲哚胺2,3-双加氧酶1(IDO1)的下调,导致免疫抑制性犬尿氨酸的显著减少。此外,恶性细胞似乎通过溶质载体SLC38A2与1型常规树突状细胞(DCs)争夺肿瘤内谷氨酰胺的可用性,至少在小鼠的黑色素瘤和CRC模型中是如此。这些发现指出了新型(免疫)治疗药物靶向癌细胞上SLC38A2的潜力。最后,通过LAT2(也称为SLC7A8)增加癌细胞谷氨酰胺摄取与前临床骨肉瘤模型中的CD47上调相关,导致吞噬作用受抑和肿瘤进展加速。综上所述,这些发现例证了谷氨酰胺代谢在癌症和免疫细胞中的多方面免疫调节功能。
(3)蛋氨酸
蛋氨酸是一种必需氨基酸,除了参与蛋白质合成外,还参与酶促甲基化反应。蛋氨酸循环酶及其产物(包括5-甲硫腺苷和S-腺苷甲硫氨酸)的水平增加与小鼠和人类肝细胞癌模型中的T细胞耗竭有关。在这种情况下,删除编码SAM合成关键酶的蛋氨酸腺苷转移酶2A(Mat2a)在体内恢复了T细胞激活和肝细胞癌控制。
类似地,蛋氨酸已被证明通过甲基化依赖的方式损害cGAS活性。值得注意的是,癌细胞通常高表达蛋氨酸转运蛋白LAT4(也称为SLC43A2),因此与T细胞竞争这种必需氨基酸。这导致T细胞中二甲基化组蛋白H3赖氨酸79(H3K79me2)的丧失、信号转导和转录激活因子5A(STAT5A)信号传导减少以及T细胞功能受抑。LAT4抑制和蛋氨酸补充都已被证明可以规避这一缺陷,并恢复携带CRC小鼠的抗癌免疫。特异性肿瘤LAT4抑制与cGAS-STING1激活相结合——通过携带Slc43a2靶向CRISPR-Cas9构建体加Zn2+离子的双金属纳米平台实现——在TNBC的临床前模型中表现出有前途的免疫治疗效果。这些例子指出了LAT4作为开发具有临床应用的新型免疫刺激剂的潜在靶点。在此背景下,必须设想靶向方法以实现选择性从癌细胞中耗尽蛋氨酸,而不是免疫细胞,这也依赖于蛋氨酸摄取来发挥其抗癌功能。
(4)色氨酸
由酶IDO1和色氨酸2,3-双加氧酶(TDO)启动的色氨酸代谢吸引了大量关注,作为开发新型免疫治疗策略的潜在目标。某些恶性细胞(以及耐受性树突状细胞(DC))中发生的IDO1过度激活介导了广泛的免疫抑制效应,这些效应主要源自犬尿氨酸的积累,犬尿氨酸强烈抑制T细胞并促进调节性T细胞(Treg)的分化。实际上,尽管色氨酸是一种必需氨基酸,但其浓度在肿瘤微环境(TME)中不会低于一个限制阈值,这意味着色氨酸短缺并不如最初提出的那样导致由IDO1驱动的免疫抑制。IDO1通路的其他免疫抑制产物包括喹啉酸,它已被证明在GBM环境下通过FOXO1和过氧化物酶体增殖物激活受体-γ(PPAR-γ)信号传导促进M2样肿瘤相关巨噬细胞(TAM)极化。
(5)赖氨酸
已证明,GBM干细胞可以重新编程赖氨酸的代谢,导致肉豆蔻酰辅酶A(crotonyl-CoA)在细胞内积累,并导致组蛋白H4赖氨酸肉豆蔻酰化。在这种情况下,抑制赖氨酸肉豆蔻酰化可以增强由双链RNA(dsRNA)和双链DNA(dsDNA)引发的I型干扰素信号,最终恢复CD8+ T细胞对肿瘤的浸润,并抑制疾病进展。这些数据表明赖氨酸代谢是开发新型免疫疗法的潜在目标,尽管目前尚不清楚这种机制是否在GBM以外的其他癌症类型中发挥作用。
靶向癌细胞代谢
数十年来,针对癌细胞代谢的小分子和单克隆抗体已被开发,其中包括目前正在临床评估的各种药物。累积的数据表明,这些药物中至少有一部分是有希望的工具,可以恢复癌症免疫监视并提高肿瘤对获批准的抗癌治疗的敏感性,这些治疗方法不仅包括免疫疗法,还包括免疫原性化疗、某些靶向抗癌药物和放射治疗(表1)。几种饮食干预措施也正在研究其改变癌细胞代谢以增强抗癌免疫的能力。
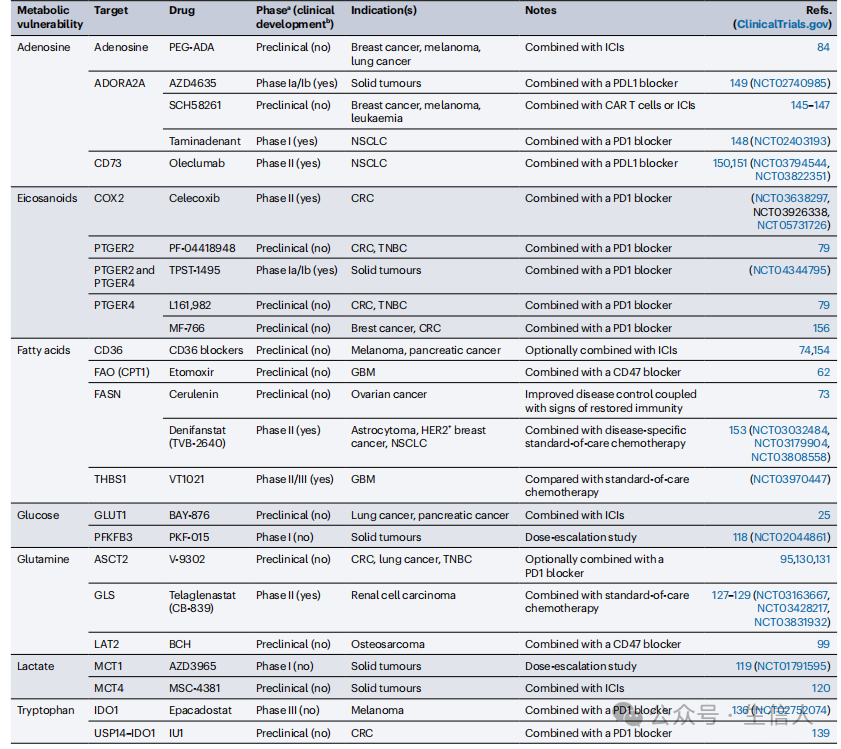
表1. 代谢抑制剂靶向癌细胞以恢复免疫监视
(1)葡萄糖和乳酸靶点
药理性GLUT1抑制剂BAY-876已被用于增加靶向PD1的ICI在胰腺癌和肺癌前临床模型中的治疗反应。然而,在这种情况下,GLUT3(也称为SLC2A3)的过表达似乎至少部分地补偿了GLUT1抑制,这表明联合GLUT1和GLUT3抑制可能是一个潜在的更优策略。PD1阻断也已被证明可以与PKF-015(一种糖酵解酶6-磷酸果糖-2-激酶/果糖-2,6-双磷酸酶3(PFKFB3)的药理性抑制剂)在黑色素瘤和结直肠癌小鼠模型中协同作用,这一效果可能归因于PFKFB3抑制诱导PDL1表达的能力。在一项测试PKF-015类似物在实体瘤患者中的剂量递增I期临床试验(ClinicalTrials.gov: NCT02044861)的初步结果中,证实了这种方法在人类中的可行性。尽管如此,靶向葡萄糖摄取或消耗用于癌症治疗仍具有挑战性,因为包括神经元在内的多种健康细胞类型都大量依赖于葡萄糖代谢来维持其正常功能,这需要开发靶向递送策略。理论上,抑制TME中的乳酸分泌或摄取可能比整体阻断糖酵解代谢面临的挑战更少。然而,以乳酸为重点的过去的药物开发努力,包括开发MCT1抑制剂AZD3965(在晚期实体瘤患者中耐受良好),已经被中止。是否最近的前临床研究结果显示出多种乳酸靶向策略(包括MCT4抑制剂如MSC-4381)与各种形式的免疫疗法的积极相互作用将重新激发这些努力尚不清楚。
(2)谷氨酸靶点
GLS(谷氨酰胺合成酶)靶向剂telaglenastat(也称为CB-839)已被报道可以与放疗协同作用,针对人类头颈部鳞状细胞癌和非小细胞肺癌(NSCLC)异种移植瘤显示出显著的放射增敏效果。然而,目前尚不清楚telaglenastat的放射增敏效应是否涉及先天免疫激活。尽管如此,telaglenastat也被证明在免疫能力正常的黑色素瘤模型中与CTLA4和PD1阻断剂协同作用,这表明该药物确实具有治疗相关的免疫刺激效应。几项独立研究的临床数据显示,在转移性肾细胞癌患者中,telaglenastat可以安全地与标准护理化疗结合使用,尽管其治疗效果较为有限。这些临床发现减少了对telaglenastat作为新型抗癌药物的开发兴趣,截至2024年2月,仅有一项针对NSCLC患者的研究仍然开放招募(ClinicalTrials.gov: NCT03831932)。
药理性抑制谷氨酰胺通过LAT2摄取的BCH(2-氨基双环(2,2,1)庚烷-2-羧酸)已被证明可以增强免疫原性化疗药物多柔比星对骨肉瘤细胞的治疗效果,这至少部分反映了CD47下调和癌细胞吞噬作用的增加。同样,谷氨酰胺摄取的药理性抑制剂V-9302(通过溶质载体ASCT2,亦称为SLC1A5)已被证明在TNBC的前临床模型中介导T细胞依赖的肿瘤控制。然而,V-9302给药在小鼠肺癌和CRC细胞中也与通过NF-κB上调PDL1相关,这抑制了肿瘤靶向的免疫反应。然而,这种免疫抑制反应伴随着恶性细胞表面死亡受体FAS(也称为CD95)的上调,使得它们对T细胞反应更为敏感,并可以通过PDL1阻断剂药理性重新激活。这些关于V-9302对抗癌免疫影响的看似矛盾的观察是否反映了不同癌细胞类型中特异性的谷氨酰胺代谢仍有待澄清。
(3)色氨酸靶点
在一大批免疫功能正常的肿瘤模型中生成的前临床数据显示,药理或遗传阻断IDO1和/或TDO活性可以显著增强免疫治疗效果,这些效果通常可以通过ICI(免疫检查点抑制剂)进一步放大。这些发现引起了对临床可测试的IDO1抑制剂(如epacadostat)开发的极大兴趣。非随机早期临床试验的初步结果表明,epacadostat可以安全有效地与PD1抑制剂联合使用于晚期实体瘤患者。然而,尽管有很高的期望,一项针对晚期黑色素瘤患者的随机III期临床研究显示,epacadostat加PD1抑制剂pembrolizumab的治疗效果并不优于单独使用pembrolizumab。是否这反映了存在替代的色氨酸降解途径——已被证明在非肿瘤环境(尤其是自身免疫疾病)中具有免疫抑制效果,并可能在IDO1抑制背景下上调——尚待证明。这些负面结果大大降低了制药公司开发IDO1抑制剂的兴趣,截至2024年2月,仅有少数临床试验仍在招募中。新颖的IDO1靶向方法(如用IU1抑制泛素特异性肽酶14(USP14)),在CRC的前临床模型中已被证明能够有效恢复T细胞依赖的疾病控制,可能会重新引发兴趣。
(4)核苷酸靶点
在多种前临床癌症模型中,药理学抑制CD39、CD73和/或腺苷受体作为独立治疗剂与恢复抗癌免疫和改善疾病控制相关联。此外,报道了针对CD73的小分子抑制剂AB680使小鼠胰腺癌对特异性PD1的ICI疗法敏感化,治疗效果表现为Treg细胞在肿瘤中的浸润减少。类似地,针对CD73的单克隆抗体据报告改善了乳腺癌前临床模型中局部放疗与CTLA4抑制剂联合治疗的治疗效果,至少部分归因于增加DC在肿瘤微环境中的招募和DC的激活。类似的结果也通过将聚乙二醇化的腺苷脱氨酶(将细胞外腺苷转化为肌醇)与PD1抑制剂联合应用于TNBC、黑色素瘤和肺癌的前临床模型中获得。
腺苷A2a受体(ADORA2A)拮抗剂已被证明与多种免疫治疗策略在前临床肿瘤模型中协同作用,包括白血病模型中的CAR T细胞治疗和乳腺癌、黑色素瘤模型中的PD1抑制剂。与这些前临床发现一致,多个I期临床试验已评估ADORA2A或ADORA2B拮抗剂在CRC、NSCLC或去势抵抗性前列腺癌患者中的应用,取得了令人鼓舞的结果。此外,两项平行的II期研究报告了一种中和CD73(oleclumab)的单克隆抗体与PDL1抑制剂durvalumab联合应用于可手术NSCLC患者的新辅助干预或治疗不可切除NSCLC患者管理中的显著活性。然而,尽管已有大量研究评估并持续评估CD39阻断剂在癌症患者中的应用,该方法的临床适用性仍不确定。
(5)脂肪酸靶点
通过CPT1阻断剂etomoxir抑制脂肪酸氧化(FAO)据报导在与CD47靶向抗体和放疗联合治疗对抗原本对放射线具有抗药性的小鼠脑胶质母细胞瘤(GBM)模型中显示出协同作用,与恢复肿瘤相关巨噬细胞对癌细胞的吞噬能力相关。然而,目前尚不清楚这些发现是否可以转化到人类GBM。
药理学抑制脂肪酸合酶(FASN)与丝氨酸脱氨酶(cerulenin)已显示在卵巢癌前临床模型中恢复DC激活和效应T细胞的肿瘤浸润,这与至少部分肿瘤控制相关。与这些发现一致,FASN抑制剂denifanstat(也称为TVB-2640)已证明在晚期肿瘤患者和高级别星形胶质瘤中耐受良好,促使在各种新生肿瘤病情患者中开展临床试验(ClinicalTrials.gov: NCT02980029、NCT03179904、NCT03808558、NCT05743621)。
CD36阻断剂在胰腺癌前临床模型中与免疫原性免疫疗法联合应用显示出有希望的活性,并在黑色素瘤前临床模型中与PD1抑制剂联合应用,但是CD36阻断剂的开发成为临床可用药物仍处于初级阶段,只有一种药物(VT1021) — 该药物靶向CD36配体血栓素结合蛋白1(THBS1) — 正在评估其用于GBM治疗的临床试验中(ClinicalTrials.gov: NCT03970447)。
(6)类二十烷酸靶点
为了保持PGE2强效抑制抗癌免疫反应的能力,COX2、PTGER2和/或PTGER4的抑制药理策略已被证明在多种前临床肿瘤模型(包括CRC、黑色素瘤、乳腺癌和NSCLC模型)中与改善肿瘤控制、恢复免疫效应功能和ICIs协同作用有关。由于肝X受体(LXRs)激动剂已被证明可以促进MFSD2A(内源性COX2抑制剂)的表达,这些激动剂可能是限制COX2依赖性免疫抑制的有前途的工具。然而,最近的证据表明,LXR激活还会导致鞘磷脂磷酸二酯酶酸样3A的表达,这种酶会积极降解cGAS产物2',3'-环状GMP-AMP,从而抑制STING1激活下游的I型干扰素产生,至少在髓样细胞中。
类似地,常规COX2抑制剂(包括塞来昔布和阿司匹林)具有一系列免疫抑制作用,包括直接抑制cGAS161。因此,通过PGE2定向策略恢复最佳抗癌免疫可能受益于拮抗PGE2受体(如PTGER2和PTGER4)的药物,而不是靶向COX2。例如,TPST-1495(一种新的PTGER2和PTGER4双重拮抗剂)目前正在作为单一治疗药物或与PD1抑制剂pembrolizumab联合治疗晚期实体瘤患者(ClinicalTrials.gov: NCT04344795)。此外,正在进行的试验还测试了塞来昔布加pembrolizumab在结直肠癌或直肠癌患者中的效果(ClinicalTrials.gov: NCT03638297、NCT03926338、NCT05731726),主要基于COX2抑制剂在该癌症指征中的已证实的癌症预防效果。
总的来说,这些发现强调了代谢抑制剂不仅作为癌症靶向药物的潜力,还作为可能与其他治疗策略协同作用以恢复免疫监视的免疫刺激剂的潜力(表1)。
小编总结
越来越多的前临床文献表明,通过靶向癌细胞代谢来实现免疫刺激效应的可能性。尽管存在挑战,癌细胞代谢仍然作为一种有前景的靶点脱颖而出,可以恢复免疫监视,从而将免疫学上“冷”的肿瘤转化为对免疫疗法有反应的“热”病灶。
参考文献:
Mara De Martino, Jeffrey C Rathmell, Lorenzo Galluzzi, Claire Vanpouille-Box. Cancer cell metabolism and antitumour immunity. Nat Rev Immunol. 2024 Apr 22. doi: 10.1038/s41577-024-01026-4.
链接:http://www.lewenyixue.com/2024/12/02/Nature%E4%B8%87%E5%AD%97%E7%BB%BC%E8%BF%B0%EF%BC%9A%E7%99%8C%E7%BB%86%E8%83%9E%E4%BB%A3%E8%B0%A2%E4%B8%8E%E6%8A%97%E8%82%BF%E7%98%A4/