年度综述:癌症领域PROTAC的发展
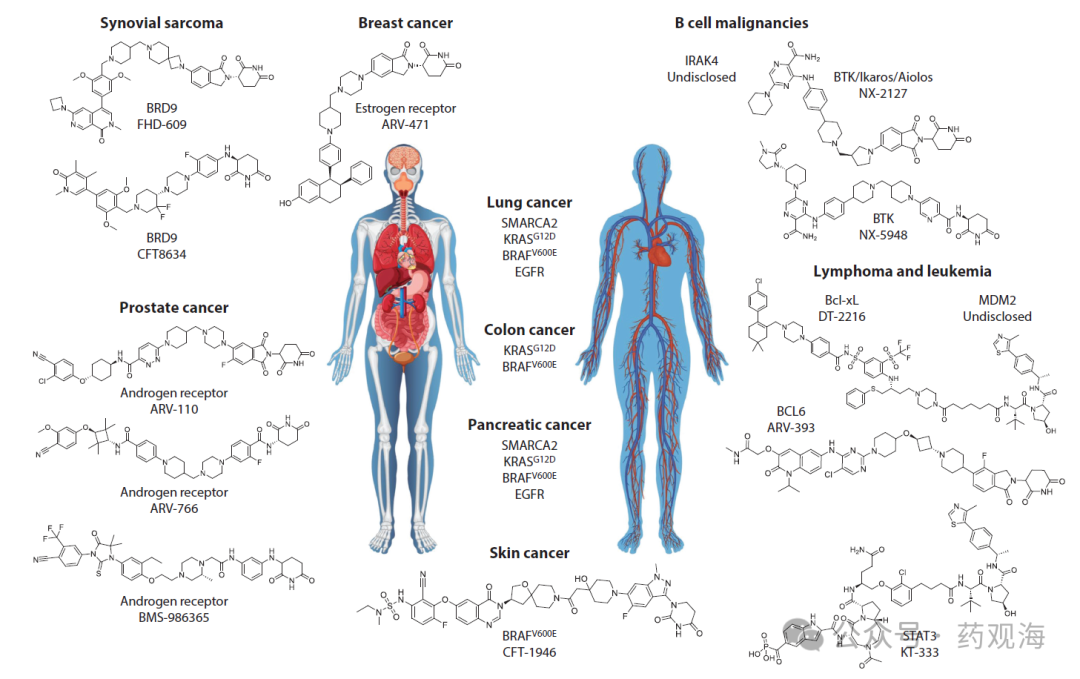
尽管近年来癌症治疗取得了显著进展,但药物毒性、疗效不足和耐药性仍然是临床治疗的主要挑战。传统的药物研发主要集中于开发小分子抑制剂,这些抑制剂通过结合蛋白质的活性位点来阻断其功能。然而,许多致癌蛋白缺乏合适的结合位点,或者抑制剂无法完全阻断蛋白质的功能,导致治疗效果不佳。靶向蛋白降解技术,特别是PROTAC技术,为克服这些挑战提供了一种新的策略。
二、PROTAC作用机制
PROTAC 是双功能小分子,由三部分组成:E3 连接酶配体、连接体和靶蛋白 (POI) 配体。PROTAC 通过将 POI 与 E3 连接酶连接起来,形成三元复合物,从而促进泛素分子转移到 POI 上。泛素化的 POI 会被蛋白酶体识别并降解。由于 PROTAC 的催化作用机制,它可以在亚化学计量浓度下发挥作用,并且可以降解高丰度蛋白,从而在低剂量下达到显著的靶蛋白降解。
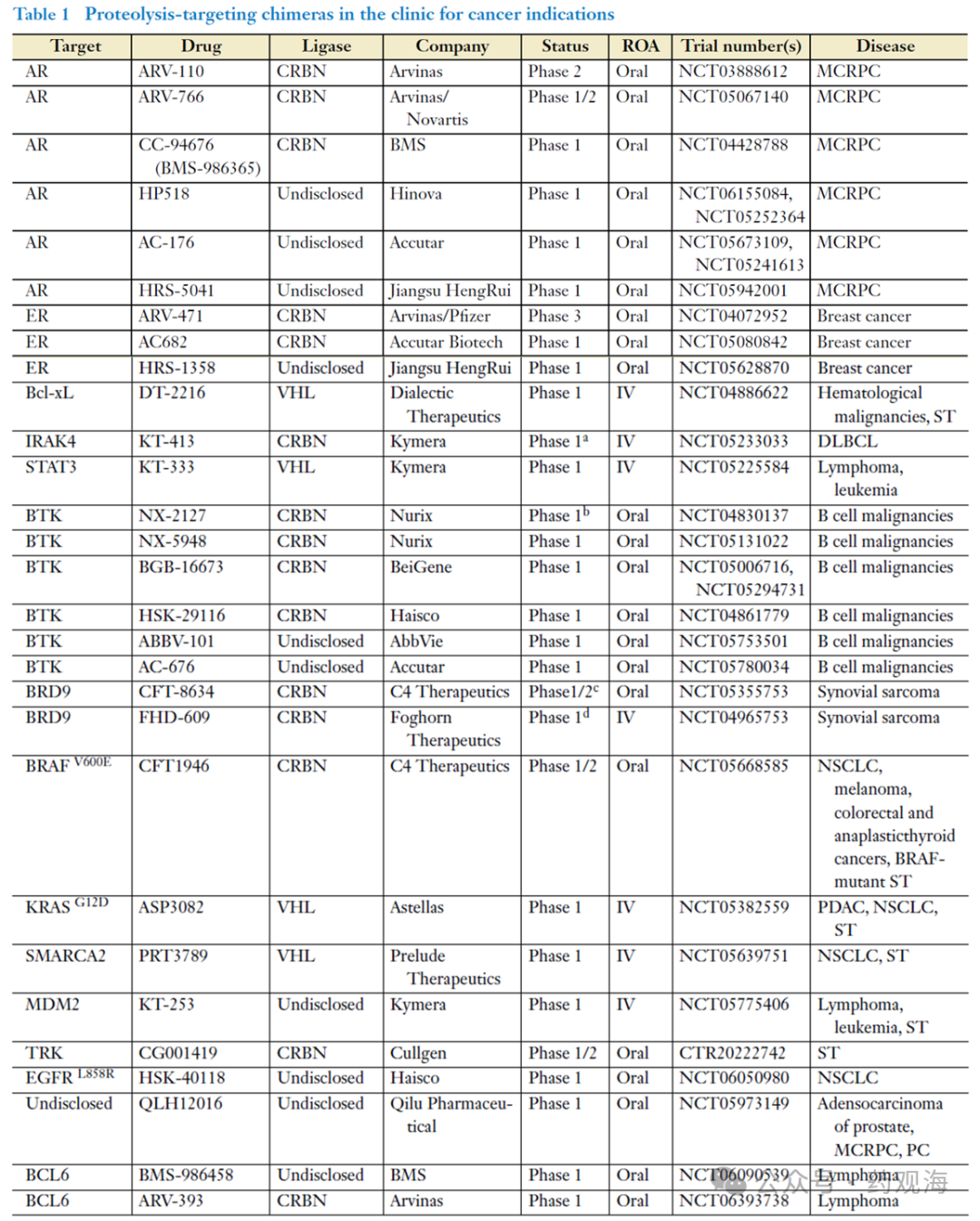
1. AR
-
作用机制: AR-PROTACs通过招募E3连接酶(例如CRBN)使AR泛素化,从而促进蛋白酶体降解AR,阻断AR信号通路,抑制前列腺癌细胞增殖。
代表药物:
ARV-110 (Bavdegaluta mide): 首个进入临床的PROTAC药物,靶向AR,用于治疗mCRPC。临床试验结果显示,ARV-110在携带AR T878X/H875Y突变的患者亚组中疗效最佳,凸显了患者分层的重要性。然而,在更广泛的mCRPC患者群体中,其疗效有限,可能与AR信号通路复杂的耐药机制有关。
ARV-766 (Luxdegalutamide): 第二代AR-PROTAC,具有更高的稳定性和更广的基因型覆盖范围,可降解野生型和突变型AR。早期临床数据显示,ARV-766在较低剂量下即可有效降低前列腺特异性抗原水平,展现出优于恩杂鲁胺的潜力。目前ARV-766正在进行激素治疗后mCRPC患者的临床试验,并计划开展一线治疗的临床试验。
CC-94676 (BMS-986365):一种异双功能口服疗法,旨在通过 AR 降解和拮抗的一流双重机制来抑制 AR 活性,ESMO2024上展现的mCRPC一期临床数据出色,计划2025启动3期注册性临床【 ESMO2024--BMS-986365数据出色,BMS计划2025启动3期注册性临床 】。
其他AR-PROTAC: 包括HP518、AC-176和HRS-5041等 ,均处于早期临床试验阶段,靶向mCRPC。这些PROTAC大多基于CRBN或其他未公开的E3连接酶。其临床疗效和安全性数据还有待进一步公布。
-
未来展望: 开发更有效的AR-PROTACs,拓展适应症至激素敏感性前列腺癌,探索与其他疗法的联合应用。
2. ER
作用机制:ER-PROTACs通过介导ER降解,抑制ER信号通路,从而发挥抗肿瘤作用。
代表药物:
ARV-471 (Vepdegestrant): 口服、高效的ER-PROTAC,用于治疗ER阳性/HER2阴性的局部晚期或转移性乳腺癌。临床前研究显示,ARV-471在多种乳腺癌细胞系中均能有效降解ER,并表现出优于氟维司群的肿瘤抑制活性。ARV-471已进入3期临床试验,并获得了FDA快速通道资格认定,有望成为治疗乳腺癌的新型有效疗法。
其他ER-PROTAC: 包括AC682 和HRS-1358等,处于 早期临床试验阶段,主要用于治疗ER阳性的乳腺癌。
-
未来展望: 进一步评估ARV-471在不同乳腺癌亚型中的疗效和安全性,探索与其他疗 法的联合应用,例如CDK4/6抑制剂或PI3K抑制剂。
3. BTK
作用机制:BTK-PROTACs通过诱导BTK降解,抑制BCR信号通路,从而治疗B细胞恶性肿瘤。
代表药物:
NX-2127 (Zelebrudomide): 双重BTK和Ikaros降解剂,兼具分子胶和PROTAC的特性。它可以降解野生型和C481S突变型BTK,以及IKZF1和IKZF3。临床试验显示,NX-2127在CLL患者中取得了良好的疗效,与BTK突变状态无关。然而,由于生产工艺改进的 需求,该药物的1期临床试验目前处于暂停状态。
NX-5948: 第二代BTK-PROTAC,具有更高的选择性和中枢神经系统渗透性。临床前研究显示,NX-5948比抑制剂和第一代降解剂更有效地抑制肿瘤生长。目前NX-5948正处于1期临床试验中,用于治疗B细胞恶性肿瘤,包括中枢神经系统肿瘤和原发性中枢神经系统淋巴瘤。
其他BTK-PROTAC: 包括BGB-16673、HSK-29116、ABBV-101、HZ-Q1070、UBX-303等,均处于早期临床试验阶段,主要用于治疗B细胞恶性肿瘤。
未来展望:进一步评估NX-5948的疗效和安全性,特别是其中枢神经系统活性;开发针对不同BTK突变的PROTACs,克服耐药性。
4. Bcl-xL
作用机制:DT-2216通过选择性降解Bcl-xL,诱导肿瘤细胞凋亡,而不会显著影响血小板存活,从而降低血小板减少症的风险。
代表药物:
DT-2216: 1期临床试验正在进行中,用于治疗复发/难治性TCL和其他血液系统恶性肿瘤。初步数据显示,DT-2216在不引起严重血小板减少的情况下具有抗肿瘤活性。
未来展望:评估DT-2216的长期疗效和安全性,探索与其他疗法的联合应用。
5. BCL6
作用机制:BCL6-PROTACs通过降解BCL6,抑制其转录调控功能,从而抑制DLBCL细胞增殖。
代表药物:
ARV-393, BMS-986458: 这两种BCL6-PROTACs均处于1期临床试验阶段,主要用于治疗DLBCL。
未来展望:评估ARV-393和BMS-986458的疗效和安全性,探索与其他疗法的联合应用,例如利妥昔单抗。
6. IRAK4
作用机制:IRAK4 是 TLR 和 IL-1R 信号通路的关键激酶,在多种炎症和癌症中发挥作用。IRAK4-PROTACs 通过降解 IRAK4 蛋白,阻断下游信号传导,从而发挥抗炎和抗肿瘤作用。
代表药物:
KT-413: 由 Kymera Therapeutics 开发,是一种 CRBN E3 连接酶为基础的 IRAK4 降解剂。临床前研究显示,KT-413 能有效降解 IRAK4,并在多种疾病模型中显示出疗效。曾开展针对非霍奇金淋巴瘤、惰性淋巴瘤、B 细胞非霍奇金淋巴瘤、滤泡性淋巴瘤、弥漫性大 B 细胞淋巴瘤和原发性皮肤大 B 细胞淋巴瘤的 I 期临床试验。尽管达到了预期的降解水平且没有剂量限制性毒性,但由于战略原因,该项目已终止开发。
未来展望:尽管 KT-413 的开发终止,但 IRAK4 仍然是一个有吸引力的靶点。未来研究可能集中在寻找新的 IRAK4 降解剂,优化其理化性质和药代动力学特性,并探索新的联合治疗策略。
7. BRD9
作用机制:BRD9 是非经典 SWI/SNF 染色质重塑复合物的一个组成部分,在滑膜肉瘤和 SMARCB1 缺陷型肿瘤中发挥关键作用。BRD9-PROTACs 通过降解 BRD9 蛋白,破坏癌细胞的转录调控,从而抑制肿瘤生长。
代表药物:
FHD-609: 由 Foghorn Therapeutics 开发,是一种 CRBN E3 连接酶为基础的 BRD9 降解剂。I 期临床试验显示 FHD-609 可有效降解 BRD9,但在较高剂量下出现 QTc 间期延长,导致试验暂停。
CFT-8634: 由 C4 Therapeutics 开发,是一款口服 BRD9 降解剂。I 期临床试验显示,尽管 BRD9 降解水平很高,但在滑膜肉瘤和 SMARCB1 缺陷型实体瘤患者中疗效不足,导致试验终止。
未来展望:尽管面临挑战,BRD9 仍然是一个有潜力的靶点。未来的研究可能需要关注滑膜肉瘤的关键驱动因素 SSX-SS19 融合蛋白。此外,也需要进一步优化 BRD9-PROTACs 的理化性质和药代动力学特性,并探索新的联合治疗策略。
8. STAT3
作用机制:STAT3 是一种参与肿瘤发生、发展和转移的转录因子。STAT3-PROTACs 通过降解 STAT3 蛋白,阻断其下游信号通路,从而抑制肿瘤生长。
代表药物:
KT-333: 由 Kymera Therapeutics 开发,是一款 VHL E3 连接酶为基础的 STAT3 降解剂。I 期临床试验显示 KT-333 能够有效降解 STAT3,并在特定患者群体中观察到临床意义的缓解。该药物已获得治疗皮肤 T 细胞淋巴瘤和外周 T 细胞淋巴瘤的孤儿药资格认定,以及 FDA 快速通道资格认定。
未来展望:KT-333 的临床试验结果令人鼓舞,有望成为治疗 STAT3 驱动型癌症的新型疗法。未来需要进一步评估其长期疗效和安全性,并探索新的联合治疗策略。
9. MDM2
作用机制:MDM2 是 p53 肿瘤抑制蛋白的负调节因子。MDM2-PROTACs 通过降解 MDM2 蛋白,稳定 p53 蛋白水平,从而激活 p53 介导的细胞周期阻滞和凋亡,抑制肿瘤生长。
代表药物:
KT-253: 由 Kymera Therapeutics 开发。临床前研究表明,KT-253 可以克服 MDM2 的负反馈回路,并在体内外均显示出抗肿瘤活性。I 期临床试验正在进行中,用于治疗多种血液系统恶性肿瘤和实体瘤。初步数据显示,在耐受剂量下,KT-253 具有良好的疗效,且未观察到中性粒细胞减少症或血小板减少症等血液学毒性。
未来展望:KT-253 的早期临床数据令人鼓舞,有望成为治疗 p53 失活型癌症的新型疗法。未来需要进一步评估其长期疗效和安全性,并探索新的联合治疗策略。
10. EGFR
作用机制:EGFR 是一种参与细胞生长、增殖和分化的受体酪氨酸激酶。EGFR-PROTACs 通过降解 EGFR 蛋白,阻断 EGFR 信号通路,从而抑制肿瘤生长。
代表药物:
HSK-40118: 由 Haisco Pharmaceutical Group 开发,靶向 EGFR L858R 突变体。I 期临床试验正在进行中,用于治疗 EGFR 突变的晚期或转移性 NSCLC。
CFT-8919: 由 C4 Therapeutics 和 Betta Pharmaceuticals 合作开发,是一款变构的、口服生物可利用的 EGFR L858R 突变体选择性降解剂。临床前研究显示,CFT-8919 能够降解 EGFR L858R 及其继发突变体,并在对第三代 EGFR 抑制剂耐药的小鼠模型中显示出抗肿 瘤活性,包括 EGFR L858R T790M 脑转移模型。
HJ-002-03(和径医药)、BG-60366(百济神州):EGFR C797S PROTAC,处于临床一期。
未来展望:EGFR-PROTACs 为治疗 EGFR 突变型 NSCLC 提供了新的治疗选择,特别是对于那些对现有抑制剂产生耐药性的患者。未来需要进一步评估 HSK-40118 和 CFT-8919 的临床疗效和安全性,并探索新的联合治疗策略。
11. SMARCA2
作用机制:SMARCA2 和 SMARCA4 是 SWI/SNF 染色质重塑复合物的 ATP 依赖性解旋酶。SMARCA4 功能缺失突变在多种恶性肿瘤中富集。SMARCA2-PROTACs 通过选择性降解 SMARCA2,利用 SMARCA2 和 SMARCA4 之间的合成致死关系,从而杀死肿瘤细胞。
代表药物:
PRT3789: 由 Prelude Therapeutics 开发,是一款 VHL E3 连接酶为基础的 SMARCA2 降解剂。目前正在 I 期临床试验 中,作为单一疗法和与多西紫杉醇联合使用,用于治疗 SMARCA4 突变的 NSCLC。但一期初步临床结果不佳【 SMARCA2降解剂:靶向增强子重编程,治疗SMARCA4突变型肺癌的新策略 】。
PRT7732:Prelude Therapeutics 开发,是一款口服SMARCA2 降解剂,可能是基于CRBN。目前正在 I 期临床试验 中。
未来展望 :SMARCA2-PROTACs 为治疗 SMARCA4 突变型癌症提供了一种新的治疗策略。未来需要进一步评估 PRT3789 的临床疗效和安全性,并探索新的联合治疗策略。
12. KRAS
作用机制:KRAS 是一种在多种癌症中 häufig 突变的癌基因。KRAS-PROTACs 通过降解 KRAS 蛋白,阻断 KRAS 信号通路,从而抑制肿瘤生长。
代表药物:
ASP3082: 由 Astellas Pharma 开发,是一款靶向 KRAS G12D 突变体的 VHL E3 连接酶为基础的降解剂,目前处于 I 期临床试验阶段,但初步临床结果不佳【 ESMO2024--安斯泰来的KRASG12D PROTAC令人失望 】。FDA 已授予 ASP3082 快速通道资格认 定,用于治疗胰腺导管腺癌。
ASP4396:Astellas Pharma另一个靶向 KRAS G12D 突变体的PROTAC,目前处于 I 期临床试验阶段,可能是基于CRBN。
未来展望:KRAS 长期以来被认为是“不可成药”的靶点,KRAS-PROTACs 的出现为 KRAS 突变型癌症的治疗带来了新的希望。未来需要进一步评估 ASP3082 和其他 KRAS 降解剂的临床疗效和安全性,并探索新的联合治疗策略。
13. BRAF
作用机制:BRAF 是一种丝氨酸/苏氨酸激酶,是 RAS-RAF-MEK-ERK 信号通路的重要组成部分。BRAF V600E 突变在多种癌症中常见。BRAF-PROTACs 通过降解突变型 BRAF 蛋白,阻断下游信号通路,从而抑制肿瘤生长。
代表药物:
CFT1946: 由 C4 Therapeutics 开发,是一款靶向 BRAF V600E 突变体的 CRBN E3 连接酶为基础的降解剂。目前正在 I/II 期临床试验中,用于治疗 BRAF V600 突变驱动的癌症,包括对抑制剂耐药的癌症。该试验将评估 CFT1946 单药治疗和与 MEK 抑制剂曲美替尼联用的疗效。
未来展望:BRAF-PROTACs 为治疗 BRAF 突变型癌症,特别是对 BRAF 抑制剂耐药的癌症,提供了新的治疗选择。未来需要进一步评估 CFT1946 的临床疗效和安全性,并探索新的联合治疗策略。
PROTAC的优势
完全消除蛋白功能: 传统的抑制剂通常只阻断蛋白质的特定功能或相互作用,而PROTACs则通过降解目标蛋白,从根本上消除其所有功能,包括催化功能、支架功能以及蛋白-蛋白相互作用等。这对于那些具有多种功能或难以通过抑制单个活性位点来有效控制的蛋白靶点尤为重要,例如转录因子、支架蛋白和致癌融合蛋白等。
靶向“不可成药”靶点: 许多疾病相关蛋白缺乏明确的结合口袋或活性位点,传统的小分子抑制剂难以靶向。而PROTACs不需要与蛋白的活性位点结合,可以靶向蛋白表面任何可及的位点,从而拓展了可成药靶点的范围,为开发靶向“不可成药”靶点的药物提供了新的途径。
催化作用机制: PROTACs以催化方式发挥作用,即一个PROTAC分子可以介导多个目标蛋白的降解,因此在亚化学计量浓度下即可有效发挥作用。这使得PROTACs药物在较低剂量下即可达到治疗效果, potentially 降低脱靶效应和毒副作用,并提高药物的治疗窗口。
更高的选择性: 即使使用对同源蛋白没有选择性的配体,PROTACs也可能实现选择性降解。这是因为PROTACs的作用依赖于三元复合物的形成,而不同蛋白与E3连接酶形成三元复合物的稳定性和空间构象可能存在差异,从而导致选择性降解。此外,可以通过合理设计PROTACs的结构,例如连接体的长度和组成,来进一步提高其选择性。
克服耐药性: 肿瘤细胞常常通过靶点蛋白突变的方式产生对抑制剂的耐药性。而PROTACs的降解机制使其对某些类型的突变不敏感,例如那些不影响PROTAC结合但影响抑制剂结合的突变。此外,PROTACs还可以降解那些导致耐药性的突变蛋白,从而克服耐药性。
作用持久: PROTAC介导的蛋白降解作用通常比抑制剂的抑制作用更持久。这是因为蛋白降解后需要一定时间才能重新合成,而抑制剂的抑制作用则会随着药物的清除而减弱。PROTACs的持久作用可以延长给药间隔,提高患者的依从性。
PROTACs面临的挑战
成药性挑战: PROTACs通常具有较高的分子量、较多的氢键供体和受体、较高的亲脂性和较多的可旋转键,这些特性使其难以满足Lipinski五规则等传统药物的理化性质要求,导致较差的细胞渗透性、溶解度和口服生物利用度,给药物的开发和临床应用带来挑战。
脱靶效应: PROTACs可能结合并降解非目标蛋白,导致脱靶效应和毒副作用。这需要在药物设计和开发过程中进行严格的筛选和优化,以提高PROTACs的特异性。
耐药性机制: 尽管PROTACs可以克服某些类型的耐药性,但肿瘤细胞也可能通过其他机制对PROTACs产生耐药性,例如E3连接酶的突变或表达下调、泛素-蛋白酶体系统的功能障碍等。需要进一步研究PROTACs的耐药机制,并开发相应的应对策略。
药物递送: 由于PROTACs的分子量较大,其在体内的递送和分布可能受到限制,特别是到达实体瘤内部。需要开发新的药物递送系统,以提高PROTACs在肿瘤组织中的浓度和疗效。
免疫原性: PROTACs作为一种新型的药物分子,其免疫原性尚不清楚。需要进行深入的研究,以评估PROTACs的免疫原性风险,并开发相应的解决方案。
生产成本: PROTACs的合成和纯化相对复杂,导致其生产成本较高。需要开发更有效、更经济的PROTACs合成方法,以降低药物的生产成本,提高其可及性。
尽管PROTACs技术面临一些挑战,但其巨大的潜力吸引了学术界和工业界的广泛关注。随着研究的不断深入和技术的进步,相信这些挑战将逐步得到解决,PROTACs技术将在未来为治疗癌症和其他疾病带来新的突破。
五、未来展望
PROTAC技术作为一种新兴的靶向蛋白降解策略,展现出巨大的潜力,但仍处于发展早期。为了充分发挥其治疗潜力,未来的研究需要关注以下几个方面:
1. 扩展E3连接酶库及优化配体:
目前,大多数PROTACs依赖于CRBN和VHL这两种E3连接酶。为了克服对这两种E3连接酶的耐药性,以及实现组织特异性降解,需要开发靶向其他E3连接酶的PROTACs,例如MDM2、cIAP1、KEAP1、RNF114等。这需要发现和鉴定新的E3连接酶配体,并深入研究其与靶蛋白相互作用的机制。
优化现有E3连接酶配体,提高其结合亲和力和选择性,降低脱靶效应。开发具有更好成药性的配体,例如口服生物利用度更高、组织分布更广的配体。
2. 优化连接体和靶蛋白配体:
连接体的长度、组成和柔性会影响PROTACs的成药性和降解效率。需要开发新的连接体设计策略,例如可裂解连接体、可控释放连接体等,以提高PROTACs的靶向性和疗效。
优化靶蛋白配体,提高其结合亲和力和选择性。开发共价结合的靶蛋白配体,提高PROTACs的降解效率和作用持久性。探索靶向蛋白-蛋白相互作用界面的配体,以更有效地干扰蛋白功能。
3. 提高PROTACs的成药性:
PROTACs通常分子量较大,理化性质较差,导致其成药性较差。需要开发新的PROTACs设计策略,例如片段化的PROTACs、双PROTACs、杂合PROTACs等,以减小分子量,提高成药性。
利用计算辅助药物设计和人工智能技术,优化PROTACs的结构,提高其细胞渗透性、溶解度和口服生物利用度。
开发新的药物递送系统,例如纳米颗粒、抗体偶联药物等,以提高PROTACs在体内的递送效率和靶向性。
4. 深入研究PROTACs的作用机制和耐药机制:
深入研究PROTACs形成三元复合物的结构和动力学,揭示其降解靶蛋白的分子机制。
研究肿瘤细胞对PROTACs的耐药机制,例如E3连接酶的突变或表达下调、泛素-蛋白酶体系统的功能障碍等,并开发相应的应对策略,例如联合用药、开发新的PROTACs等。
5. 拓展PROTACs的应用领域:
PROTACs技术不仅可以用于治疗癌症,还可以用于治疗其他疾病,例如神经退行性疾病、感染性疾病、自身免疫性疾病等。
探索PROTACs在疾病诊断和生物标志物开发中的应用。
6. 开发新型靶向蛋白降解技术:
除了PROTACs技术外,还可以开发其他靶向蛋白降解技术,例如分子胶、自噬靶向嵌合体(AUTAC)、溶酶体靶向嵌合体(LYTAC)等,以拓展靶向蛋白降解的范围和应用。
7. 加强产学研合作:
加强学术界和工业界的合作,推动PROTACs技术的临床转化和应用。
建立PROTACs技术平台,共享资源和技术,加速PROTACs药物的研发进程。
总而言之,PROTAC技术具有广阔的应用前景,但仍面临诸多挑战。通过持续的创新和研究,不断优化PROTACs的设计和开发,克服其面临的挑战,PROTACs技术有望在未来为治疗多种疾病带来新的突破,造福人类健康。
六、结论
PROTAC 技术在癌症治疗领域展现出巨大的潜力。随着研究的不断深入,PROTAC 有望成为治疗癌症和其他疾病的新型有效疗法。然而,要充分发挥 PROTAC 的潜力,仍需要克服一些挑战,例如优化其理化性质、探索新的 E3 连接酶、开发组织特异性 PROTAC 以及研究其耐药性机制。相信随着技术的不断进步,PROTAC 将在未来为癌症患者带来更多希望。
链接:http://www.lewenyixue.com/2024/11/27/%E5%B9%B4%E5%BA%A6%E7%BB%BC%E8%BF%B0%EF%BC%9A%E7%99%8C%E7%97%87%E9%A2%86%E5%9F%9FPROTAC%E7%9A%84%E5%8F%91%E5%B1%95/