Sci Adv丨徐志爱团队开发点击型PD-L1抑制剂克服肿瘤免疫耐受
近年来,免疫治疗已经在肿瘤临床治疗中取得了重大突破。其中肿瘤免疫检查点阻断 (Immune checkpoint blockade,ICB) 疗法的发展激发了免疫检查点抗体药物和小分子抑制剂的开发热潮。目前已经有多款PD-L1抗体药物获批用于肿瘤免疫治疗。然而,PD-L1抗体药物在实体瘤的渗透受限,且会引起严重的免疫相关不良事件。和抗体药物相比,小分子PD-L1抑制剂在实体瘤的渗透性较好,血液清除半衰期较短,便于调整给药方案,有望避免抗体药物体内长循环导致的毒副作用。然而,常规的小分子PD-L1抑制剂存在口服吸收效率低、给药剂量较高、以及非特异性分布导致毒副作用等问题,限制了其临床转化。与传统的小分子抑制剂相比,共价抑制剂通过形成共价键稳定结合靶蛋白,显示出更好的靶标亲和力和治疗效果。然而,常规靶向天然氨基酸残基 (半胱氨酸、丝氨酸、酪氨酸、赖氨酸以及精氨酸) 的共价策略存在脱靶效应,易导致毒副作用。因此,如何开发肿瘤特异性的小分子PD-L1抑制剂,是改善抗肿瘤免疫疗效、避免免疫相关毒副作用的关键挑战。
近日,来自华东师范大学的 徐志爱教授团队在 Science Advances 发表了题为 Tumor-Specific Delivery of Clickable Inhibitor for PD-L1 Degradation and Mitigating Resistance of Radioimmunotherapy 的研究论文,该研究成果 展示了基于生物正交点击化学设计的可点击PD-L1抑制剂,实现肿瘤选择性PD-L1蛋白抑制,并克服放疗免疫耐受。
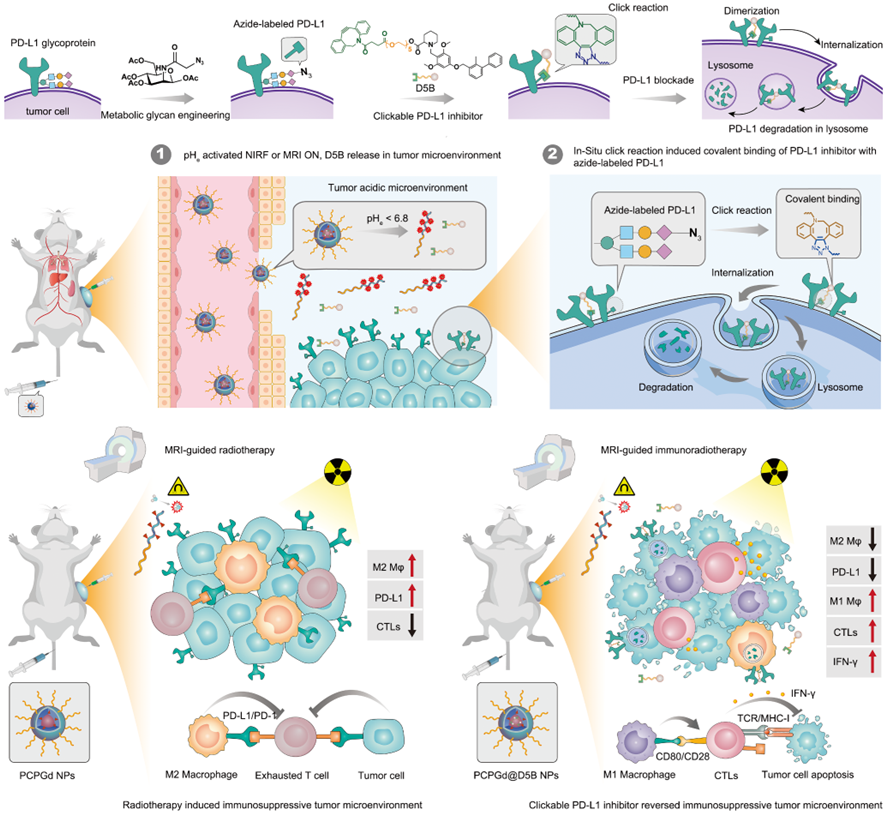
图1. 点击型共价抑制剂特异性降解肿瘤PD-L1以克服放射免疫耐受的原理示意图。
为了阐明可点击PD-L1抑制剂的构-效关系,研究人员设计了一系列具有不同长度柔性寡聚乙二醇 (Oligoethylene glycol,OEG) 链的可点击PD-L1抑制剂,以调节可点击PD-L1抑制剂的空间构型,优化出最佳分子结构。为了实现点击型PD-L1抑制剂的肿瘤特异性递送和PD-L1精准阻断,研究人员进一步构建了具有多模态成像功能的肿瘤微酸环境激活型纳米递送平台,用于可点击PD-L1抑制剂的肿瘤胞外区域选择性递送。该纳米递送平台在正常生理环境中保持稳定,可在肿瘤酸性胞外微环境中特异性激活释放可点击PD-L1抑制剂,并利用磁共振和荧光成像导航,实现精准放射免疫联合治疗。
本研究发现肿瘤放射治疗可上调肿瘤细胞和肿瘤相关巨噬细胞PD-L1,并诱导肿瘤相关巨噬细胞向M2型极化,导致免疫抑制微环境,严重制约肿瘤放疗效果。研究人员利用糖代谢策略实现代谢活跃的肿瘤细胞和肿瘤相关巨噬细胞的叠氮标记,通过点击化学反应实现了PD-L1抑制剂在肿瘤组织的局部富集,进而特异性降解肿瘤细胞和肿瘤相关巨噬细胞膜表面PD-L1,有效地逆转了放疗诱导的免疫抑制肿瘤微环境,克服放疗免疫耐受,从而抑制肿瘤生长。
华东师范大学博士研究生候博 (现为中国科学院上海药物研究所博士后) 为论文第一作者,中国科学院上海药物研究所硕士研究生叶佳依 (现为浙江大学博士研究生) 、博士研究生黄潞嘉为论文共同第一作者,华东师范大学徐志爱教授为论文通讯作者。中国科学院上海药物研究所于海军研究员、赵玉军研究员、黄蔚研究员给予了大力支持。
文章链接:https://doi.org/10.1126/sciadv.adq3940
制版人:十一
版权声明:本文为“乐问号”作者或机构在乐问医学上传并发布,仅代表该作者或机构观点,不代表乐问医学的观点或立场,不能作为个体诊疗依据,如有不适,请结合自身情况寻求医生的针对性治疗。
链接:http://www.lewenyixue.com/2024/11/26/Sci%20Adv%E4%B8%A8%E5%BE%90%E5%BF%97%E7%88%B1%E5%9B%A2%E9%98%9F%E5%BC%80%E5%8F%91%E7%82%B9%E5%87%BB%E5%9E%8BPD/
THE END






赶快来坐沙发