免疫疗法爆发多年后,癌症治疗的现状如何?
癌症是世界上每个国家的主要死亡原因之一。 随着人口的快速增长、以及吸烟和食用超加工食品等不健康习惯的养成,全球癌症的发病率和死亡率正在增加。
根据美国癌症协会的数据,1991年美国癌症死亡率最高。自1991年以来,癌症死亡率下降了33%。美国癌症研究协会(AACR)报告称,2016年至2019年期间,癌症死亡率下降了2.3%。从2015年到2019年,美国男性和女性的总体癌症死亡率分别下降了2.3%和1.9%[1]。在此期间,男性11种癌症和女性14种癌症的死亡率下降。黑色素瘤和肺癌的死亡率每年下降超过 4%。1991年至2019年期间,美国预防了350万人死于癌症。癌症死亡率下降的主要原因是新的癌症治疗方法、癌症筛查测试和烟草使用的减少。
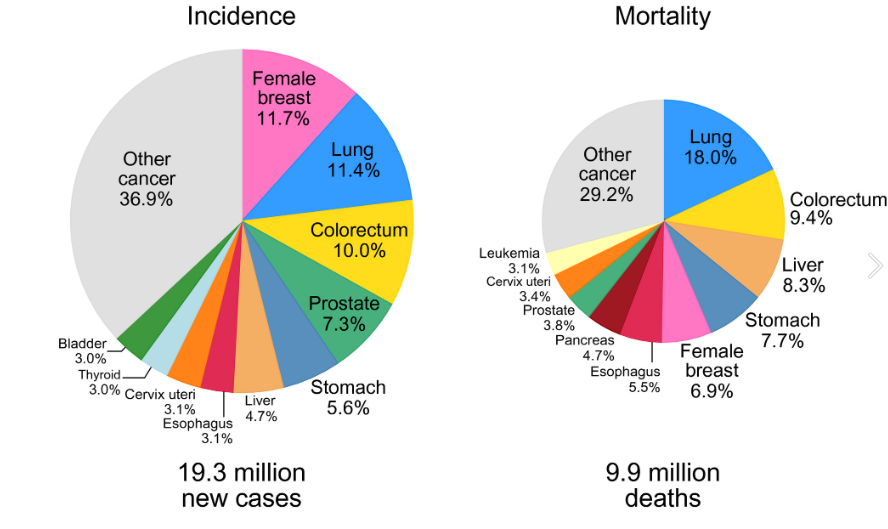
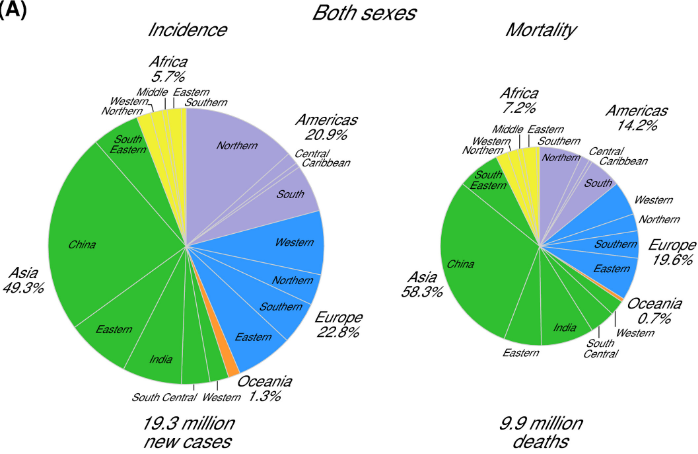
根据GLOBOCAN2020,全球新发癌症病例数为1930万,癌症死亡人数约为1000万[2]。最常诊断的癌症是女性乳腺癌。全球新诊断出 230万乳腺癌病例。其他常见的癌症包括胃癌、肺癌、前列腺癌和结直肠癌。肺癌导致的癌症死亡人数最多。大约180万人死于肺癌。其他导致大量死亡的癌症包括乳腺癌、结直肠癌、胃癌和肝癌。2020年,中国有300万人死于癌症,占全球癌症相关死亡人数的30.2%。
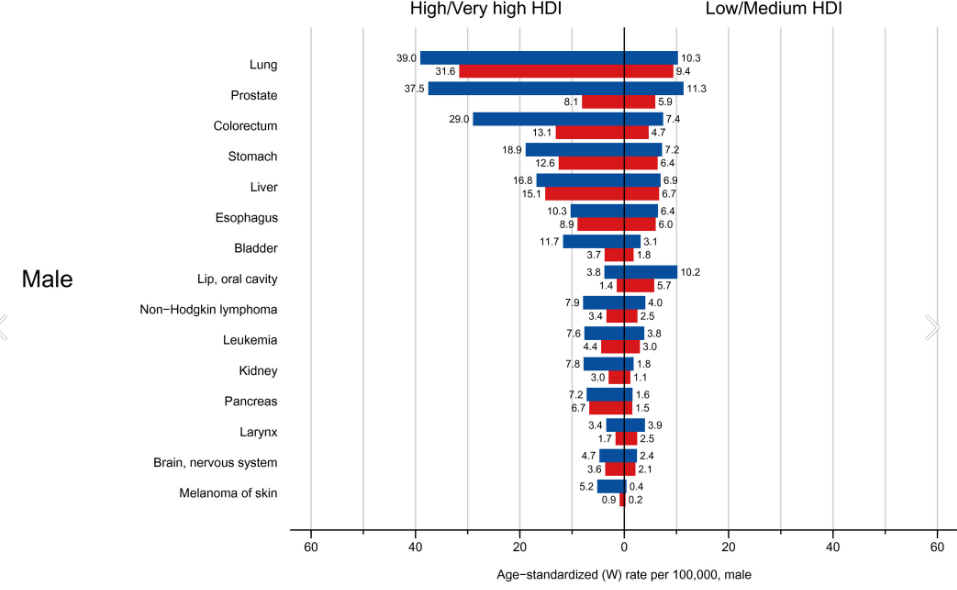
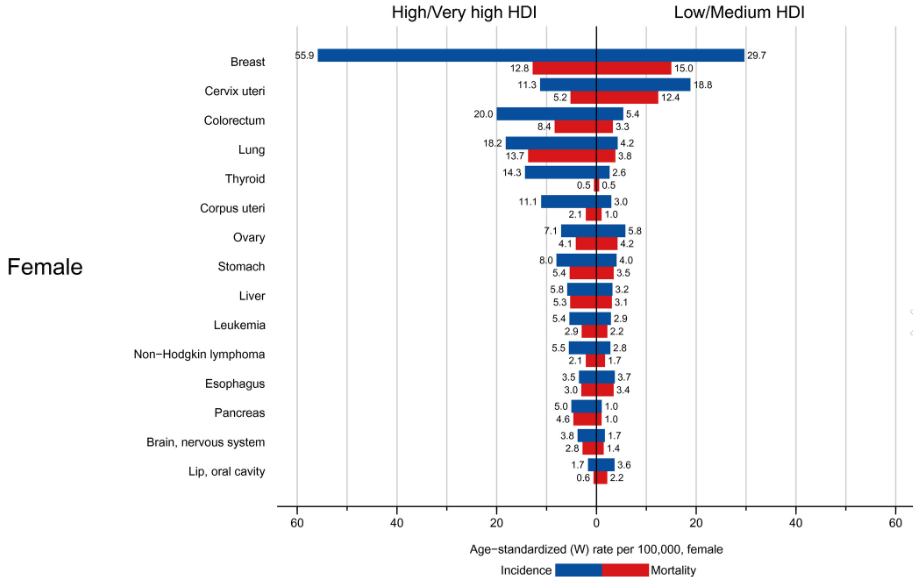
高/极高人类发展指数(HDI)国家和低/中HDI国家的癌症发病率和死亡率(图源:文献2)
1995年至2014年间,加拿大、英国、新西兰、澳大利亚、挪威、爱尔兰和丹麦等高收入国家大多数癌症的1年和5年净生存率有所增加[3]。英国NHS报告称,从2005年到2020年,总体第一年生存率增加了9%。癌症的生存率因国家而异。发展中国家和发达国家的白血病5年净生存率存在很大差异。在加拿大、澳大利亚和比利时,白血病的 5年净生存率超过85%,而在墨西哥,5年净生存率为46%[4]。
诊断时年龄低于75岁的年轻人的癌症生存率显着提高,因为他们能够耐受化疗和积极治疗。胰腺癌、食道癌、肺癌和胃癌等预后不良的癌症的生存率也显着提高。全直肠系膜切除等新手术技术提高了直肠癌的生存率。使用PET-CT成像对癌症进行诊断和分期,以及使用分子标记来选择患者进行靶向治疗也提高了多种癌症的生存率。
由于癌症的早期发现和缓慢生长的癌症的识别,癌症的存活率被夸大了。只有当疾病负担减轻时,癌症存活率的提高才表明抗击癌症取得了进展。从 2001年到2018年,美国神经内分泌胰腺癌和腺癌的五年生存率有所增加,但这两种癌症的发病率和死亡率也有所增加。从1975年到2010年,美国结直肠癌和霍奇金淋巴瘤的五年生存率有所增加[5]。在此期间,这两种癌症的死亡率和疾病负担有所下降,这表明针对这两种癌症的治疗取得了进展。
在过去的十年里,免疫疗法改变了癌症治疗,并帮助降低了癌症死亡率。免疫疗法是增强患者免疫系统靶向和破坏癌细胞能力的癌症治疗方法。免疫疗法可以静脉内、局部或口服给予。免疫检查点抑制剂是免疫治疗药物,已用于治疗不同类型的癌症,如肺癌、肾细胞癌和黑色素瘤。
免疫检查点抑制剂可防止检查点蛋白与伴侣蛋白结合。免疫检查点抑制剂分为三类:细胞毒性T淋巴细胞抗原4 (CTLA-4)抑制剂、程序性细胞死亡蛋白1 (PD-1)抑制剂和程序性细胞死亡配体1 (PDL-1)抑制剂。Pembrolizumab和Nivolumab是PD-1抑制剂。Ipilimumab是一种CTLA-4抑制剂,Avelumab和Atezolizumab是PDL-1抑制剂。2011年,ipilimumab成为第一个获得FDA批准的免疫检查点抑制剂。它被批准用于转移性黑色素瘤患者。免疫检查点抑制剂也非常昂贵,患者每年必须花费15万至25万美元才能接受这种治疗。在贫穷国家很少有人能获得这种治疗。某些类型的癌症,例如胶质母细胞瘤和胰腺癌,对免疫疗法没有反应。免疫疗法可以提高生存率和缓解率,但不能提高治愈率。
《美国医学会杂志》上发表的一项研究报告称, 适合使用免疫检查点抑制剂药物的癌症患者百分比以及对这些药物有反应的患者百分比有所增加[6] 。2011年,1.54%的癌症患者符合服用免疫检查点抑制剂的条件。2018年,43.63%的癌症患者符合服用免疫检查点抑制剂的条件。同样,2011年有0.14%的癌症患者对免疫检查点抑制剂有反应。2018年有12.46%的癌症患者对免疫检查点抑制剂有反应。
在发达国家,黑色素瘤的癌症死亡率急剧下降。2013年,荷兰黑色素瘤患者的中位总生存期为11.8个月。2018年,黑色素瘤患者的中位总生存期为21.1个月[7]。2010年至2019年间,美国新发黑色素瘤病例每年增加1.2%,但黑色素瘤死亡率下降了3.2%。黑色素瘤通常影响白人,2013年至2016年,美国白人的黑色素瘤总体死亡率下降了17.9%。接受nivolumab治疗的既往未治疗黑色素瘤患者的1年总生存率为72.9%[8]。Nivolumab和Ipilimumab的组合在晚期黑色素瘤患者的5年总生存率达到52%[9]。
免疫疗法还导致肺癌死亡率急剧下降。根据美国肺脏协会的数据,NSCLC的五年生存率已从14%增加至23.7%[10]。 一旦免疫治疗药物的适应症扩大,肺癌的生存率将进一步提高。接受免疫检查点抑制剂治疗的NSCLC患者的总生存期比接受化疗的患者更长[11]。
《JAMAOncology》发表的一项研究显示,2011年年龄小于55岁的晚期非小细胞肺癌(NSCLC)患者的2年生存率为37.7%[12]。2018年的2年生存率为50.3%。对于75岁或以上的患者,2011年的2年生存率为30.6%。2018年的2年生存率为36.2%。该研究还报道,使用近年来,免疫检查点抑制剂在肺癌患者中的使用也有所增加。2015年,4.7%的晚期NSCLC患者使用免疫检查点抑制剂。2019年,晚期NSCLC患者使用免疫检查点抑制剂的比例为45.6%。接受nivolumab治疗的可切除NSCLC患者的5年总生存率(OS)和无复发生存率(RFS)分别为80%和60%[13]。
在一项3期试验KEYNOTE-189中,转移性NSCLC患者被随机给予铂类药物和培美曲塞联合pembrolizumab或安慰剂。接受pembrolizumab和安慰剂的患者12个月时的总生存率分别为69.2%和49.4%[14]。在3期试验KEYNOTE-024中,接受pembrolizumab和化疗的NSCLC患者5年总生存率分别为31.9%和16.3%[15]。
接受pembrolizumab联合铂类化疗和培美曲塞的非鳞状NSCLC患者的5年总生存率为19.4%。相比之下,接受安慰剂联合铂类化疗和培美曲塞的患者的5年总生存率为11.3%[16]。接受pembrolizumab联合卡铂和紫杉醇或白蛋白结合型紫杉醇治疗的鳞状NSCLC患者的5年总生存率为18.4%。相比之下,接受卡铂加紫杉醇或白蛋白结合型紫杉醇安慰剂的患者的5年总生存率为9.7%。
在临床试验中,免疫治疗药物也提高了其他癌症的生存率。Nivolumab可显着提高头颈癌患者的生存率。接受nivolumab和标准化疗的患者1年生存率分别为36.0%和16.6%[17]。Nivolumab和Ipilimumab联合治疗晚期肾细胞癌18个月总生存率达到75%[18]。
在3期试验JAVELINBladder 100中,接受avelumab的尿路上皮癌患者1年总生存率为71.3%。那些未接受该药物的患者的1年总生存率为58.4%[19]。在3期试验KEYNOTE-826中,pembrolizumab在宫颈癌患者中的2年总生存率达到50.4%[20]。接受pembrolizumab治疗的食管癌患者的12个月总生存率为43%[21]。在不可切除的肝细胞癌患者中,Atezolizumab和抗血管生成药物贝伐珠单抗联合使用12个月总生存率达到67.2%[22]。接受nivolumab治疗的肾细胞癌(RCC)患者的5年总体生存率为27.7%[23]。
在发达国家,癌症存活率一直在增加。近年来,使用免疫检查点抑制剂等免疫治疗药物的患者数量有所增加。因此,免疫检查点抑制剂显着提高了晚期黑色素瘤和肺癌的生活质量和生存率。
[1]Cronin, K. A., Scott, S., Firth, A. U., Sung, H., Henley, S. J., Sherman, R. L., ... & Jemal, A. (2022). Annual report to the nation on the status of cancer, part 1: National cancer statistics. Cancer, 128(24), 4251-4284.
[2]Sung, H., Ferlay, J., Siegel, R. L., Laversanne, M., Soerjomataram, I., Jemal, A., & Bray, F. (2021). Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: a cancer journal for clinicians, 71(3), 209-249.
[3] Arnold, M., Rutherford, M. J., Bardot, A., Ferlay, J., Andersson, T. M., Myklebust, T. Å., ... & Bray, F. (2019). Progress in cancer survival, mortality, and incidence in seven high-income countries 1995–2014 (ICBP SURVMARK-2): a population-based study. The Lancet Oncology, 20(11), 1493-1505.
[4] Ssenyonga, N., Stiller, C., Nakata, K., Shalkow, J., Redmond, S., Bulliard, J. L., ... & Alverson, G. (2022). Worldwide trends in population-based survival for children, adolescents, and young adults diagnosed with leukaemia, by subtype, during 2000–14 (CONCORD-3): analysis of inpidual data from 258 cancer registries in 61 countries. The lancet child & adolescent health, 6(6), 409-431.
[5] Cho, H., Mariotto, A. B., Schwartz, L. M., Luo, J., & Woloshin, S. (2014). When do changes in cancer survival mean progress? The insight from population incidence and mortality. Journal of the National Cancer Institute Monographs, 2014(49), 187-197.
[6] Haslam, A., & Prasad, V. (2019). Estimation of the percentage of US patients with cancer who are eligible for and respond to checkpoint inhibitor immunotherapy drugs. JAMA network open, 2(5), e192535-e192535.
[7] Franken, M. G., Leeneman, B., Aarts, M. J. B., van Akkooi, A. C. J., van den Berkmortel, F. W. P. J., Boers-Sonderen, M. J., ... & Uyl-de Groot, C. A. (2021). Trends in survival and costs in metastatic melanoma in the era of novel targeted and immunotherapeutic drugs. ESMO open, 6(6), 100320.
[8] Robert, C., Long, G. V., Brady, B., Dutriaux, C., Maio, M., Mortier, L., ... & Ascierto, P. A. (2015). Nivolumab in previously untreated melanoma without BRAF mutation. New England journal of medicine, 372(4), 320-330.
[9]Larkin, J., Chiarion-Sileni, V., Gonzalez, R., Grob, J. J., Rutkowski, P., Lao, C. D., ... & Wolchok, J. D. (2019). Five-year survival with combined nivolumab and ipilimumab in advanced melanoma. New England Journal of Medicine, 381(16), 1535-1546.
[10] Ferreira, M., & Reckamp, K. L. (2022). Impact of immunotherapy in lung cancer. Frontiers in Oncology, 12, 1083524.
[11] Ruiz‐Patiño, A., Arrieta, O., Cardona, A. F., Martín, C., Raez, L. E., Zatarain‐Barrón, Z. L., ... & CLICaP. (2020). Immunotherapy at any line of treatment improves survival in patients with advanced metastatic non‐small cell lung cancer (NSCLC) compared with chemotherapy (Quijote‐CLICaP). Thoracic Cancer, 11(2), 353-361.
[12] Voruganti, T., Soulos, P. R., Mamtani, R., Presley, C. J., & Gross, C. P. (2023). Association between age and survival trends in advanced non–small cell lung cancer after adoption of immunotherapy. JAMA oncology, 9(3), 334-341.
[13] Rosner, S., Reuss, J. E., Zahurak, M., Zhang, J., Zeng, Z., Taube, J., ... & Forde, P. M. (2023). Five-year clinical outcomes after neoadjuvant nivolumab in resectable non–small cell lung cancer. Clinical Cancer Research, 29(4), 705-710.
[14] Gandhi, L., Rodríguez-Abreu, D., Gadgeel, S., Esteban, E., Felip, E., De Angelis, F., ... & Garassino, M. C. (2018). Pembrolizumab plus chemotherapy in metastatic non–small-cell lung cancer. New England journal of medicine, 378(22), 2078-2092.
[15] Reck, M., Rodríguez-Abreu, D., Robinson, A. G., Hui, R., Csőszi, T., Fülöp, A., ... & Brahmer, J. R. (2021). Five-year outcomes with pembrolizumab versus chemotherapy for metastatic non–small-cell lung cancer with PD-L1 tumor proportion score≥ 50%. Journal of Clinical Oncology, 39(21), 2339.
[16] Garassino, M. C., Gadgeel, S., Speranza, G., Felip, E., Esteban, E., Dómine, M., ... & Rodríguez-Abreu, D. (2023). Pembrolizumab plus pemetrexed and platinum in nonsquamous non–small-cell lung cancer: 5-year outcomes from the phase 3 KEYNOTE-189 study. Journal of Clinical Oncology, 41(11), 1992.
[17] Ferris, R. L., Blumenschein Jr, G., Fayette, J., Guigay, J., Colevas, A. D., Licitra, L., ... & Gillison, M. L. (2016). Nivolumab for recurrent squamous-cell carcinoma of the head and neck. New England Journal of Medicine, 375(19), 1856-1867.
[18] Larkin, J., Chiarion-Sileni, V., Gonzalez, R., Grob, J. J., Rutkowski, P., Lao, C. D., ... & Wolchok, J. D. (2019). Five-year survival with combined nivolumab and ipilimumab in advanced melanoma. New England Journal of Medicine, 381(16), 1535-1546.
[19] Powles, T., Park, S. H., Voog, E., Caserta, C., Valderrama, B. P., Gurney, H., ... & Grivas, P. (2020). Avelumab maintenance therapy for advanced or metastatic urothelial carcinoma. New England Journal of Medicine, 383(13), 1218-1230.
[20] Colombo, N., Dubot, C., Lorusso, D., Caceres, M. V., Hasegawa, K., Shapira-Frommer, R., ... & Monk, B. J. (2021). Pembrolizumab for persistent, recurrent, or metastatic cervical cancer. New England Journal of Medicine, 385(20), 1856-1867.
[21] Kojima, T., Shah, M. A., Muro, K., Francois, E., Adenis, A., Hsu, C. H., ... & KEYNOTE-181 Investigators. (2020). Randomized phase III KEYNOTE-181 study of pembrolizumab versus chemotherapy in advanced esophageal cancer. Journal of Clinical Oncology, 38(35), 4138-4148.
[22] Finn, R. S., Qin, S., Ikeda, M., Galle, P. R., Ducreux, M., Kim, T. Y., ... & Cheng, A. L. (2020). Atezolizumab plus bevacizumab in unresectable hepatocellular carcinoma. New England Journal of Medicine, 382(20), 1894-1905.
[23] Topalian, S. L., Hodi, F. S., Brahmer, J. R., Gettinger, S. N., Smith, D. C., McDermott, D. F., ... & Sznol, M. (2019). Five-year survival and correlates among patients with advanced melanoma, renal cell carcinoma, or non–small cell lung cancer treated with nivolumab. JAMA oncology, 5(10), 1411-1420.
版权声明:本文为“乐问号”作者或机构在乐问医学上传并发布,仅代表该作者或机构观点,不代表乐问医学的观点或立场,不能作为个体诊疗依据,如有不适,请结合自身情况寻求医生的针对性治疗。
链接:http://www.lewenyixue.com/2024/11/20/%E5%85%8D%E7%96%AB%E7%96%97%E6%B3%95%E7%88%86%E5%8F%91%E5%A4%9A%E5%B9%B4%E5%90%8E%EF%BC%8C%E7%99%8C%E7%97%87%E6%B2%BB%E7%96%97%E7%9A%84%E7%8E%B0%E7%8A%B6%E5%A6%82%E4%BD%95%EF%BC%9F/
THE END










赶快来坐沙发