NEJM丨以inavolisib为基础的PIK3CA突变晚期乳腺癌治疗
撰文丨菠萝西瓜
研究表明约35%至40%的激素受体阳性乳腺癌会发生PIK3CA激活突变。此类突变的存在是晚期乳腺癌患者的不良预后因素,也是对磷脂酰肌醇3-激酶 (PI3K) 抑制剂反应的预测生物标志物。临床试验表明,针对激素受体阳性乳腺癌的关键致癌驱动因子的方案对患者有疗效,主要包括内分泌疗法联合细胞周期蛋白依赖性激酶4和6 (CDK4/6) 抑制剂或PI3K-蛋白激酶B-哺乳动物雷帕霉素靶点 (PI3K-AKT-mTOR) 信号通路节点抑制剂;然而,治疗耐药性仍然是临床实践中的一大挑战。驱动激素受体阳性局部晚期或转移性乳腺癌的三种关键致癌途径 (雌激素受体、CDK4/6和PI3K) 高度相互关联,具有复杂的反馈机制,可能导致适应和对治疗的抵抗。基于此,需要一种有效的、具有可接受安全水平的、针对所有三种信号通路的治疗方案。临床前研究表明,在PIK3CA突变的异种移植模型中,同时阻断雌激素受体、CDK4/6和PI3K通路可以实现显着的协同作用,从而进一步减少肿瘤负荷并防止或延缓对治疗的抵抗力的出现。然而,以往在临床上使用这种方法并不成功,主要是因为与治疗相关的副作用。inavolisib是一种高效选择性抑制剂,可抑制PI3K复合物p110催化亚基的α异构体,还可促进突变p110α的降解。以前的PI3K抑制剂与标准治疗药物联合使用时会产生毒性作用和不可接受的副作用。而inavolisib可增强对p110α的选择性抑制和对突变p110α的降解,从而扩大治疗窗口,使inavolisib可与标准治疗疗法联合使用,以实现持续的通路抑制。一项首次人体I期研究 (ClinicalTrials.gov编号为NCT03006172) 表明,inavolisib可与哌柏西利 (palbociclib) 和氟维司群 (fulvestrant) 联合使用,每种药物的最大单药剂量均未发生药物间相互作用,副作用可接受,并且在PIK3CA突变、激素受体阳性、人表皮生长因子受体2 (HER2) 阴性的局部晚期或转移性乳腺癌中具有良好的初步抗肿瘤活性。
近日,来自英国伦敦Royal Marsden Hospital and Institute of Cancer Research的 Nicholas C. Turner教授携临床团队在 The New England Journal of Medicine 杂志上发表文章 Inavolisib-Based Therapy in PIK3CA-Mutated Advanced Breast Cancer 。 本临床结果显示,对于PIK3CA突变、激素受体阳性、HER2阴性的局部晚期或转移性乳腺癌患者,inavolisib联合哌柏西利-氟维司群治疗组的无进展生存期显著长于安慰剂联合哌柏西利-氟维司群治疗组,但毒性作用发生率与之较高。整体上因不良事件而停用任何试验药物的患者比例较低。
试验设计:INAVO120试验招募了来自28个国家的患者。患有PIK3CA突变、激素受体阳性、HER2阴性局部晚期或转移性乳腺癌的绝经前、绝经期或绝经后女性或男性均符合入选条件。其他入选标准包括辅助内分泌治疗期间或完成治疗后12个月内出现疾病复发或进展 (排除原发转移性乳腺癌患者) 、空腹血糖水平低于126 mg/dL、糖化血红蛋白水平低于6.0%、根据《实体肿瘤疗效评价标准》 (RECIST) 1.1版有可测量病变。按1:1的比例将患者随机分配接受inavolisib (剂量为9 mg,口服,每日1次,每个28天周期的第1至28天) 或安慰剂 (每日1次) 治疗,每组均联合使用哌柏西利 (剂量为125 mg,口服,每日1次,每个28天周期的第1至21天) 和氟维司群 (剂量为500 mg,肌肉注射,第1周期的第1天和第15天以及此后大约每28天一次) 。绝经前或围绝经期女性和男性在试验干预期间接受促黄体激素释放激素激动剂治疗以抑制激素。试验药物的给药持续至出现疾病进展、不可接受的毒性作用、患者撤回知情同意或死亡。
临床终点:主要终点是无进展生存期,定义为从随机分组到首次出现疾病进展或任何原因死亡 (以先发生者为准) 的时间。未出现疾病进展或任何原因死亡的患者的数据在最后一次肿瘤评估时截止。次要终点包括总生存期;经证实的客观缓解、最佳总体缓解、临床益处和缓解持续时间;以及患者报告的结果。还评估了安全性、不可接受的副作用和药代动力学。
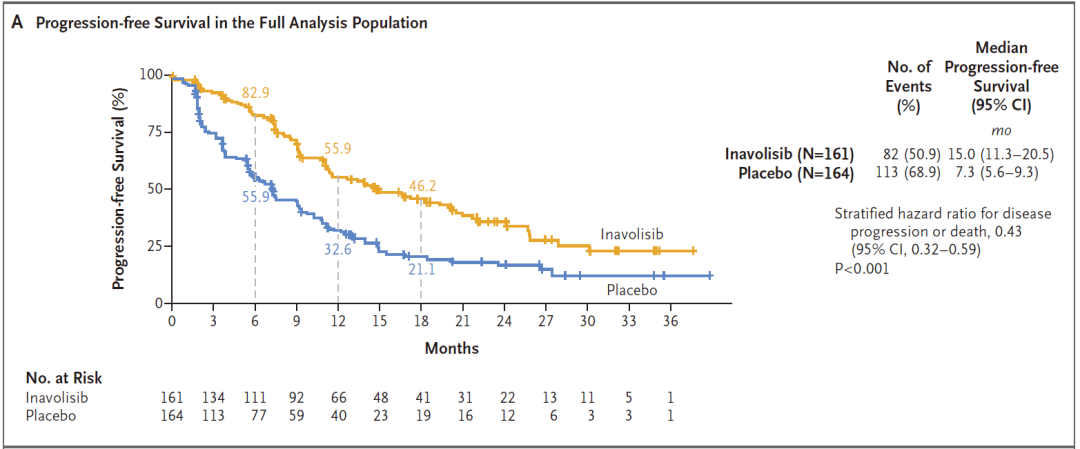
临床结果:本临床试验共计161名患者被分配至inavolisib组,164名患者被分配至安慰剂组;中位随访时间分别为21.3个月和21.5个月。inavolisib组和安慰剂组的中位无进展生存期分别为15.0个月 (95% CI,11.3至20.5) ,而安慰剂组为7.3个月 (95% CI,5.6至9.3)(HR=0.43;95% CI,0.32至0.59;P<0.001) 。inavolisib组58.4%的患者出现客观缓解,而安慰剂组为25.0%。inavolisib组3级或4级中性粒细胞减少症的发生率为80.2%,而安慰剂组为78.4%;3级或4级高血糖,分别为5.6%和0%;3级或4级口腔炎或黏膜炎症,分别为5.6%和0%;3级或4级腹泻,分别为3.7%和0%。未观察到3级或4级皮疹。因不良事件而停用任何试验药物的患者在inavolisib组占6.8%,在安慰剂组占0.6%。
由此,本临床试验表明,对于PIK3CA突变、激素受体阳性、HER2阴性的局部晚期或转移性乳腺癌患者,inavolisib联合哌柏西利-氟维司群治疗组的无进展生存期显著长于安慰剂联合哌柏西利-氟维司群治疗组,但毒性作用发生率与之较高。但整体因不良事件而停用任何试验药物的患者比例较低。 (本临床试验由F. Hoffmann-La Roche资助;INAVO120 ClinicalTrials.gov编号为NCT04191499。)
原文链接:https://doi.org/10.1056/NEJMoa2404625
制版人:十一
链接:http://www.lewenyixue.com/2024/11/19/NEJM%E4%B8%A8%E4%BB%A5inavolisib%E4%B8%BA%E5%9F%BA%E7%A1%80%E7%9A%84/






赶快来坐沙发