Nature | 针对ecDNA阳性肿瘤的新型治疗策略–CHK1抑制剂曙光乍现
导语:ecDNA(外染色体DNA)的遗传物质因其在肿瘤发展和治疗抗性中的重要作用而成为研究的热点。最近,一项发表在《自然》杂志上的研究通过增强转录-复制冲突来选择性地消除含有ecDNA的肿瘤细胞,为我们提供了新的治疗策略。
外染色体DNA(ecDNA)是肿瘤研究中的一个新兴热点,是一种在肿瘤细胞中独立于常规染色体存在的DNA分子,与肿瘤的侵袭性、治疗抗性和快速进化密切相关。ecDNA因其能够大量扩增致癌基因(oncogene)的表达而备受关注,这种扩增与多种肿瘤类型的预后不良有关。尽管ecDNA在肿瘤发展中的重要性日益凸显,但目前尚无针对ecDNA的特效治疗手段。
以往的研究表明,ecDNA具有独特的生物学特性,例如高度可及的染色质结构和增强的致癌基因表达,这些特性为肿瘤细胞提供了适应性优势。此外,ecDNA的圆形结构和开放的染色质环境导致了异常的转录活性和基因表达,但如何利用这一特点进行治疗,但同时也是挑战。此外,ecDNA阳性肿瘤细胞在面对DNA损伤和复制应激时表现出更高的依赖性,这为开发新的治疗策略提供了潜在的靶点。
2024年11月, Nature 发表了题为“Enhancing transcription–replication conflict targets ecDNA-positive cancers”的研究,探索通过增强转录与复制冲突,靶向消灭ecDNA的肿瘤细胞,为开发针对ecDNA阳性肿瘤的新型治疗药物提供科学依据。

研究设计
研究采用了一系列的分子生物学和遗传学方法来探索ecDNA的特性。研究者们首先通过全球运行-on测序(GRO-seq)和核糖体RNA(rRNA)耗尽的RNA测序(Ribo-Zero)来分析ecDNA的转录情况。接着,利用kethoxal辅助的单链DNA测序(KAS-seq)来评估ecDNA上的单链DNA积累。此外,还使用了一系列的细胞培养、药物处理、基因敲除和动物模型实验来验证假设。包括了对ecDNA阳性和阴性的肿瘤细胞株的比较,以及对特定药物(如 CHK1抑制剂BBI-2779)的敏感性测试。
研究结果
研究结果表明,ecDNA上的转录活性显著增强,导致了复制应激的增加。与染色体位点相比,ecDNA上的复制叉速度更慢,复制应激更高。研究者们发现,通过抑制CHK1(一种细胞周期检查点激酶),可以显著增加ecDNA阳性肿瘤细胞的死亡,并开发了一种高选择性、强效且生物可用的口服CHK1抑制剂BBI-2779,该药物能够选择性地杀死含有ecDNA的肿瘤细胞。在动物模型中,BBI-2779不仅抑制了肿瘤生长,还有效抑制了ecDNA介导的对泛FGFR抑制剂Infigratinib的获得性抗性。
ecDNA的广泛转录与单链DNA积累
研究发现,与染色体位点相比,ecDNA区域的RNA转录普遍增加,涉及编码和非编码区域,包括之前未注释的转录本(图1c,d)。这种广泛的转录增加是ecDNA特有的,因为GRO-seq和Ribo-Zero测序读数在COLO320DM和COLO320HSR的染色体上是可比的。此外,ecDNA区域的转录活性与H3K36me3组蛋白标记相关联,该标记与RNA聚合酶II延伸相关,从而验证了广泛的转录活动(图1c,e和扩展数据图3a)。研究还发现,ecDNA区域的单链DNA积累增加,这与转录过程、RNA:DNA杂交体和转录-复制冲突有关(图1b,c)。

图1 ecDNA上的频繁转录驱动ssDNA积累
ecDNA上的转录-复制冲突导致的复制应激(RS)
研究进一步探讨了ecDNA上的转录-复制冲突对复制叉速度的影响。通过结合DNA纤维实验和DNA荧光原位杂交(FISH)技术,研究者发现ecDNA上的复制叉速度比染色体上的相应序列慢(图2c)。此外,通过免疫荧光(IF)检测pRPA2-S33(复制应激的一个标记),发现ecDNA阳性肿瘤细胞的复制应激显著增加(扩展数据图4b)。特别是在EdU阳性细胞中,ecDNA上的复制应激更高,表明在活跃复制的细胞中,ecDNA上的复制应激更为显著(图2e)。

图2 转录-复制冲突在额ecDNA上产生RS
ecDNA阳性肿瘤细胞对CHK1抑制剂的敏感性
研究者假设ecDNA阳性肿瘤细胞由于其内在的高复制应激,可能对CHK1抑制剂(CHK1i)更加敏感。通过CRISPR技术敲除CHK1基因,发现ecDNA阳性的HeLa细胞比对照组细胞显示出更高的生长抑制(图3c)。药理学上,使用CHIR-124抑制CHK1后,ecDNA阳性肿瘤细胞比对照组细胞更敏感,COLO320DM细胞的半抑制浓度(IC50)大约是COLO320HSR细胞的四倍(图3d)。这一发现通过三种结构不同的CHK1抑制剂得到了验证。

图3 ecDNA肿瘤细胞中CHK1的抑制
口服CHK1抑制剂BBI-2779的抗肿瘤效果
研究者开发了一种新的口服CHK1抑制剂BBI-2779,并在体外和体内模型中验证了其效果。BBI-2779在体外显示出对CHK1的强效抑制作用,其生化抑制IC50为0.3 nM,细胞内诱导复制应激的IC50为3 nM(表1)。在动物模型中,BBI-2779显示出良好的生物利用度和药物暴露量(表2)。更重要的是,BBI-2779与泛FGFR抑制剂Infigratinib联合使用时,能够显著抑制FGFR2-amplified ecDNA阳性胃癌SNU16异种移植瘤的生长,并防止了单药Infigratinib治疗后肿瘤细胞对Infigratinib的获得性抗性(图4e,f)。
表1 BBI-2779和参考化合物

表2 BBI-2779在小鼠体内具有良好的耐受性

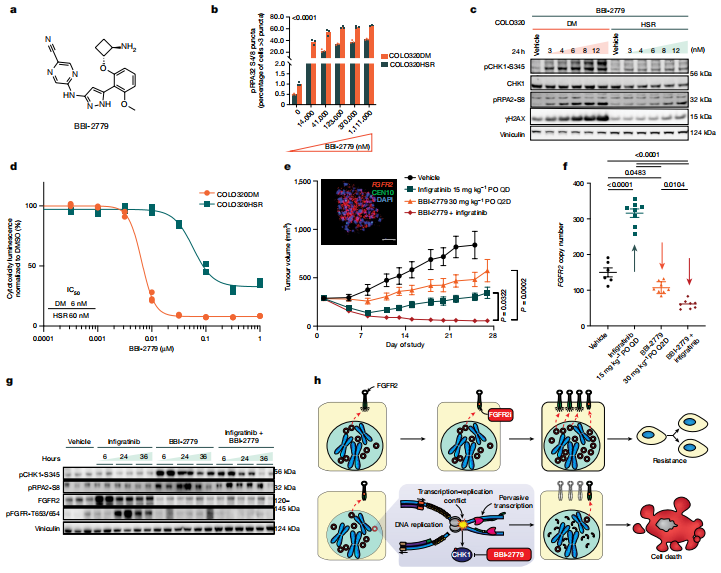
图4口服CHK1i与泛FGFRi联合使用显示出协同作用
总结讨论
本研究指出,通过增强转录-复制冲突,我们可以开发出针对ecDNA阳性肿瘤的新型治疗策略。这一策略不仅为肿瘤治疗提供了新的靶点,还展示了如何利用肿瘤细胞的特定生物学特性来开发治疗药物。尽管这一发现具有重要的临床潜力,但还需要进一步的临床试验来验证这些初步结果,并确定最佳的治疗策略。此外,研究者们还指出,这种治疗策略可能与其他靶向治疗相结合,以提高治疗效果并克服治疗抗性。总的来说,这项研究为ecDNA阳性肿瘤的治疗提供了新的视角和希望。
参考文献
TANG J, WEISER N E, WANG G, et al. Enhancing transcription-replication conflict targets ecDNA-positive cancers[J]. Nature. 2024; 635(8037): 210-218. DOI:10.1038/s41586-024-07802-5.
链接:http://www.lewenyixue.com/2024/11/18/Nature%20%7C%20%E9%92%88%E5%AF%B9ecDNA%E9%98%B3%E6%80%A7%E8%82%BF%E7%98%A4/