【CACA周刊】81期 四阴性乳腺癌——渴望独立的新亚型
本期看点
序言
三阴性乳腺癌(TNBC)是乳腺肿瘤中最具有侵袭性的一种乳腺癌亚型,从数据上看,这种恶性肿瘤更“偏爱”年轻女性尤其是中国的年轻女性。
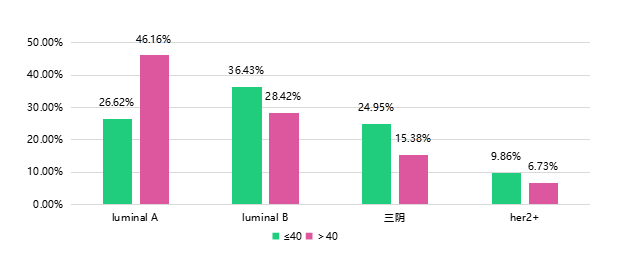
美国年轻与非年轻乳腺癌患者分子分型占比
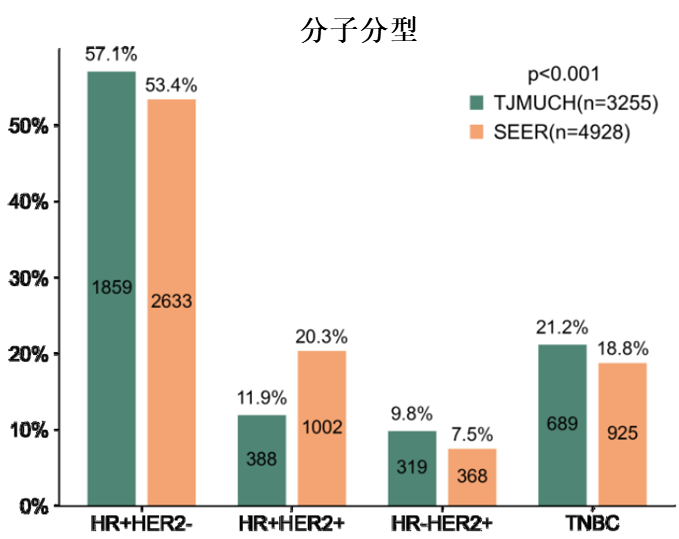
中西方年轻乳腺癌患者分子分型占比(中国为绿色)
随着乳腺癌研究的逐渐深入,雄激素受体(AR)逐渐成为重要靶点。一些研究显示,AR与良好预后相关;但也有研究得出了截然不同的结论。究其原因,AR表达的评判标准、乳腺癌亚型不同以及研究人群的差异都可能影响AR对预后的预测效果。
AR作为类固醇受体超家族的一员,更常见于男性特有的前列腺癌。AR在70%~90%的乳腺癌中表达,与ER存在串扰,在TNBC中的表达最少。不过,尽管部分TNBC患者AR表达较低,但其接受抗雄激素疗法如比卡鲁胺、醋酸阿比特龙+泼尼松、恩杂鲁胺联合化疗仍有获益 [1] 。
尽管AR在乳腺癌中的预后作用存在争议,但鉴于越来越多的数据显示QNBC比AR阳性肿瘤更具侵袭性和有更差的预后,国内许多学者认为应当将四阴性乳腺癌(QNBC)定为乳腺癌的一个独立的亚型并开展相关研究标准化乳腺癌的AR检测,以便改善中国乳腺癌患者生存预后。
目前评价AR表达水平的主要手段是免疫组化染色,主要以1%或10%作为AR表达的阈值。更精细的阈值选择有助于识别可从抗雄激素治疗中获益的那部分患者。其他检测手段包括近年来发展迅速的液体活检,该方法通过检测体液中循环肿瘤细胞DNA中AR的拷贝数、突变和剪接变异等都可用来指导临床治疗。
相比于AR阳性,AR阴性TNBC表现出更差的OS。后者在TNBC中的占比为63%~87%,具体取决于AR阴性的评价标准 [2]。AR对预后的不确定影响可能与转录本的结构重排或选择性剪接有关,也与人种相关。非洲血统的女性AR阴性的概率更高,发病年龄更小,进展时间和OS比欧洲血统的女性差,具有独特的分子表达特征。
由于基因表达特征的差异,QNBC的化疗方案需要进一步研究。将它简单归类为AR阴性TNBC可能是不合理的,二者之间生物标志物的差异性表达可能会赋予QNBC新的可操作靶点,使这部分乳腺癌患者获益。
有研究通过TCGA数据库分析指出,与其他亚型相比,QNBC有着更高的抗肿瘤相关基因的表达上调。因此,免疫治疗有望在QNBC中取得更优的疗效,带来了更多“生”的希望。
在靶向治疗领域,QNBC相比于AR阳性的TNBC,EGFR、Ki-67、CDK6、TOPO2A以及ACSL4等的表达高度上调,或许可以开发成为新的靶点。
此外,今年的“诺奖新秀”——microRNA以及一众表观遗传修饰在QNBC的发展中也起到了重要作用。虽然现有的表观遗传药物效果有限,山雨欲来风满楼的“悸动”已经出现,表观遗传药物未来可期,极有可能成为肿瘤治疗的下一个“爆点”。
目前,QNBC作为一种“全新”的乳腺癌形式正逐渐浮出水面,要求其成为独立亚型的呼声越来越高。但国内暂时仍缺乏QNBC的生物学、流行病学以及相关临床药物研究。
综合来看,随着我国乳腺癌发病年轻化以及三阴性乳腺癌对年轻女性的“偏爱”,QNBC的威胁正日益凸显。目前已证实QNBC是细胞毒性化疗和免疫治疗的理想候选者,但其对紫杉烷类药物的获得性抗性也很常见,解决耐药问题也是提高患者预后的直接解决方案。
未来,除生物学特征、危险因素、流行病学和AR标准化评估,新药研发领域也需投入更多资源去探索QNBC的“敏感点”。
药事纵横
……
1-
10月1日, Nature Medicine :中国医学科学院肿瘤医院徐兵河院士公布Trop-2 ADC戈沙妥珠单抗治疗HR +HER2 -转移性乳腺癌的Ⅲ期EVER-132-002研究结果 [3]。
TROPiCS-02研究展现了戈沙妥珠单抗治疗HR +HER2 -转移性乳腺癌的优秀效果,显著改善了PFS和OS。然而,TROPiCS-02研究中亚洲患者较少。因此,本研究分析了EVER-132-002研究的亚洲患者结果,为我国乳腺癌患者用药提供更优证据。
入组患者被随机分配到戈沙妥珠单抗(n=166)和化疗(n=165)组。本研究达到了主要终点:与化疗相比,戈沙妥珠单抗显著改善了患者的中位PFS(4.3个月 vs 4.2个月,HR:0.67,95% CI:0.52~0.87, P =0.0028)和中位OS(21.0个月 vs 15.3个月,HR:0.64,95% CI:0.47~0.88, P =0.0061)。
研究中最常见的3级及以上AE是中性粒细胞减少、白细胞减少和贫血,安全性与既往研究一致。与化疗相比,戈沙妥珠单抗显著改善了PFS和OS。
2-
10月9日, Nature :NSCLC患者接受CTLA-4阻断可消除KEAP1/STK11对PD-(L)1抑制剂的耐药性 [4]。
对于晚期NSCLC患者,CTLA-4抑制剂和PD-(L)1抑制剂联合的双重ICB拥有更高的抗肿瘤活性和免疫相关毒性,但目前还没有经过验证的生物标志物来预测患者能否从双重免疫检查点抑制中获益。
研究者发现,在Ⅲ期POSEIDON研究中,STK11和/或KEAP1肿瘤抑制基因突变患者接受度伐利尤单抗+曲美木单抗联合化疗相比度伐利尤单抗联合化疗有更多临床获益。无偏倚的遗传学筛选确定这两个基因的确实是患者对PD-(L)1抑制剂耐药的独立驱动因素,而KEAP1缺失是双重ICB疗效增强的最强预测因子。
在小鼠模型中,KEAP1和STK11的改变与不良肿瘤微环境相关。肿瘤微环境的特征为抑制性髓系细胞占优势、CD8 +细胞毒性T细胞耗竭、CD4 +效应T细胞减少。双重ICB作用于CD4 +效应T细胞,将肿瘤髓样细胞区室重编程为表达iNOS的抗肿瘤亚型。
医谷回声
……
1-
10月15日, Nature Communications :浙江大学医学院附属第二医院肖乾教授利用血浆蛋白质组学和多基因分析改善结直肠癌风险分层和个性化筛查 [5]。
本研究旨在通过将蛋白质组学特征与遗传/非遗传因素(QCancer-15)相结合对结直肠癌发病进行预测来改进个性化初始筛查的风险分层和估计年龄。
研究采用两阶段策略,先考虑15种蛋白质生物标志物作为蛋白质风险评分(ProS)的预测因子,再将蛋白质组学概况与多基因风险评分(PRS)和QCancer-15风险评分(QCancer-S)相结合,构建风险预测模型。该模型性能相比单独的QCancer-S性能更好(训练集,C-statistic:0.79 vs 0.71, P =4.94×10 -3 ;验证集0.75 vs 0.69, P =5.49×10 -4 )。
该模型对结直肠癌发病风险进行了分层,建议ProS、PRS或综合风险评分较高的参与者在46岁、41岁或40岁之前开始筛查。

高峰科讯
……
1-
10月10日, Advanced Science :重庆医科大学附属第二医院周智航研究团队发现CPS1通过增加天冬氨酸水平调节HCC增殖与转移 [6]。
代谢重编程是癌症发生、发展过程的重要标志之一,研究团队想要分析氨甲酰磷酸合酶1(CPS1)在肝细胞癌中作用。
CPS1在HCC组织和循环肿瘤细胞中呈低表达,且与HCC分期和预后呈负相关。CPS1缺失导致天冬氨酸水平降低,进而增强了HCC的转移能力。CPS1一方面通过抑制磷脂酰胆碱特异性磷脂酶C活性来阻断二酰甘油(DAG)的生物合成,抑制癌细胞侵袭和转移;另一方面,通过增加细胞内S-腺苷甲硫氨酸水平来增强SLC1A3的m6A修饰,促进细胞增殖。
该研究提示癌细胞转移与CPS1缺失导致的胞内天冬氨酸水平下降有关,这为HCC治疗提供新的视角和潜在靶点。

2-
10月11日, Cell Death&Disease :福建医科大学附属协和医院研究团队发现cNEK6通过SNRPA/PPA2c/mTORC1轴促进PDAC的糖酵解,诱导吉西他滨耐药 [7]。
目前缺乏判断PDAC对吉西他滨耐药与否的生物标志物和新的化疗增敏策略。
研究人员建立了吉西他滨耐药细胞系,通过circRNA测序分析,观察到cNEK6在吉西他滨耐药组外周血、肿瘤组织和异种移植瘤中高表达。cNEK6通过促进PDAC糖酵解来增强对吉西他滨的耐药性。cNEK6阻止泛素化介导的SNRPA降解,SNRPA积累后通过结合PP2Ac mRNA的5'UTR中的G4结构来抑制PP2Ac的翻译,由于PP2Ac的缺失,mTORC1通路发生异常磷酸化和激活,进一步促进糖酵解过程并增强PDAC细胞对吉西他滨的耐药性。cNEK6表达水平与mTORC1通路的激活程度和糖酵解程度显著正相关。
研究表明cNEK6高表达患者在吉西他滨治疗中联合mTORC1抑制剂可抑制糖酵解,进而显著获益。
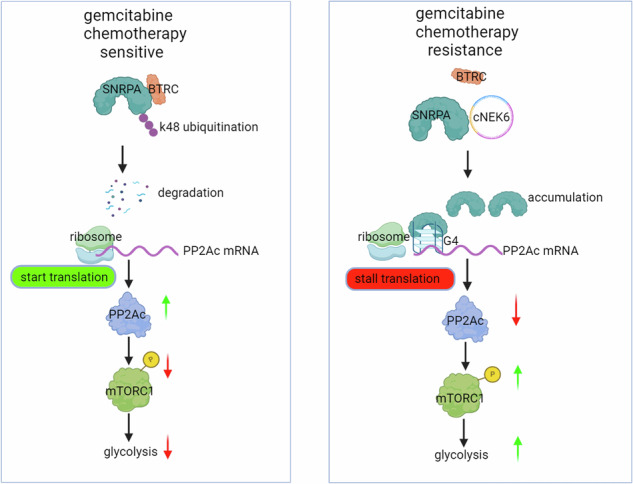
3-
10月14日, Signal Transduction and Targeted Therapy :上海交通大学医学院附属仁济医院谭蔚泓院士、孙洋教授、徐海燕教授提出核酸适体偶联药物(ApDC)负载细菌协同治疗胰腺癌新策略 [8]。
约70%的胰腺癌患者表现出“致密”的肿瘤微环境,其高密度结缔组织和高浓度细胞外基质不仅阻碍了药物的有效递送,还可能削弱化疗和其他治疗方式的有效性。
研究团队提出了一种新型协同疗法,利用了细菌的实体瘤穿透能力和ApDC的靶向和毒性作用,通过“点击化学”方法,将ApDC共价结合VNP20009。该组合方法可显著延长ApDC的血清稳定性至48小时,并导致肿瘤部位的药物浓度增加。此外,核酸适配体与癌细胞的靶向结合使肿瘤部位的细菌定植增加了两倍以上,导致肿瘤细胞死亡和T细胞浸润增加。
这种协同治疗策略实现了优化的药物递送、增强治疗效果和激活靶向免疫反应,为胰腺癌的治疗提供了一种有效的协同策略,具有广阔的应用前景。
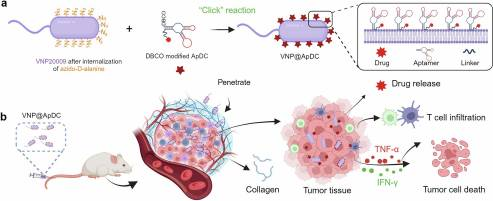
刊后语
大风泱泱,大潮滂滂;大道如砥,医者无疆。
积跬步以至千里,每一期周刊都是恶性肿瘤学科发展的剪影;积小流以成江海,一年周刊浓缩肿瘤领域各科前沿进展的精华!关注CACA周刊,带你领略恶性肿瘤学科发展的四季花开。
CACA周刊,我们下周不见不散!
编辑 | 李瑞源 丁凡
排版 | 晓晓
审核 | 李瑞源
链接:http://www.lewenyixue.com/2024/11/13/%E3%80%90CACA%E5%91%A8%E5%88%8A%E3%80%9181%E6%9C%9F%20%E5%9B%9B%E9%98%B4%E6%80%A7%E4%B9%B3%E8%85%BA%E7%99%8C%E2%80%94%E2%80%94/







赶快来坐沙发