Science丨乳腺癌通过神经信号通路绕过血脑屏障实现骨转移至脑膜
乳腺癌患者被诊断出转移至脑脊膜时,其中位生存期不到6个月。尽管最近在治疗脑实质转移方面取得了一些进展,但脑脊膜疾病的预后几乎没有改善。脑脊膜疾病有效靶向治疗发展的一个重大障碍是对调控在脑脊膜微环境中转移入侵和生存的分子机制了解有限,这种微环境在解剖学和免疫学上都是隔离的,且营养贫乏。有实验表明,乳腺癌细胞可以通过破坏脉络丛的血液-脑脊液屏障进入脑脊膜。脉络丛是位于大脑脑室内的脑脊液分泌上皮。然而,许多脑脊膜疾病患者并没有脉络丛受累的证据。
与营养丰富的骨髓环境相比,营养贫乏的脑脊膜环境对于生存来说是严酷的。肿瘤在这种环境下适应细胞压力的机制尚不完全清楚。此外,尽管脑脊膜中免疫细胞相对较少,但其中含有大量常驻巨噬细胞群。巨噬细胞在许多组织中具有促肿瘤作用;然而,乳腺癌细胞如何颠覆脑膜巨噬细胞以增强其在脑脊膜中的生存,目前研究较少。
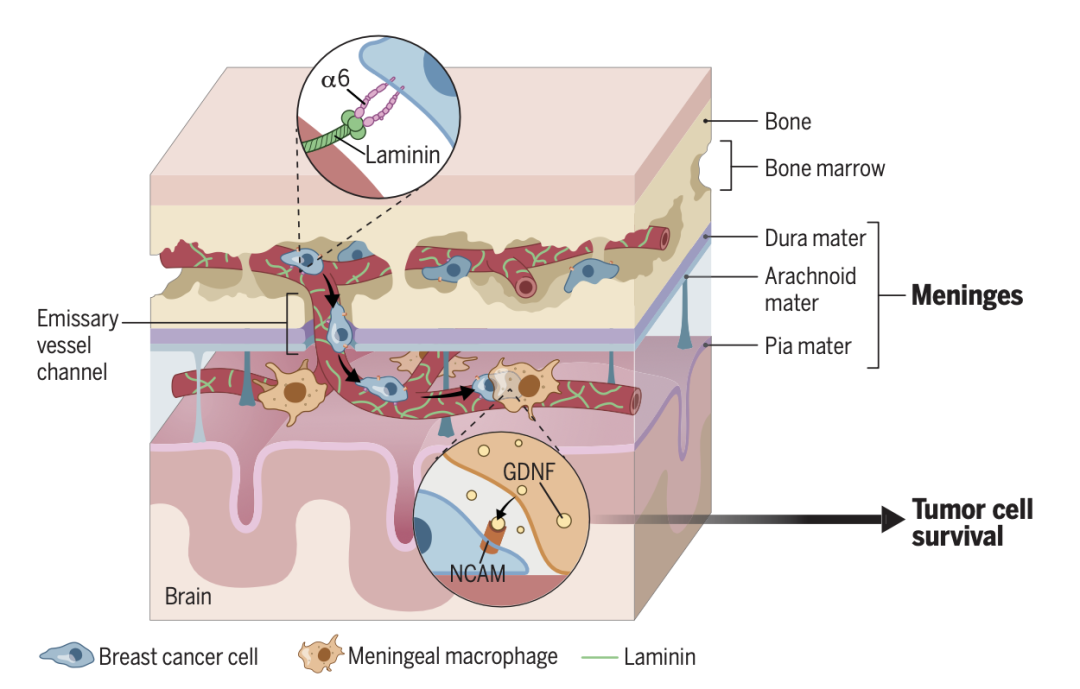
来自杜克大学的 Dorothy A. Sipkins 团队在 Science 上发表题为 Breast cancer exploits neural signaling pathways for bone-to-meninges metastasis 的文章。本文 发现乳腺癌细胞可以沿着富含层粘连蛋白的导静脉外表面迁移,从椎骨或颅骨骨髓进入脑脊膜,而无需穿过血脑屏障。这一过程依赖于乳腺癌细胞通过整合素α6与血管基底膜层粘连蛋白的结合。
作者将乳腺癌细胞系通过lentiviral转导标记上tdTomato-荧光素酶以及整合素α6过表达。这些标记和过表达的细胞系用于追踪肿瘤细胞在小鼠体内的迁移和生长,并研究整合素α6在脑脊膜转移中的作用。使SCID、C57BL/6和MacGreen小鼠,通过心内注射注入乳腺癌细胞,建立骨转移和脑脊膜转移模型。成功建立了乳腺癌骨转移和脑脊膜转移的小鼠模型,观察到了肿瘤细胞在脑脊膜中的浸润和生长。接下来作者通过CRISPR-Cas9技术敲除整合素α6基因,并用流式细胞术和Western blot确认敲除效果。敲除整合素α6显著减少乳腺癌细胞在脑脊膜中的迁移和生长,表明整合素α6在肿瘤细胞侵袭中的关键作用。
作者使用颅骨变薄技术进行高分辨率成像,定位脑脊膜中的肿瘤细胞分布。并同时通过免疫组化、流式细胞术和RT-qPCR等方法进行数据分析。成像和分析结果显示,乳腺癌细胞通过沿导静脉外表面迁移进入脑脊膜。进入脑膜后,大多数乳腺癌细胞与巨噬细胞共定位,并且这些乳腺癌细胞的存在刺激了巨噬细胞分泌神经细胞存活分子,即胶质细胞源性神经营养因子 (glial-derived neurotrophic factor GDNF) 。GDNF在健康成年人的大脑和脑膜中的表达极少,但在脑损伤中,胶质细胞和巨噬细胞可以分泌GDNF。
作者接下来利用CSF1R特异性GDNF敲除小鼠,通过PLX5622 (CSF1R抑制剂) 进行处理,并使用GDNF中和抗体进行体内和体外GDNF阻断实验。阻断GDNF信号、特异性敲除巨噬细胞中的GDNF,或从乳腺癌细胞中敲除GDNF受体NCAM,都显著抑制了乳腺癌在脑脊膜中的生长,表明GDNF在肿瘤细胞生存中的关键作用。
本研究发现, 乳腺癌细胞可以通过沿导静脉外表面迁移从骨髓进入脑脊膜,依赖于整合素α6与层粘连蛋白的结合。一旦进入脑脊膜,肿瘤细胞通过诱导脑膜巨噬细胞分泌GDNF来增强其生存能力。这些发现为开发针对整合素α6和GDNF信号轴的治疗策略提供了新的靶点,具有重要的临床意义。
https://www.science.org/doi/10.1126/science.adh5548
制版人:十一
版权声明:本文为“乐问号”作者或机构在乐问医学上传并发布,仅代表该作者或机构观点,不代表乐问医学的观点或立场,不能作为个体诊疗依据,如有不适,请结合自身情况寻求医生的针对性治疗。
链接:http://www.lewenyixue.com/2024/08/06/Science%E4%B8%A8%E4%B9%B3%E8%85%BA%E7%99%8C%E9%80%9A%E8%BF%87%E7%A5%9E%E7%BB%8F%E4%BF%A1%E5%8F%B7%E9%80%9A%E8%B7%AF%E7%BB%95/
THE END






赶快来坐沙发