抑制肿瘤生长和复发!中山大学苏中振团队:治疗“最毒乳腺癌”的多功能纳米药物
作者:Jerry
导读: 临床上高度侵袭性三阴性乳腺癌(TNBC)的治疗具有挑战性。
7月25日,中山大学苏中振研究团队在期刊《Advanced Science》上发表了研究论文,题为“19F MRI/CEUS Dual Imaging-Guided Sonodynamic Therapy Enhances Immune Checkpoint Blockade in Triple-Negative Breast Cancer”,本研究中,研究人员开发了一种脂质体纳米药物(LP@PFH@HMME),将显像剂和治疗剂结合在一起,用于双模态成像引导的声动力治疗(SDT)。该药物可增强免疫原性,从而通过免疫检查点阻断(ICB)对三阴性乳腺癌进行有效的免疫治疗。在酸性肿瘤微环境(TME)中,由于PH响应性脂质融合,LP@PFH@HMME发生了“纳米-微”转化,这使得液滴在超声造影(CEUS)和SDT研究中对超声(US)更加敏感。该纳米药物通过氟-19磁共振成像(19F MRI)和超声造影双模态成像显示出稳健的双模态成像能力,在19F含量较高的水溶液中表现出良好的溶解性和较长的横向弛豫时间(T2 = 1.072 s),适用于高性能的19F MRI,此外尾静脉注射后纳米药物可有效蓄积。因此,19F MRI/CEUS双重成像可以显示超声辐照肿瘤部位的足够时间点,从而诱导高效的SDT,产生大量的活性氧(ROS)触发免疫原性细胞死亡(ICD),以辅助基于ICD的免疫治疗。 声动力联合免疫治疗的治疗设计有效抑制了TNBC的生长和复发,凸显了多功能纳米药物治疗TNBC的前景。

https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202401182
研究背景
01
三阴性乳腺癌(TNBC)是一种全球流行的恶性肿瘤,预后极差。约46%的患者发生远处转移,突显了TNBC的高侵袭性。可是,转移后的中位生存时间仅为13.3个月,而且术后复发率飙升至惊人的25%。目前仍缺乏高效、规范的TNBC治疗方案。近年来,基于免疫检查点阻断(ICB)的免疫治疗,包括抗CTLA4治疗和PD-L1/PD-1治疗,在多种肿瘤中显示出良好的治疗效果。遗憾的是,只有一部分TNBC患者对ICB治疗表现出有效的抗肿瘤应答,在未经选择的患者中,缓解率约为5%,在接受帕博利珠单抗治疗的初治pd - l1阳性患者中,缓解率约为23%。因此,迫切需要开发新的策略,通过有效增强TNBC患者的免疫应答来实现实质性的治疗获益。目前,化疗、放疗、光动力疗法(PDT)、声动力疗法(SDT)联合ICB已显示出协同抗肿瘤作用。其中,SDT作为一种超声介导的治疗技术,作为一种潜在的肿瘤治疗方法受到了相当大的关注。SDT可通过产生活性氧(ROS)诱导癌细胞发生免疫原性细胞死亡(ICD),导致肿瘤抗原暴露增加,促进树突状细胞(DC)抗原提呈。这进而启动抗肿瘤免疫级联反应,以增强ICB治疗的疗效。
为了优化超声成像的效果,传统的超声造影剂,如SonoVue,通常是微型的。然而,这些微泡在超声上表现出增强的回声对比,在穿透肿瘤渗漏的血管系统时经常遇到挑战。遗憾的是,对于有效的癌症治疗,理想的纳米药物需要相对较小的尺寸(100 - 400nm),以便通过增强渗透性和滞留性(EPR)效应来延长血液循环和在肿瘤中的积累。因此,开发一种智能纳米平台,在肿瘤微环境(TME)的响应下进行自发的“纳米微”生长,将是解决一个纳米给药系统中成像和治疗困境的一个非常有益的策略。例如,由于胆固醇(Chol)的ph响应性脂质融合,纳米药物可以被设计成在酸性TME中经历“纳米到微”的转化。对于双重成像,全氟碳化合物最近成为19F MRI和CEUS的有价值的试剂。其中,全氟己烷(PFH)脂类由于其沸点升高(≈56°C),在体内具有相对较高的稳定性。一旦在超声(US)照射下,PFH脂质迅速气化,产生用于超声造影成像的空化力。
体内抗肿瘤治疗效果
02
由于有前景的体外结果证明了ICD的抗肿瘤疗效和免疫激活,研究人员扩大了研究范围,在4T1荷瘤小鼠中评估了基于LP@PFH@ hmme的SDT及其与ICB的联合的体内抗肿瘤效应。研究人员将小鼠随机分为5组:PBS组、LP@PFH@HMME组、aPD-L1组、US + LP@PFH@HMME组和US + LP@PFH@HMME + aPD-L1组。接种后第7天,当肿瘤体积达到约100 mm3时,采用尾静脉注射的方式给药,之后每3 d给药1次。每次静脉注射后12 h给予US照射,aPD-L1组和US + LP@PFH@HMME + aPD-L1组分别于第4、6、8天腹腔注射aPD-L1抗体。如图1B,C所示,与PBS组和LP@PFH@HMME组的快速生长相比,aPD-L1单药治疗组的肿瘤生长明显受到抑制。值得注意的是,US + LP@PFH@HMME治疗显著抑制肿瘤生长,强调了LP@PFH@HMME在US照射下治疗效果的特异性。尤其是,US + LP@PFH@HMME + aPD-L1的联合治疗显示出最有效的肿瘤生长抑制作用。生存分析结果与肿瘤生长抑制结果一致。尽管US + LP@PFH@HMME和US + LP@PFH@HMME + aPD-L1组均显示出对小鼠生存期的有利影响,但US + LP@PFH@HMME + aPD-L1治疗似乎在延长动物生存期方面最有效。此外,所有治疗组小鼠的体重没有显著变化。
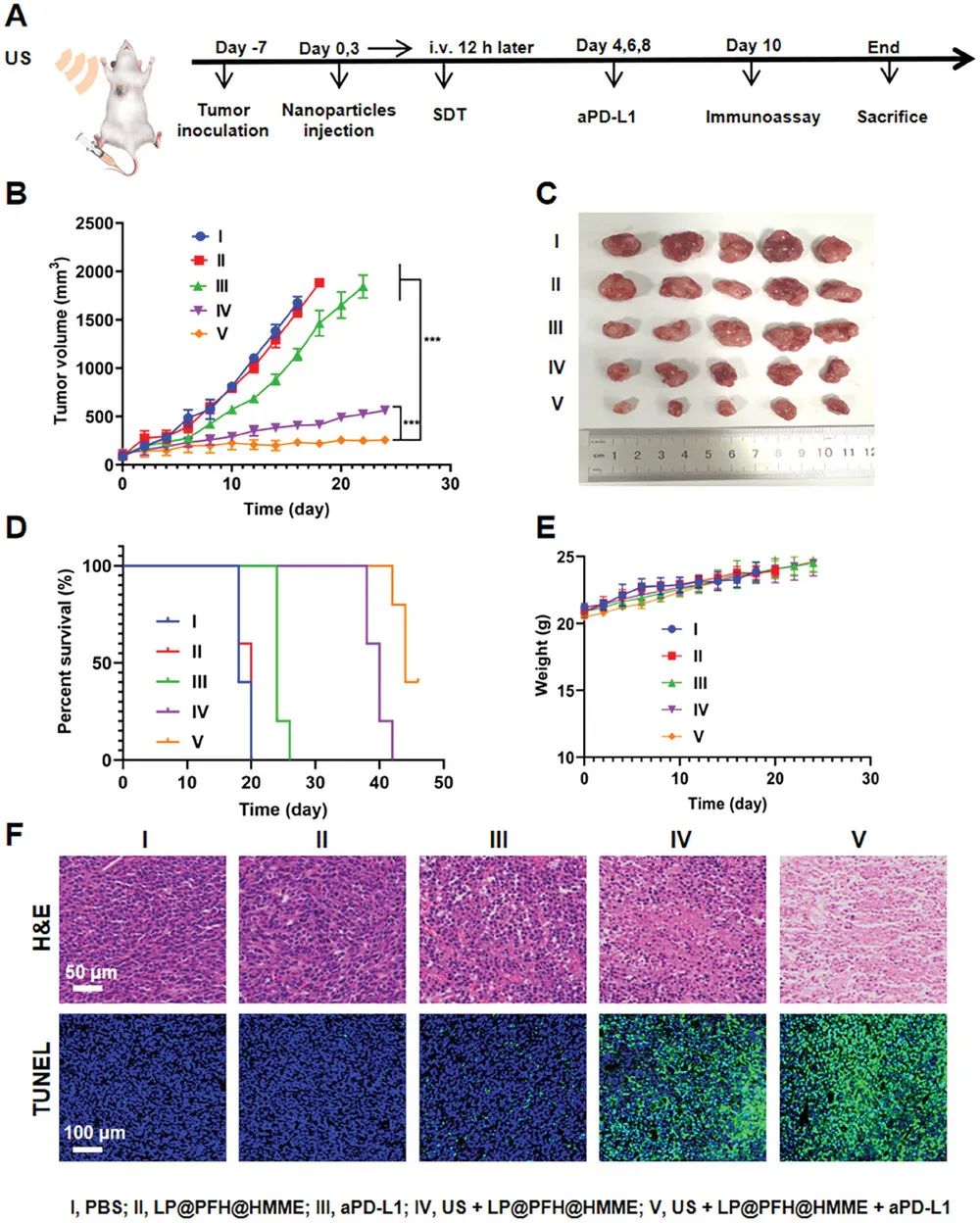
图1:基于LP@PFH@ hmme的声动力免疫疗法的体内抗肿瘤治疗效果
主要器官的血红素-伊红(H&E)图像未显示明显的全身毒性病理征象。治疗组与PBS组血清生化指标无显著差异。这些结果强调了基于纳米药物的SDT和免疫治疗联合治疗的高治疗性生物安全性。基于纳米药物的SDT和免疫疗法的协同治疗效果通过组织病理学评估进一步得到证实。H&E染色和TUNEL染色检测肿瘤组织,发现US + LP@PFH@HMME + aPD-L1治疗组的凋亡和坏死细胞比例最高,说明SDT + ICB联合治疗方式取得了显著的治疗效果。
研究小结
03
联合使用aPD-L1阻断PD-L1检查点,LP@PFH@HMME在超声照射下诱导有效的抗肿瘤免疫激活和免疫记忆效应,从而抑制TNBC的肿瘤生长和复发。此外,显像剂PFH的加入使诊疗用纳米药物具有较长的横向弛豫时间(T2 = 1.072 s)和双模态成像能力(19F MRI/CEUS),从而有利于肿瘤的可视化和纳米药物在肿瘤部位的蓄积,为SDT治疗三阴性乳腺癌提供了重要的指导。因此,LP@PFH@HMME融合了19F MRI/CEUS双影像引导SDT和ICB治疗的多功能,有望成为TNBC治疗的有效平台。
参考资料:
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202401182
链接:http://www.lewenyixue.com/2024/07/30/%E6%8A%91%E5%88%B6%E8%82%BF%E7%98%A4%E7%94%9F%E9%95%BF%E5%92%8C%E5%A4%8D%E5%8F%91%EF%BC%81%E4%B8%AD%E5%B1%B1%E5%A4%A7%E5%AD%A6%E8%8B%8F%E4%B8%AD%E6%8C%AF%E5%9B%A2%E9%98%9F%EF%BC%9A/




 知道|国家药品不良反应监测年度报告(2024年)
知道|国家药品不良反应监测年度报告(2024年)
赶快来坐沙发