GOG-3015试验:指明了卵巢癌免疫治疗的一个研究方向
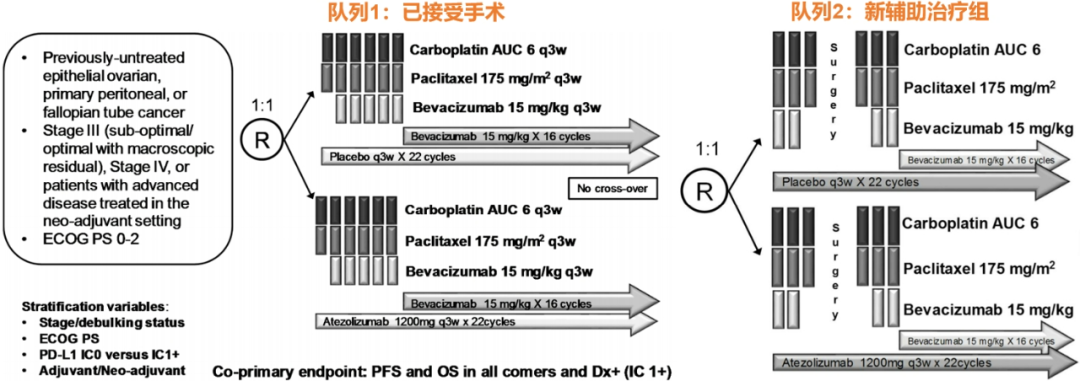
之前写过一篇文章: 重温GOG-3015试验:细分可能从免疫治疗中获益的卵巢癌亚组人群 ,在这篇文章中,我们详细分析了该试验于2021年发表于《Journal of Clinical Oncology》的 PFS结果,强烈建议在阅读本文之前,先点击链接回顾之前的内容,以便更好地理解本试验的内容。
-
全人群和PD-L1 IC≥1% 人群的PFS均为阴性结果;PD-L1 IC≥1%人群的PFS有获益趋势 (HR始终<1) ,但未达统计学意义 (P值大于预设的界值) 。(IC:Immune cell,免疫细胞阳性比例分数) -
把IC的界值提高至5,在PD-L1 IC≥5%的人群中做了分析,结果显示在这部分人群中,免疫治疗具有明显的获益趋势:对照组的mPFS是20.2月,免疫治疗组的mPFS未达到,但其95%置信区间的下限就已达到20.8月;HR值始终<1;两条曲线从治疗的一开始就已明显分开。 -
研究者又使用TC的标准评价PD-L1,然后做了一下事后分析(TC:Tumor cell,肿瘤细胞阳性比例分数),依然看到了这部分卵巢癌患者从免疫治疗中获益的明显趋势。对照组的mPFS为15.0月,其95%置信区间的上限也只有20.8月;免疫治疗组的mPFS未达,但其95%置信区间的下限都已达到22.1月,高于对照组的上限;HR值始终<1。
我们知道,OS才是评价肿瘤治疗的金标准,PFS能否替代OS,这是有争议的。那么,今天我们再继续回顾本试验的OS结果,该结果于2023年发表于《Gynecologic Oncology》。
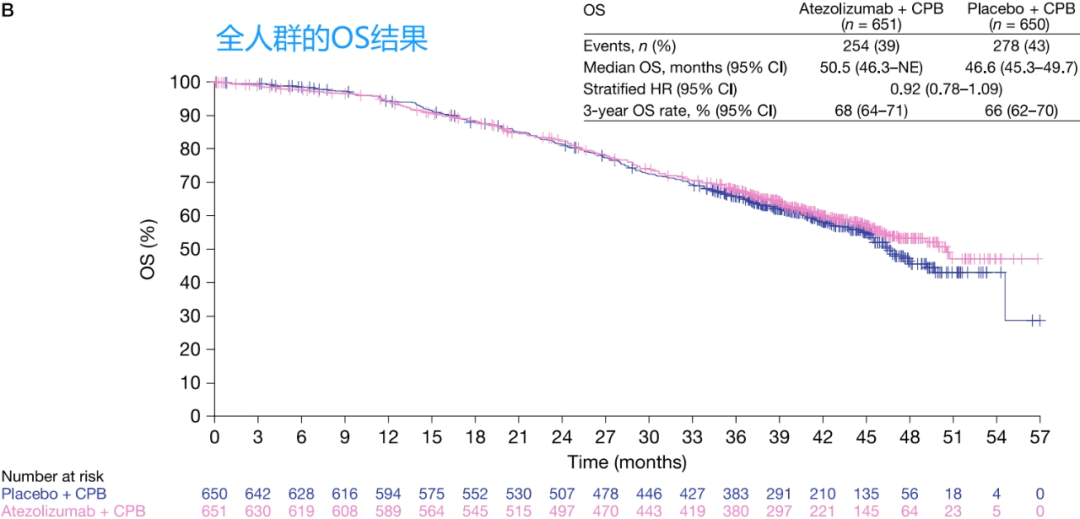
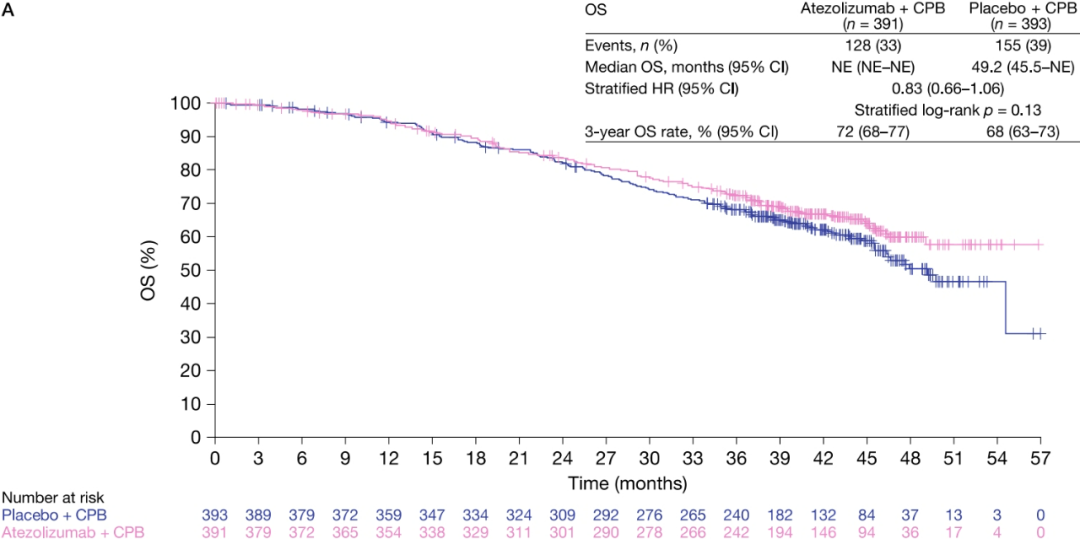
-
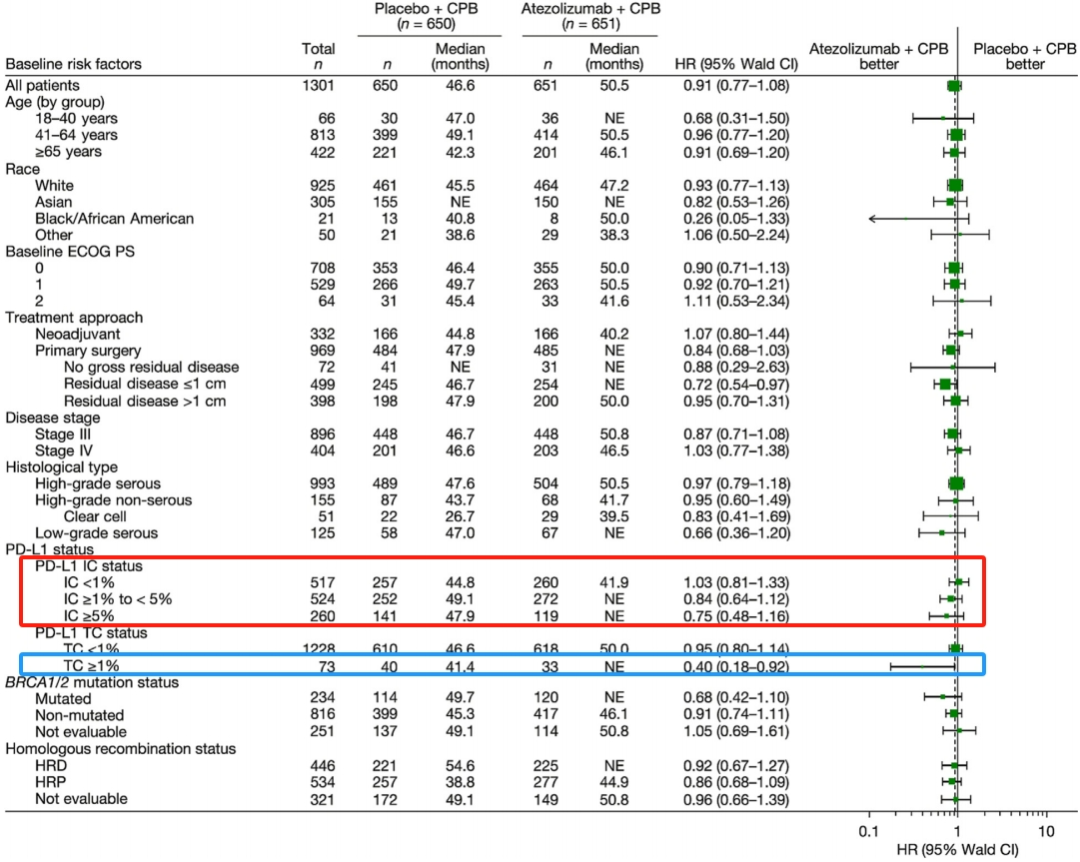
PD-L1 IC的界值越高,患者越能从免疫治疗中获益(HR值从1.03到0.84、再到0.75,HR值越小,即死亡风险越小)。 (下图的红色框) -
与PFS结果一致,如果采用TC评价PD-L1,那么在PD-L1 TC≥1%的患者中,OS也有明显的获益趋势,HR值=0.40,降低了60%的死亡风险,HR的95%置信区间为0.18-0.92,始终小于1,死亡风险始终低于安慰剂组。 (下图的蓝色框)


那么,本试验给我们什么样的研究方向?
1.既然随着PD-L1 IC界值的提高,患者获益趋势越大,那何不直接筛选IC高的患者进行临床试验?比如IC>10%?甚至>20%?
目前免疫疗法在卵巢癌已有多个大三期试验,包括阿替利珠单抗的ENGT-O29试验和ANITA试验,阿维鲁单抗的JAVELIN Ovarian 200试验、JAVELIN Ovarian 100试验和JAVELIN OVARIAN PARP 100 试验,以及度伐利尤单抗的DUO-O试验,他们在OS方面均未取得阳性结果; 但我们知道这些试验的主要终点都是在全人群或PD-L1阳性人群中评估,而均未将PD-L1高表达的人群作为主要终点人群。
这个其实可以参考乳腺癌的Keynote-355试验。该试验比较了帕博利珠单抗联合化疗 vs 安慰剂联合化疗 一线治疗复发或转移性三阴性乳腺癌患者的疗效和安全性,主要终点就包含了三类人群:全人群、PD-L1 CPS≥1和CPS≥10。结果在全人群和PD-L1 CPS≥1的人群中,PFS和OS都没有显著获益,而在PD-L1 CPS≥10的人群中取得了阳性结果,帕博利珠单抗也因此在FDA获得了该人群的一线适应症。
2.如前面所分析,如果使用TC评价PD-L1,那在PD-L1 TC≥1%的患者中,PSF和OS均有明显的获益趋势。但是,遗憾的是,本试验中PD-L1 TC阳性的患者数量较少,一共有73例是PD-L1 TC≥1% ,包括试验组33例、对照组40例。

所以,这就带给我们第二个研究方向:我们能否开展一个类似的试验,但是只纳入PD-L1 TC阳性的人群,并且适当增加、扩展样本量,以此进一步验证免疫联合疗法能否为这部分人群带来生存获益。
总之,尽管GOG-3015试验的主要终点是阴性结果,但是我们依然能从亚组分析中看到一些潜在的获益人群,至于这些获益趋势是否具有统计学意义,就需要进一步的研究来验证,也因此给了我们一些可能的研究方向。同时,换一句话说,在没有针对潜在获益人群进一步开展研究验证之前,似乎并不能完全下结论说所有的卵巢癌患者都不能从免疫治疗中获益。
我们期待相关研究的开展。
链接:http://www.lewenyixue.com/2024/05/15/GOG-3015%E8%AF%95%E9%AA%8C%EF%BC%9A%E6%8C%87%E6%98%8E%E4%BA%86%E5%8D%B5%E5%B7%A2%E7%99%8C%E5%85%8D%E7%96%AB%E6%B2%BB/