重磅综述:人工智能在体外肿瘤建模和肿瘤微环境表征中的应用
今天我们来介绍一篇关于 人工智能助力 体外肿瘤建模和 肿瘤微环境相关研究 的综述,该文章发表在Advanced Healthcare Materials上,题目为“ Application of Artificial Intelligence to In Vitro Tumor Modeling and Characterization of the Tumor Microenvironment ”, 体外肿瘤模型在增强对肿瘤细胞和分子组成及其生化和生物物理特征的理解方面发挥了至关重要的作用。技术的进步使肿瘤模型从二维细胞培养物演变为三维打印肿瘤模型,其复杂性和输出参数也越来越多样化。随着复杂性的增加, 新一代模型能够比其前面的研究模型更真实地复制肿瘤微环境的结构和异质性 。近年来,人工智能(AI)在医疗保健和研究中得到了广泛的应用,基于人工智能的工具也被应用于肿瘤模型的精确开发。人工智能的结合促进了高通量系统的使用,用于实时监测肿瘤发生和生物物理肿瘤特性,提高了将人工智能与肿瘤建模结合使用以实现个性化医疗的可能性。这篇文章回顾了人工智能工具在肿瘤建模中的集成,包括 微流控设备和肿瘤芯片模型 ,以更好的 探究肿瘤微环境 。
论文原文链接: https://doi.org/10.1093/eurheartj/ehad736
1. 背景介绍
肿瘤具有高度异质性,其特征取决于 肿瘤微环境(TME) 中的细胞相互作用。正常细胞与肿瘤微环境之间的相互作用可维持组织稳态,而肿瘤细胞与肿瘤微环境之间的相互作用则可导致细胞重编程,从而使肿瘤微环境发生进化,支持肿瘤发生和耐药性。由于肿瘤细胞和免疫细胞处于异质环境中,深入了解和描述TME可能有助于发现改善患者管理策略的机制和生物标志物。因此,人们一直在努力开发能模拟癌症生物学中TME的肿瘤模型。此类模型使我们能够在受控条件下 量化药物敏感性和代谢变化,从而测试治疗方法的有效性 。
2. 体外肿瘤建模技术
由于人工智能技术的不断发展,体外肿瘤模型近年来取得了显著进展,从最初的2D细胞培养发展到现在的3D-TME模型。3D模型旨在通过结合3D细胞间/ECM相互作用、组织刚度、营养转运、代谢废物和氧梯度来概括TME的全部细节。
3. TME分析工具
一个设计良好的肿瘤模型提供了一个可控的TME,这反过来又促进了对复杂肿瘤系统的研究。为此,免疫分析工具可以准确量化表征体外肿瘤模型TME特性的各种生物因素。基于组织的技术,为TME中DNA、RNA和蛋白质水平的分子变化提供了前所未有的见解。因此,它可以更好地了解肿瘤组织内分子改变的原位细胞背景,并通过发现新的生物标志物和治疗靶点大大加速转化性癌症的研究。其中 包括多重免疫组化、质控细胞成像技术和空间转录组三个主要技术着力点。
多重免疫组化(mIHC)扩展了可用于荧光标记或金属同位素标记测定的标记数量,用于空间蛋白质组学分析。在mIHC中,荧光标记使用附着在二抗上的荧光团来筛选感兴趣的标记物,而基于金属的方法使用激光扫描或离子束来检测金属同位素代替荧光团。进而可以表征免疫细胞和标记物的相对空间分布,揭示免疫细胞、癌细胞和基质细胞之间的重要相互作用。通过mIHC在一张载片上同时量化6个或更多的标记物,可以进行深度免疫表型分析,并有助于更深入地了解癌症的诊断和进展,以及预后和治疗结果预测。多项研究证实了mIHC的可重复性和有效性,并强调了该技术在肿瘤中增殖细胞和其他标志物鉴定中的潜在应用。除了允许在单个样品中检测多个标记物外,mIHC还提供有关细胞组成和空间排列的全面信息。下图为利用多重免疫组化和硅学方法确定肿瘤免疫微环境实现精准免疫疗法的全流程。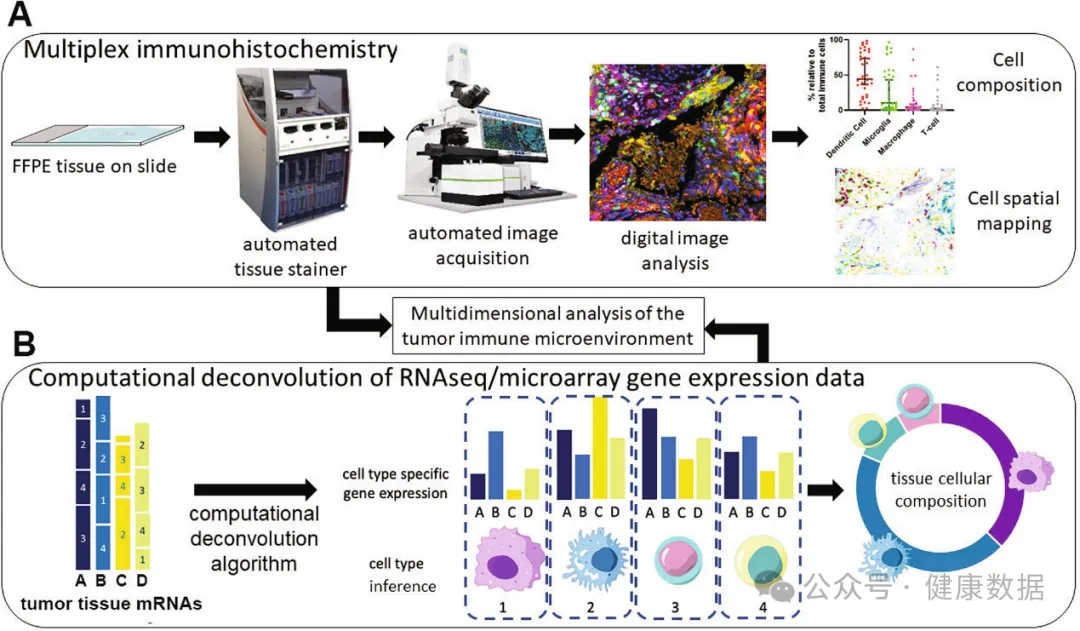
图片来源于 DOI: 10.1038/s42256-022-00471-x
质控细胞成像技 术(IMC) 用于通过将IHC染色与金属同位素标记的抗体、高分辨率激光消融和基于飞行时间质谱(MS)的检测相结合来产生高维图像。这允许同位素的空间映射和随后的分析使用数字分析工具,如historat。通过促进重要免疫细胞的识别和提供治疗相关的空间信息,多路复用技术可以提高我们对肿瘤进化的理解,从而有助于肿瘤模型的工程设计。结合真实的肿瘤建模技术,这些方法可以促进诊断和预后生物标志物的识别。此外,将自动化集成到医学成像中,提高了图像采集和分析的速度,并减少了使用所得图像划定肿瘤区域所需的时间。这种诊断和治疗计划的技术使得这个过程比手工的更健壮,更容易复制。此外,自动图像采集分析也可以在体外应用。
空间转录组学(ST) 技术的出现使得TME的无偏谱分析成为可能,与空间蛋白质组学(SP)技术测量蛋白质相反,它允许测量数百到数万个RNA转录物。这些技术使得可以在样本中分析的RNA种类的数量大大增加。ST技术可分为基于成像的方法和基于下一代测序(NGS)的方法。由于新技术的快速发展,转录空间分析技术的分辨率、灵敏度、通量和可及性不断得到改进。这些改进将有助于识别存在于抗癌治疗无效的患者群体中的基因和生物分子。此外,随着对癌细胞进化的深入了解,临床医生将更好地尽早发现癌症并识别潜在的耐药机制,进一步帮助临床医学发展精准靶向治疗。
4. 人工智能在TME分析中的应用
肿瘤分析的组织病理学方面已被证明对我们了解肿瘤进展至关重要。通常,数以万计甚至数以百万计具有不同表型特征的细胞进行分析,其中每个细胞和亚细胞区室可以被描绘为数千个基因和多种蛋白质测量。因此,对于高维大数据的分析,人工智能的引入是必不可少的。人工智能在TME分析中的关键应用,包括但不限于 (i)疾病诊断,(ii)生物标志物检测, (iii)免疫结构表征,[110](iv)硅染色预测,[111]和(v)全片图像标准化 。应用AI进行肿瘤微环境(TME)分析的研究实例如下表所示。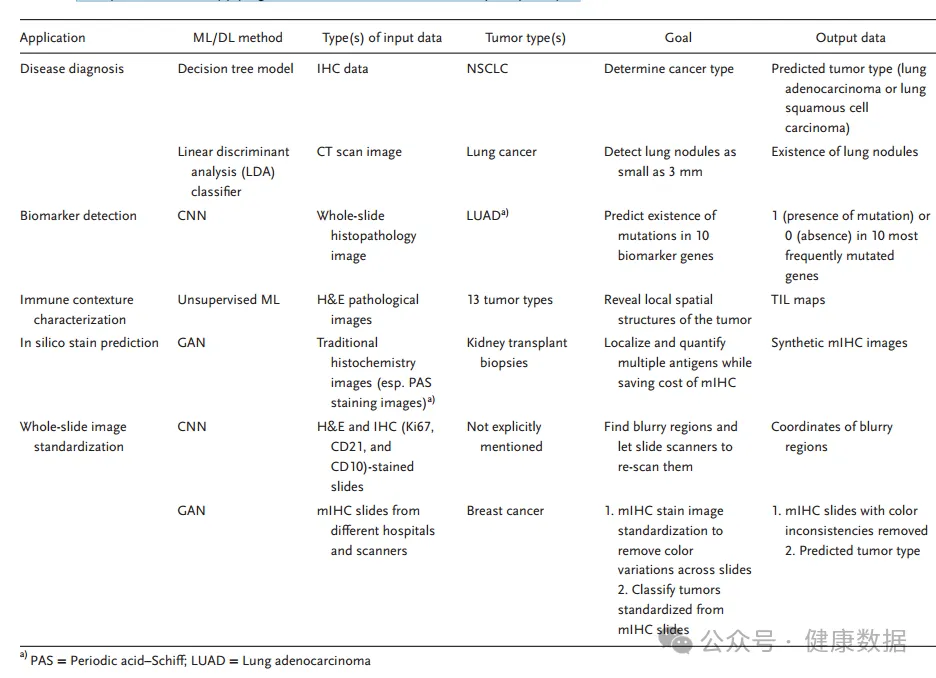
5. 人工智能在体外肿瘤建模中的应用
实现高精度的微尺度结构(即片上结构)需要对材料特性和打印参数进行精细控制,人工智能应用为精度和效率提供了新的机会。应用越来越多地部署在3d打印过程中,包括 (i)工艺优化(流变特性、喷嘴规格、喷嘴温度、路径高度和油墨成分的影响),(ii)制造缺陷的检测,(iii)尺寸精度的评估,以及(iv)材料特性的预测 。其主要应用如下表所示。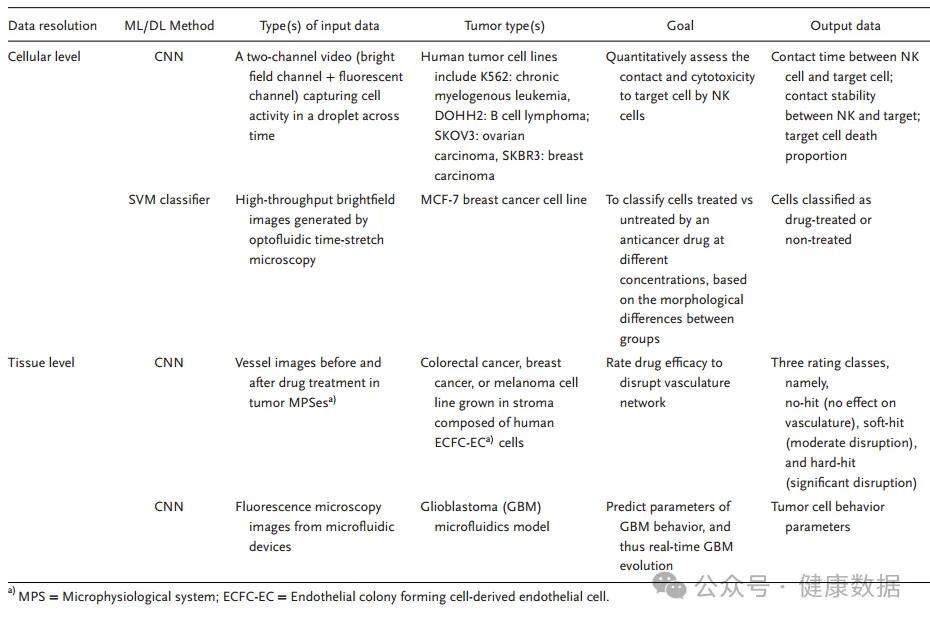
高保真肿瘤模型 构成了与真实肿瘤及其微环境非常相似的可控生物物理系统。通过部署先进的数据测量技术和人工智能支持的数据分析,这些模型除了详细表征和预测肿瘤生长和免疫逃避之外,还为高通量药物筛选和生物标志物发现开辟了新的机会。
6. 总结
将人工智能应用于肿瘤模型将使高通量系统能够实时建模和监测肿瘤发生和生物物理肿瘤特性,并进行大型数据集分析。尽管越来越多的人工智能技术被开发来解决TME分析和肿瘤建模中的上述挑战,但流行的ML和DL方法有一些局限性。这些包括对时间和硬件资源的高要求,对模型训练的大输入数据集的要求,以及许多深度学习方法的原始结果不是直观的,需要专业知识来准确解释它们的原始结果。 最新开发的Transformer具有更小的模型参数尺寸,从而大大缓解了前两个限制 。我们相信,在不久的将来,所有这三个限制都可以通过新的ML和DL方法来解决,这些方法具有更简单的模型架构以及更直观的模型假设和输出结果。总而言之,在肿瘤建模工作中整合新颖而强大的人工智能方法将为检查TME中未探索的区域和相互作用提供额外的机会。
来源 | HealthIT
链接:http://www.lewenyixue.com/2024/04/30/%E9%87%8D%E7%A3%85%E7%BB%BC%E8%BF%B0%3A%E4%BA%BA%E5%B7%A5%E6%99%BA%E8%83%BD%E5%9C%A8%E4%BD%93%E5%A4%96%E8%82%BF%E7%98%A4%E5%BB%BA%E6%A8%A1%E5%92%8C%E8%82%BF%E7%98%A4%E5%BE%AE/







赶快来坐沙发